AAV 在肾脏疾病研究中的应用
派真生物
肾脏疾病是威胁人类健康的主要疾病之一,全球约有 13% 人口受其影响。目前对肾脏疾病的干预措施包括透析和肾脏移植,这些措施的效果或可用性有限,并且通常会引起各种并发症如心血管疾病和免疫抑制等。因此,迫切需要为肾脏疾病开发新的治疗方法。
值得注意的是,高达 30% 的肾脏疾病病例是由单基因疾病引起的,故基因药物治疗可能对此有所帮助;但由于肾脏结构和功能的复杂性,针对肾脏疾病的基因治疗的研究和开发滞后于肝脏、神经肌肉和眼睛等,目前还没有任何一种针对肾脏的基因治疗药物获批上市。
AAV 是目前体内基因治疗最合适的载体,已有研究人员利用 AAV 进行体内外肾脏的基因递送研究,并取得一定的成果。我们相信如何用 AAV 靶向肾脏是部分老师关心的重点问题。本文将详细介绍肾脏研究中针对不同细胞,如何选择不同的血清型和启动子,以及 AAV 导入肾脏的方式,希望能够帮助从事相关研究的老师获得有用的实验信息,节约宝贵的时间。
案例一、AAV 基因疗法治疗由 NPHS2 基因突变引起的肾病综合征[1]
足细胞是肾脏中的一种细胞类型,其基因突变(如 NPHS2 基因)是儿童遗传性肾病综合征的常见原因。这篇文章旨在探索用 AAV 基因疗法治疗由 NPHS2 基因突变引起的肾病综合征。

实验设计
AAV-LK03 和 AAV 2/9 的选择:研究者比较了 AAV-LK03 和 AAV 2/9 两种血清型在人类和鼠类足细胞中的转导效率。
体外实验:通过体外培养的突变人类足细胞中来测试基因疗法的效果。
体内实验:在诱导型足细胞蛋白(Podocin)敲除小鼠模型中测试疾病诱导前(预防性)的基因治疗效果,在诱导型突变 Podocin 敲入小鼠中测试疾病诱导后(治疗性)的基因疗法效果。
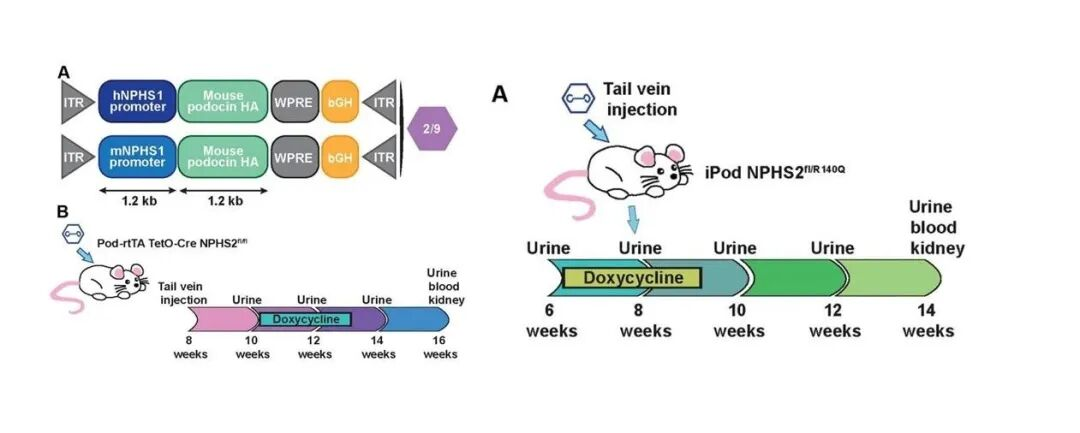
图 4 体内实验设计示意图
实验结果
AAV-LK03 的高效转导:在体外实验中,AAV-LK03 是人类足细胞的高效转导剂。
功能恢复:AAV-LK03 介导的足细胞蛋白在突变人类足细胞中实现了功能恢复。
预防性策略的效果:在诱导型 Podocin 敲除小鼠模型中,AAV 治疗组小鼠的尿白蛋白/肌酐比(ACR)、血清肌酐和尿素水平显著降低,血清白蛋白水平有所升高。肾组织显示出较少的肾小球硬化和间质纤维化,与生理盐水组相比,AAV 治疗组的肾小球足突结构较为正常。
治疗性策略的效果:在诱导型突变 Podocin 敲入小鼠中,AAV 治疗组小鼠的尿白蛋白/肌酐比(ACR)显著降低,血清白蛋白水平有所升高,血清肌酐和胆固醇水平没有显著变化,肾组织显示出较少的肾小球硬化和间质纤维化,足突结构恢复较好。
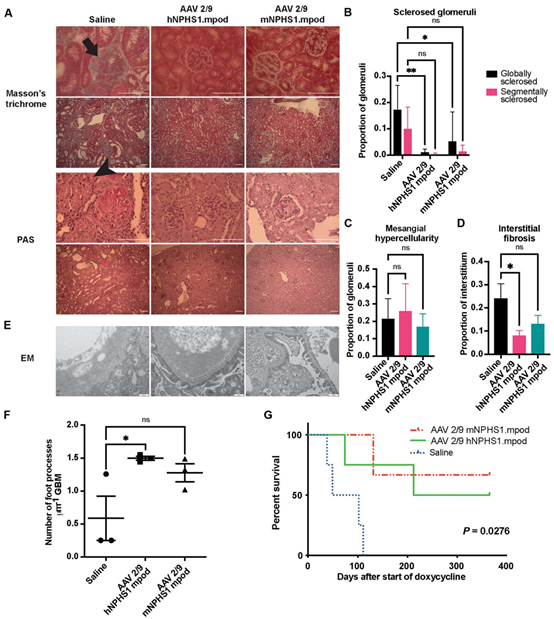
图 5 接受生理盐水或 AAV 处理的 Pod-rtTA TetO-Cre NPHS2fl/fl 小鼠的肾脏组织学和存活情况,这些小鼠在疾病诱导之前接受了治疗。
案例二、miR-29b 用于治疗肾脏纤维化的概念验证[2]
慢性肾病(CKD)是一种进行性疾病,其特征是肾功能逐渐丧失,最终可能导致需要肾脏替代治疗或肾移植。肾脏纤维化是 CKD 患者几乎普遍存在的一种病理变化。已有研究结果显示 miR-29b 可以抑制肾纤维化,因此 miR-29b 替代疗法可能是肾纤维化治疗的有效方法。这篇文章主要研究 miR-29b 用于肾脏纤维化基因治疗的可行性。

实验设计
确定最适合肾脏靶向基因递送的 AAV 血清型。
体外实验:在正常大鼠成纤维细胞、NRK-49F、TEC 和 NRK-52E 细胞中评估 miR-29b 对 TGF-β1 诱导的肾细胞纤维化的影响。
体内实验:在 UUO 小鼠模型中评估 miR-29b 对肾脏纤维化的影响。
实验结果
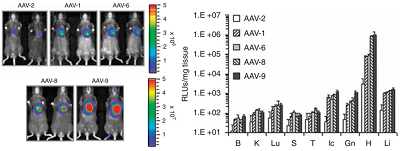
AAV 血清型选择:体外细胞实验结果显示 rAAV1、2 和 6 是适合靶向肾细胞的 AAV 血清型,小鼠体内实验结果显示 rAAV6 是最合适的载体。
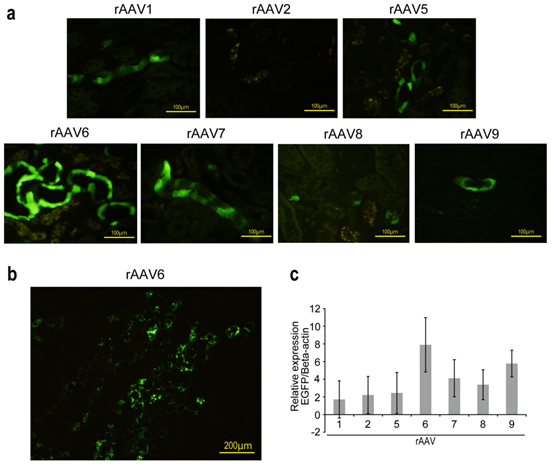
图 6 rAAV6 载体适合在小鼠体内进行肾脏靶向基因递送
miR-29b 对肾脏纤维化的影响:miR-29b 在体外抑制了 TGF-β1 诱导的肾细胞纤维化。在 UUO 小鼠模型中,rAAV6 介导的 miR-29b 递送可以抑制肾脏纤维化和 Snail1 的表达。
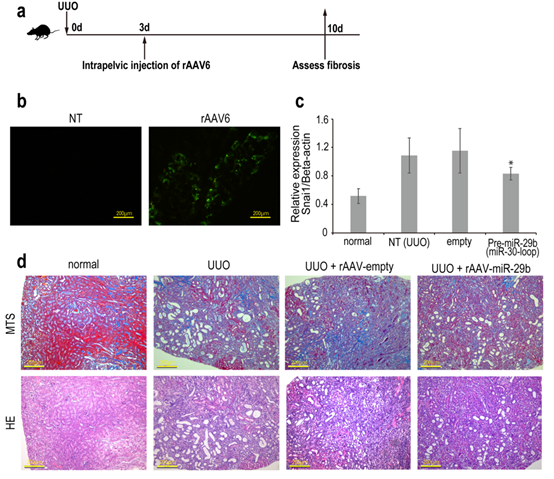
图 7 rAAV6 介导的 miR-29b 递送可以抑制 UUO 小鼠模型中的肾纤维化
[1]Ding WY, Kuzmuk V, Hunter S, Lay A, Hayes B, Beesley M, Rollason R, Hurcombe JA, Barrington F, Masson C, Cathery W, May C, Tuffin J, Roberts T, Mollet G, Chu CJ, McIntosh J, Coward RJ, Antignac C, Nathwani A, Welsh GI, Saleem MA. Adeno-associated virus gene therapy prevents progression of kidney disease in genetic models of nephrotic syndrome. Sci Transl Med. 2023 Aug 9;15(708):eabc8226.
[2]Saito S, Ohno SI, Harada Y, Oikawa K, Fujita K, Mineo S, Gondo A, Kanno Y, Kuroda M. rAAV6-mediated miR-29b delivery suppresses renal fibrosis. Clin Exp Nephrol. 2019 Dec;23(12):1345-1356.