万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 提供商:
北京义翘神州科技股份有限公司
- 服务名称:
病毒灭活/清除验证服务
- 规格:
询价
病毒清除工艺简介
常用的特定病毒清除工艺:巴氏消毒法、干热法、有机溶剂/去污剂(S/D)处理法、膜过滤法、低pH孵育法、色谱法等。
| 血液制品 | 重组生物制品 | 生化药品 | 医疗器械 |
| S/D、干热灭活、除病毒过滤、巴氏消毒法 | 低pH孵育、S/D孵育、层析、除病毒过滤 | 强碱处理、低pH孵育、高温、层析、 分级沉淀、超滤 | 辐照(钴60)、强碱处理、氧化剂(过氧化氢)、分子交联工艺(Glutaraldehyde浸泡) |
常用病毒检测方法:病毒含量或滴度检查(包括蚀斑形成试验和细胞病变法)或定量病毒核酸检测相关技术。
- 蚀斑形成试验原理:病毒感染细胞后,由于固体介质的限制,释放的病毒只能向周边扩散,形成一个细胞病变区。一个蚀斑由一个病毒颗粒形成,因此该方法可对病毒进行数量的评估。
- TCID50原理:又称半数组织细胞感染量,是将含有病毒的样品进行系列稀释,不同稀释度接种到能够产生明显细胞病变的细胞上,使细胞一半呈阳性反应的最高稀释度为病毒滴度。可与蚀斑法进行换算。
- qPCR:病毒提取核酸,用引物及探针对提取后的病毒核酸进行qPCR探针法检测,反应完毕根据所得的Cp值对应病毒的标准曲线计算出病毒拷贝数。该方法可评估总病毒的含量,包括可感染性和非感染性病毒,甚至是病毒游离的核酸。可利用核酸酶消化游离的核酸,避免检测不准确。
检测方法优缺点对比
为保证生物制品安全性,根据《药品注册管理办法》的要求,由人或动物的组织、体液提取的制品、动物源性单克隆抗体及真核细胞表达的重组制品,应增加病毒清除工艺验证。义翘神州的病毒清除验证实验室具有以下几个优势:
• 北京市备案的生物安全二级负压实验室
• 已通过CNAS认证
• 严格按照GLP规范进行设计和管理
• 仪器设备齐全
义翘神州具有15年以上病毒清除验证经验,在清除研究开展之前有专门的实验人员对接客户,帮助您选择合适的病毒和工艺过程进行验证,达到提高效率和节约成本的目的。目前义翘神州已完成超过3000次病毒清除验证研究,包括抗体、蛋白、疫苗等产品类型,成功支持客户完成IND和BLA申报。另外,义翘神州提供的工艺验证数据可支持中外双报,满足出海需求。
病毒清除工艺验证技术平台

- 苏州病毒清除检测中心
- 北京病毒清除检测中心
- 先进的仪器设备

服务检测范围
义翘神州可提供工艺研发、新药临床试验申报 (IND)、生物制品许可申请 (BLA)、上市后产品补充验证的全套病毒安全性评价服务,涵盖CHO、昆虫、Vero等系统表达的单克隆抗体、蛋白、疫苗等产品,血液制品,生化药品,动物源性医疗器械,基因治疗产品等。

支持的验证工艺
常用的特定病毒清除工艺包括巴氏消毒法、干热法、有机溶剂/去污剂(S/D)处理法、膜过滤法、低pH孵育法、色谱法等。综合考虑可能污染病毒及产品的特性,义翘神州能帮助客户选择合适的病毒清除工艺,并建立缩小模型,方法学经过严格验证,达到ICH标准。

指示病毒选择
病毒清除研究中的一个主要问题是确定使用何种病毒。根据ICH指导原则,为了测试生产工艺去除病毒的总体能力,供清除评价和工艺鉴定研究用的病毒应与可能污染产品的病毒相似,而且要有广泛的理化特性。这些病毒可分为三类:"相关"病毒(用于生产过程中评价病毒去除情况的病毒)、特异"模型"病毒(与已知病毒或可疑病毒密切相关,并具有类似理化特性的病毒,如MuLv和PRV)和非特异"模型"病毒(用来为生产工艺去除病毒能力定性的病毒,如Reo-3和MVM)。目前义翘神州指示病毒种类丰富,纯度高,滴度可达8log10以上。
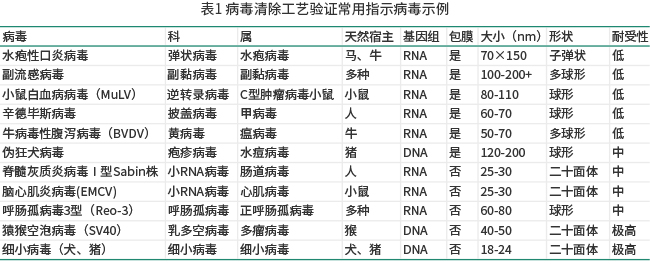
注:以上只是一些病毒的举例,并不强制使用。
病毒清除验证服务案例
义翘神州已为众多知名公司提供了病毒清除工艺验证服务,总共完成了3000次以上病毒清除验证研究,包括100多个IND项目,20余个BLA项目,100%一次性通过评审。公司设置独立的验证室和客户办公室,保证客户隐私。以客户利益为先,义翘神州积极帮助客户解决验证遇到的任何问题。同时公司提供细胞库检测业务,可打包服务降低客户成本。
我们的服务
病毒清除常见问题解答
更多CMA & CNAS认证的病毒清除工艺验证服务相关内容
CMA(中国计量认证)和CNAS(中国合格评定国家认可委员会)认证的病毒清除工艺验证,是指在生物制品的生产过程中,对具有病毒去除或灭活效果的工艺步骤进行的一系列验证活动。这些验证活动确保了生产工艺能够有效地清除或灭活潜在的病毒,从而保证最终产品的安全性。
病毒清除工艺验证通常包括:
- 确定生产工艺中各个步骤对病毒的去除或灭活能力。
- 计算去除或灭活病毒的降低系数。
- 进行动力学验证,以确保病毒清除的效率和稳定性。
用途
- 生物制品安全保证:主要用于血液制品、疫苗、生物技术药物等生物制品的生产过程中,确保产品不含有活性病毒,保障患者安全。
- 法规遵从:满足国家药典及国际药品监管机构对生物制品病毒安全性的法规要求。
- 新药临床试验申报(IND):为新药的临床试验提供必要的安全性数据支持。
- 生物制品许可申请(BLA):为生物制品的市场准入提供病毒清除效果的证明。
优势
- 提高产品质量:通过验证的工艺可以确保生物制品的病毒安全性,提高产品质量和市场竞争力。
- 满足监管要求:CMA和CNAS认证的病毒清除工艺验证有助于企业顺利通过药品监管部门的审查,加快产品上市进程。
- 增强消费者信心:CMA和CNAS的认证增加了消费者对产品安全性的信任。
- 国际互认:CNAS认证是国际互认的,有助于企业产品的国际流通和市场拓展。
- 专业服务:通过CMA和CNAS认证的实验室通常具备专业的技术能力和丰富的行业经验,能够提供高质量的验证服务。
更多生物安全检测服务
病毒清除工艺验证相关资源
- 讲师介绍
徐明明
- 视频介绍
2020年版的《中国药典》增加生物制品病毒安全性控制,同时NMPA公布的ICH指导原则Q5A为《来源于人或动物细胞系的生物技术产品的病毒安全性评价》。结合生物制品生产过程,按照《药品注册管理办法》的要求,进行病毒清除验证工艺是必需的。
本次讲座将对《中国药典》2020年版中病毒清除工艺验证的相关内容进行深入解读,并对病毒清除工艺验证中的重点、难点进行分析。
立即咨询CMA & CNAS认证的病毒清除工艺验证服务
扫码咨询CMA & CNAS认证的病毒清除工艺验证服务

(欢迎小伙伴来咨询哦! 请注明来源姓名,单位)
下载产品相关技术资料,获取更多CMA & CNAS认证的病毒清除工艺验证服务相关内容!
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验性的方式,来诱导IL10的产生(这是由于MCMV感染后,NK细胞被激活且生存和增殖能力加强)。这个发现引入注目,其研究的结果有更广泛的意义:因为这个研究结果对慢性病毒感染过程中的免疫调节,及相关的免疫病理和病毒清除有启示意义。文献已经报道,在其它慢性病毒如HCMV、HCV和HIV感染的过程中,表达激活受体的NK细胞所占比例的改变,可以上调IL-10水平。因此本研究的意义在于进一步证实了,NK细胞的早期激活有助于限制CD8T细胞引起的免疫病理及病毒的持续感染。 【PI主页】 http
控制的描述 5、起始物料、原料 6、质控策略 7、工艺验证/评价 8、 生产工艺开发和相关信息CTD格式的提交 9、产品生命周期 10、示例 1. 介绍 讨论稿:CTD 的第2部分如何做? 涉及CTD的 3.2.s的多个部分 和Q8,Q9和Q10密切相关 两种不同研发方式:传统的和进步的。 传统方式:利用重复性及检测的符合性 进步方式:风险管理及科学研究 针对单元操作 确立设计空间及质控策略 提高管理自由度 传统方式和进步的方式不相互
神奇!肥胖竟还有健康益处,Cell 子刊揭示肥胖可增强抗病毒免疫
。即肥胖相关的阴道菌群组成变化可影响粘膜对病毒感染的免疫反应,对于肥胖小鼠的早期病毒清除至关重要。 图 1:来源 Cell Reports 肥胖小鼠具有独特的抗病毒能力 大量研究表明,肥胖会损害机体的免疫系统。它通过损害淋巴管、T 细胞发育和淋巴细胞生成,诱导机体抗肿瘤免疫功能障碍,并且还促进肿瘤进展。例如,它会诱导胸腺衰老,导致 T 细胞数量减少。肥胖还会抑制骨髓中的淋巴细胞生成。临床观察表明,肥胖与病毒感染的不良预后有关。然而,目前尚无直接证据能够解释清楚肥胖对病毒感染机体的影响