相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 提供商:
云舟生物科技(广州)股份有限公司
- 服务名称:
提供定制载体及辅助载体
概述
CRISPR / Cas9载体是几种新兴的基因组编辑工具之一,可以在基因组的靶位点快速有效地创建突变(另外两种流行的是ZFN和TALEN)。
Cas9是一类RNA引导的DNA核酸酶的成员,它们是天然原核免疫系统的一部分,可赋予对外来遗传元素(如质粒和噬菌体)的抗性。在细胞内,Cas9酶与引导RNA(gRNA)形成复合物,通过与基因组中同源的18-22nt靶序列直接相互作用提供靶向特异性。gRNA与靶位点的杂交定位Cas9,然后切割基因组中的靶位点。
为了实现CRISPR介导的基因靶向,靶细胞必须同时共表达Cas9和靶位点特异性gRNA。这可以通过表达来自同一载体(又名多合一载体)的Cas9和gRNA序列或使用单独的载体来驱动Cas9和gRNA表达(分别是仅Cas9和仅gRNA载体)来实现。与一体化载体相比,使用单独的载体表达Cas9和gRNA的优势在于,根据用户的实验目标,它可以灵活地组合使用不同的gRNA表达载体与各种Cas9变体(野生型核酸酶、切口酶、核酸酶死)。
我们在Cas9核酸酶系列中提供了源自化脓性链球菌的最广泛使用的SpCas9的多种变体,以方便您在我们的在线门户网站上进行载体设计。这些变体包括 - hCas9,野生型SpCas9的人源化版本,可在目标位点有效产生双链断裂(DSB);hCas9-D10A,hCas9的“切口酶”突变形式,仅在DNA中产生单链切割;dCas9,SpCas9的催化无活性变体,携带D10A和H840A突变;SpCas9-HF1,SpCas9的高保真变体;和eSpCas9,SpCas9的增强特异性变体。dCas9与dCas9 / VP64和dCas9 / VPR等激活域或抑制结构域(如dCas9 / KRAB)的融合也分别可用于CRISPRa和CRISPRi应用。此外,我们提供源自金黄-色葡萄球菌的 SaCas9,用于需要更短 Cas9 变体的应用,而源自酸氨基球菌的 Spcas9 和 AsCpf1 可通过交错的 DNA 双支架断裂实现 DNA 切割。
AAV Cas9表达载体首先在大肠杆菌中构建为质粒。然后将其与辅助质粒一起转染到包装细胞中,其中两个倒置末端重复序列(ITR)之间的载体区域被包装成活病毒。放置在两个ITR之间的Cas9表达盒与病毒基因组的其余部分一起被引入靶细胞中。用户选择的启动子驱动Cas9表达,然后在存在靶位点特异性gRNA序列的情况下将其定向到感兴趣的DNA靶位点。
野生型AAV基因组是一种线性单链DNA(ssDNA),两端有两个ITR形成发夹结构。因此,它也被称为ssAAV。为了在宿主细胞中表达ssAAV载体上的基因,ssDNA基因组需要首先通过两条途径转化为双链DNA(dsDNA):1)以现有的ssDNA基因组为模板,以3' ITR为启动位点,通过宿主细胞的DNA聚合酶机制合成第二链DNA;2)正负链ssAAV基因组之间分子间dsDNA的形成。前者是主导途径。
AAV基因组DNA在宿主细胞核中形成游离体连接体。在非分裂细胞中,这些连接体可以在宿主细胞的一生中保留。在分裂细胞中,AAV DNA通过细胞分裂的稀释效应而丢失,因为游离体DNA不会与宿主细胞DNA一起复制。AAV DNA可以随机整合到宿主基因组中,但极为罕见。这在许多基因治疗环境中是可取的,在这些环境中,载体整合的潜在致癌作用可能引起重大关注。
AAV的一个主要实际优势是,在大多数情况下,AAV可以在生物安全1级(BSL1)设施中处理。这是由于AAV本质上缺乏复制,产生很少或没有炎症,并且没有引起已知的人类疾病。由于在宿主生物体中的免疫原性低,我们的AAV Cas9表达载体是基于CRISPR的体内应用的完美工具。
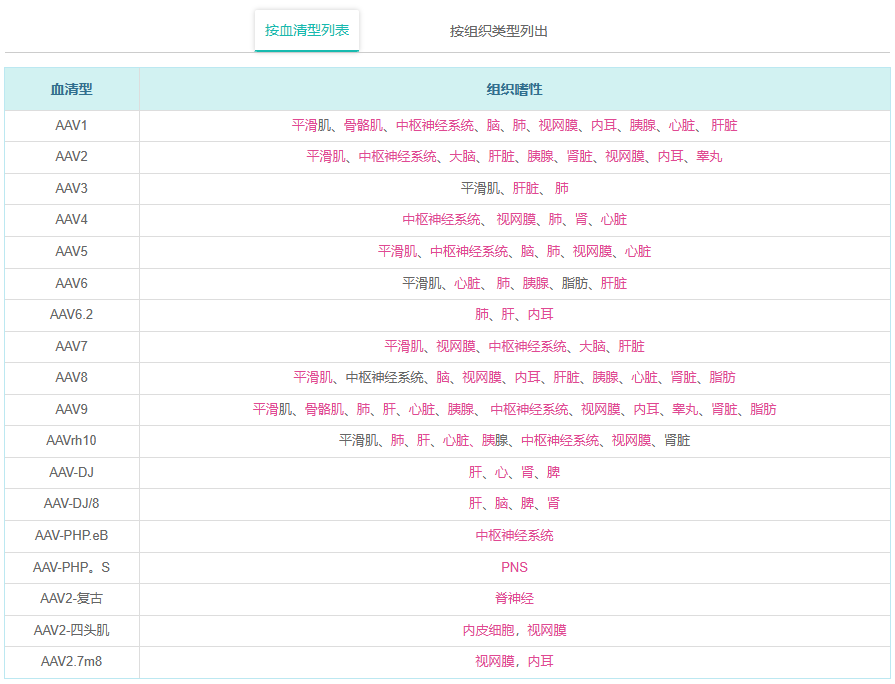
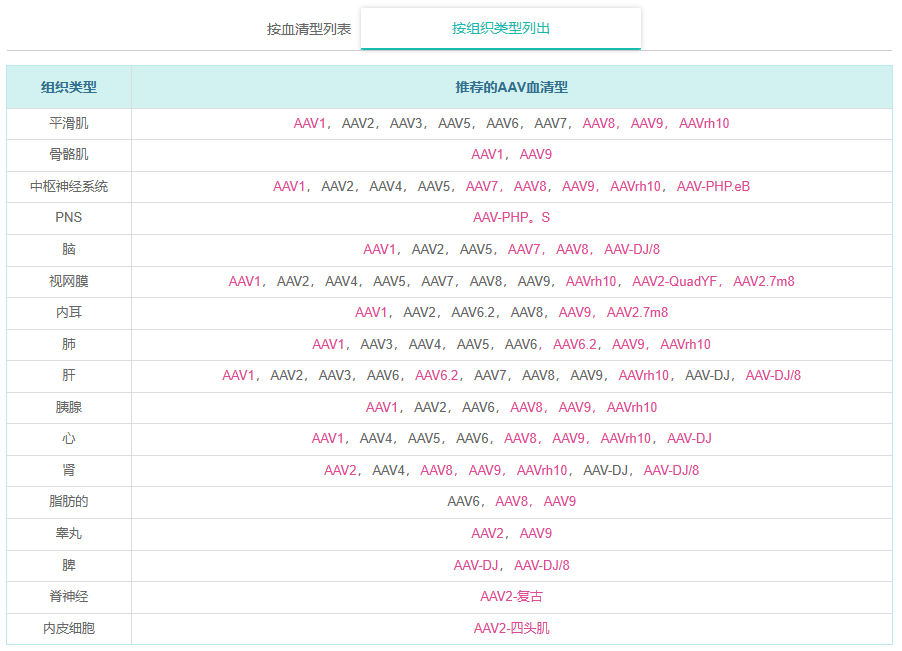
在自然界中已经鉴定出许多AAV菌株。它们根据病毒表面衣壳蛋白的不同抗原性分为不同的血清型。不同的血清型可以使病毒具有不同的组织嗜性(即感染的组织特异性)。当我们的AAV载体被包装成病毒时,通过使用不同的衣壳蛋白进行包装,可以将不同的血清型赋予病毒。我们目前为AAV载体系统提供的血清型包括 - 血清型1,2,3,4,5,6,6.2,7,8,9,rh10,DJ,DJ / 8,P-HP.eB,P-HP。S,AAV2-复古和AAV2-QuadYF。下表列出了不同的AAV血清型及其组织嗜性。
安全:AAV是最安全的病毒载体系统。AAV本质上缺乏复制,并且不知道会导致任何人类疾病。
宿主基因组破坏风险低: 转导到宿主细胞后,AAV载体在细胞核中保留为游离体DNA。缺乏与宿主基因组的整合可能是体内人类应用的理想特征,因为它降低了可能导致癌症的宿主基因组破坏的风险。
高病毒滴度:我们的AAV载体可以包装成高滴度病毒。当通过我们的病毒包装服务获得AAV病毒时,滴度可以达到>1013每毫升基因组拷贝数(GC/毫升)。
广义向性: 当将我们的AAV载体包装成适当的血清型时,可以使用我们的AAV载体轻松转导来自常用哺乳动物物种(如人,小鼠和大鼠)的各种细胞和组织类型。但某些细胞类型可能难以转导,具体取决于所使用的血清型(参见下面的缺点)。
体外和体内有效性: 我们的载体通常用于转导活体动物的细胞,但它也可以在体外有效使用。
技术复杂性: 使用病毒载体需要在包装细胞中产生活病毒,然后测量病毒滴度。与传统质粒转染相比,这些程序在技术上要求很高且耗时。这些需求可以通过在订购载体时选择我们的病毒包装服务来缓解。
PAM 要求:基于CRISPR/Cas9的靶向依赖于对位于gRNA识别序列3'末端的原间隔相邻基序(PAM)的严格要求。所需的PAM序列因所使用的Cas9变体而异。
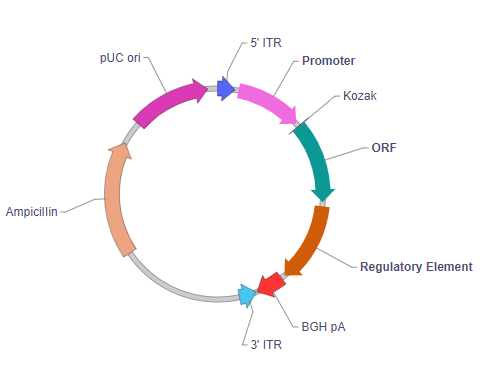
5' ITR: 5' inverted terminal repeat. In wild type virus, 5' ITR and 3' ITR are essentially identical in sequence. They reside on two ends of the viral genome pointing in opposite directions, where they serve as the origin of viral genome replication.
Promoter: The promoter that drives the expression of the downstream Cas9 gene is placed here.
Kozak: Kozak consensus sequence. It is placed in front of the start codon of the ORF of interest because it is believed to facilitate translation initiation in eukaryotes.
ORF: The open reading frame of the Cas9 nuclease variant chosen by the user.
Regulatory element: Allows the user to add the Woodchuck hepatitis virus posttranscriptional regulatory element (WPRE). WPRE enhances virus stability in packaging cells, leading to higher titer of packaged virus and enhances expression of transgenes.
BGH pA: Bovine growth hormone polyadenylation signal. It facilitates transcriptional termination of the upstream ORF.
3' ITR: 3' inverted terminal repeat. See description for 5’ ITR.
Ampicillin: Ampicillin resistance gene. It allows the plasmid to be maintained by ampicillin selection in E. coli.
pUC ori: pUC origin of replication. Plasmids carrying this origin exist in high copy numbers in E. coli.
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验有关该矢量系统的更多信息,请参阅以下论文。
| 引用 | 主题 |
|---|---|
| 科学。339:819 (2013) | 使用CRISPR/Cas9系统进行基因组编辑的描述 |
| 国家生物技术.31:827 (2013) | RNA引导的Cas9核酸酶的特异性 |
| 国家公社。9:1911 (2018) | 对各种Cas9变体的综述 |
| 科学。351:400 (2016) | AAV介导的CRISPR / Cas9编辑 |
一、试剂准备 1、Cas9 过表达慢病毒载体选择。 货号 名称 CR2001 pLV-Cas9-Puro CR2002 pLV-Cas9-Neo CR2003 pLV-Cas9Nick-Puro CR2004
遗传性眼病是一类由于基因缺陷而导致的疾病,目前已报道大约有 200 种遗传性眼病和超过 400 种具有眼部表现的系统性疾 病。遗传性眼病引起的视觉功能丧失通常很难通过传统的手术、激光治疗和局部药物治疗来治愈。基因治疗已成为治疗这类疾 病最重要的手段。腺相关病毒(AAV)由于具有安全性好、免疫原性低、表达时间长、有多种组织和细胞特异性血清型可选 择、高稳定性等优势,已被广泛应用于眼科疾病基因治疗。首款获批上市的遗传性视网膜疾病基因治疗药物 Luxturna(约 85 万 美元/剂)采用了 AAV
诺奖得主 Science 发文:基因编辑诞生 10 年,未来将如何改变世界?
3D)。 目前,存在多种用于哺乳动物系统中 CRISPR 基因编辑的递送方式,广泛划分为进入物理递送、基于病毒的递送,以及基于合成材料的递送。常见的物理递送方法包括显微注射和电穿孔,允许控制剂量,效率递送高,但仅限于离体递送。基于病毒的递送方式包括腺病毒、腺相关病毒和慢病毒,它们以质粒 DNA 的形式通过载体传播,具有良好的效率。基于合成材料的递送方法更安全且有高水平的控制和灵活性,但其效率要低于病毒, 递送效率受到材料的体积和阳离子性质的限制,易导致间质分散不良。 因此,改进当前的递送
 技术资料
技术资料暂无技术资料 索取技术资料