万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 提供商:
BrainVTA
- 服务名称:
CRISPR-Cas9基因敲除服务
一、原理介绍
CRISPR/Cas9(Clustered Regularly Interspaced Short Palindromic Repeats/Cas9)系统是目前被广泛运用的基因编辑系统,其原理是由CRISPR转录产生的sgRNA(small guide RNA)识别并结合目标基因的靶向序列,引导Cas9对结合位点进行剪切,产生DNA双链断裂(double-strand break,DSB),机体自身通过非同源末端重组(non-homologous end joining,NHEJ)的方式修复DSB,参与修复的蛋白经常会在DNA末端插入或删除几个碱基,修复后的基因由于产生突变而导致功能丧失,从而实现机体内的基因敲除(Gene Knockout)。
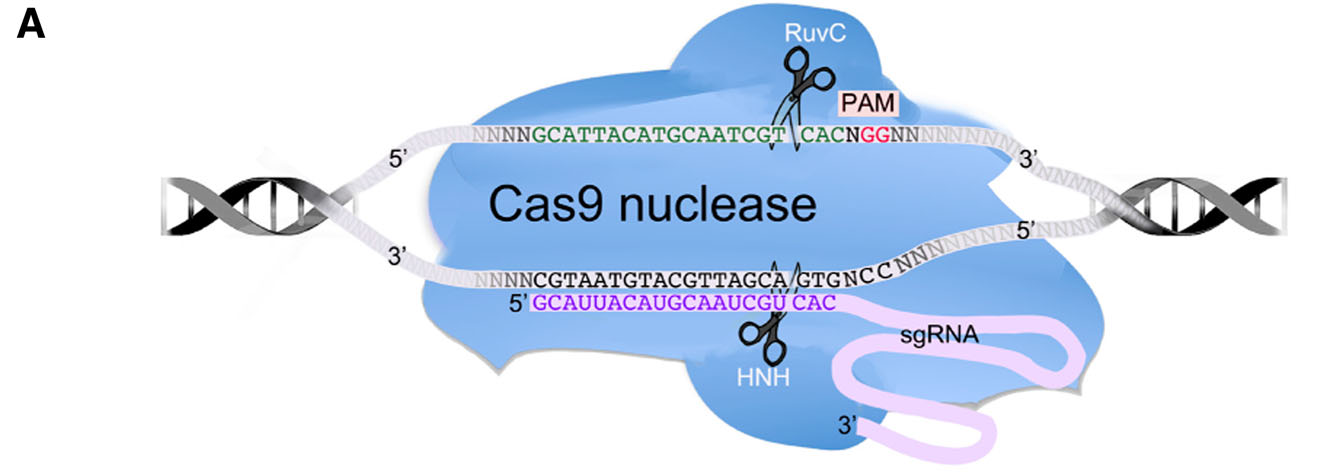
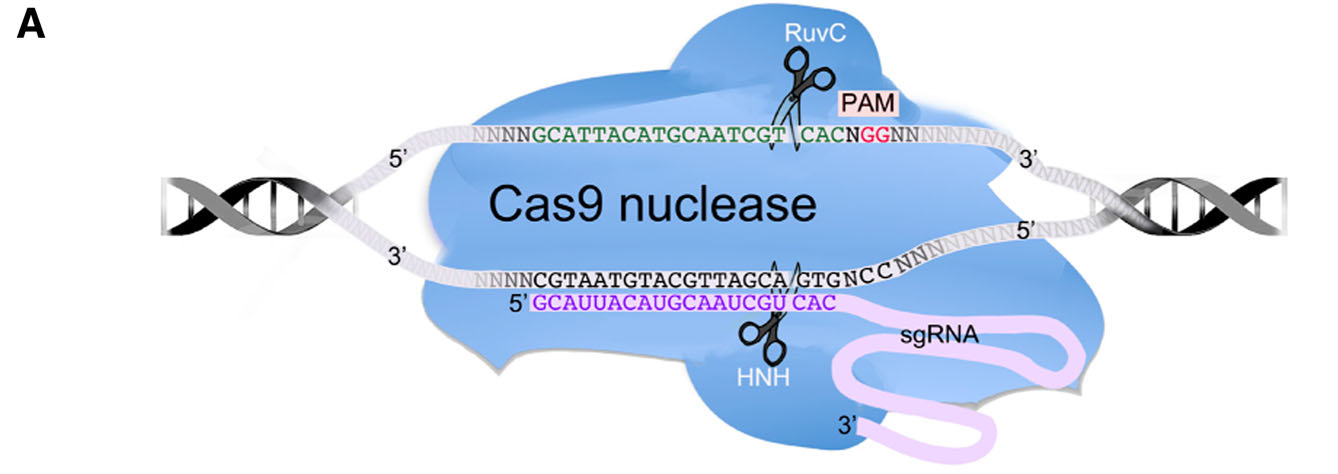
图1.CRISPR/Cas9系统介导的基因编辑(Wiles MV,et al.Mamm Genome,2015)
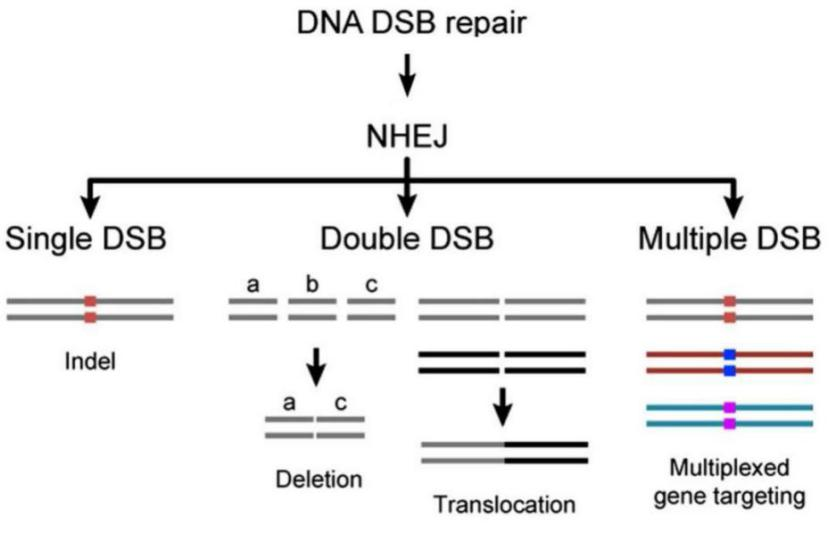
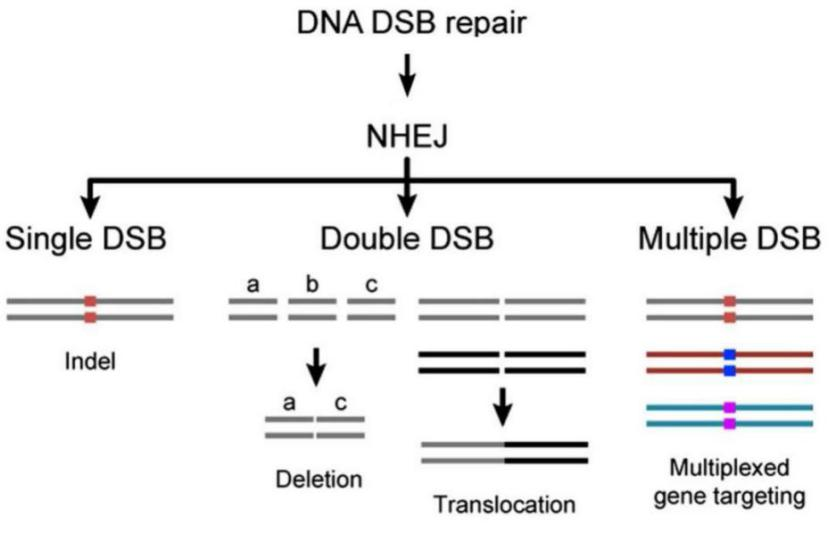
图2.非同源重组修复DSB(Wiles MV,et al.Mamm Genome,2015)
二、应用实例
1.利用CRISPR/Cas9去除HBV感染(Zhen S, et al.Gene Ther.2015)
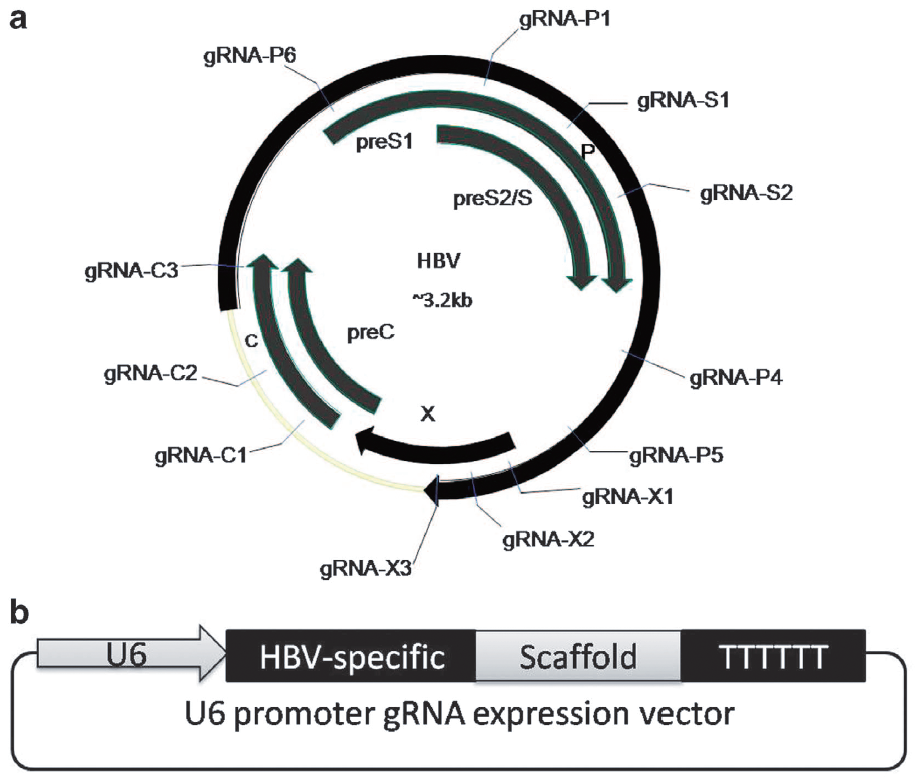
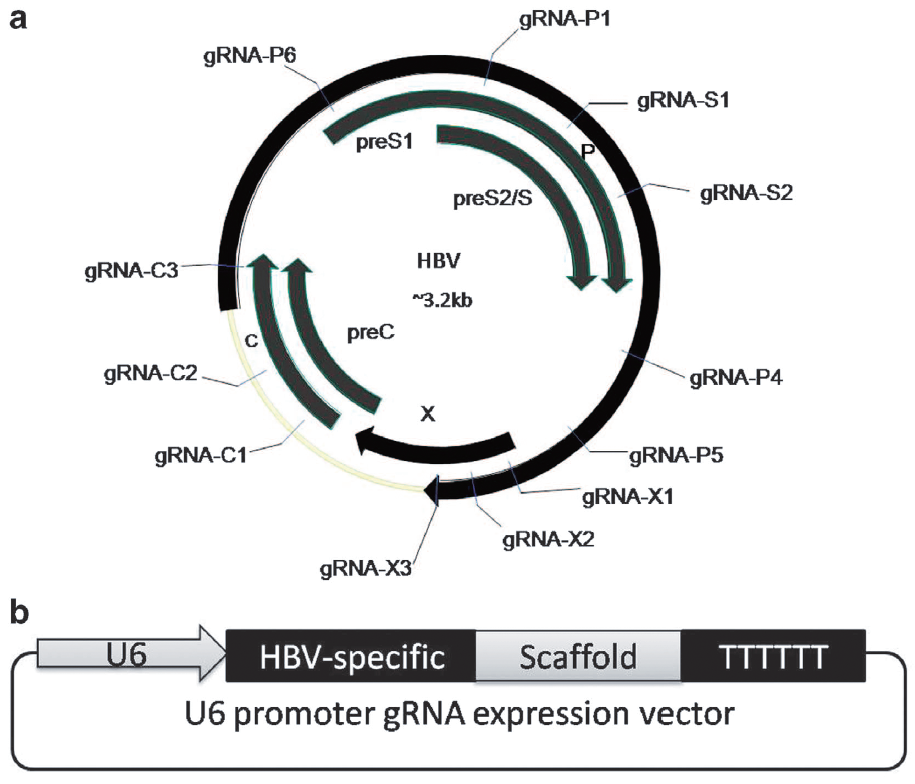
图3.靶向HBV基因组不同位置的gRNA
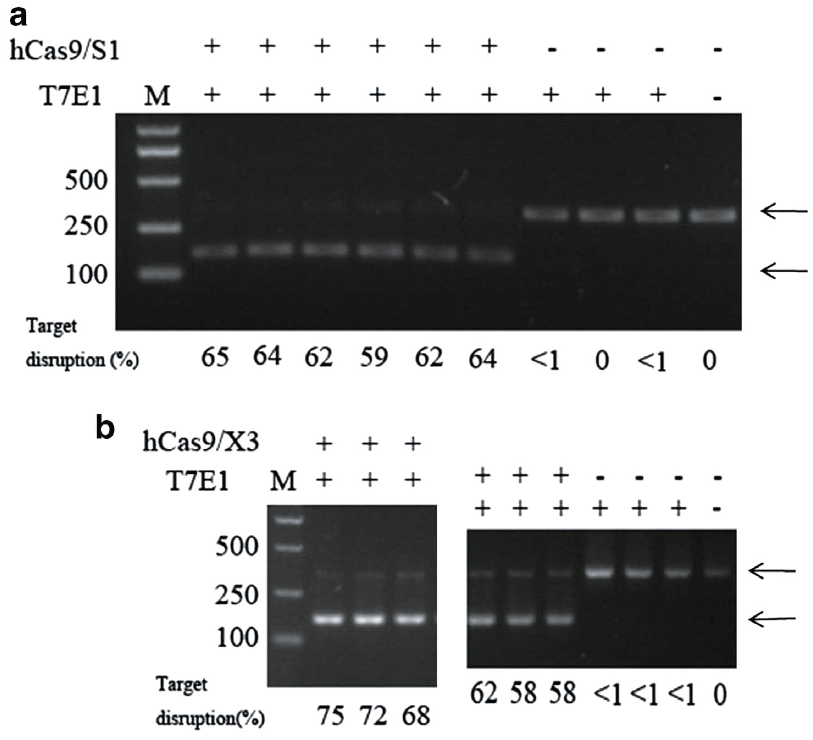
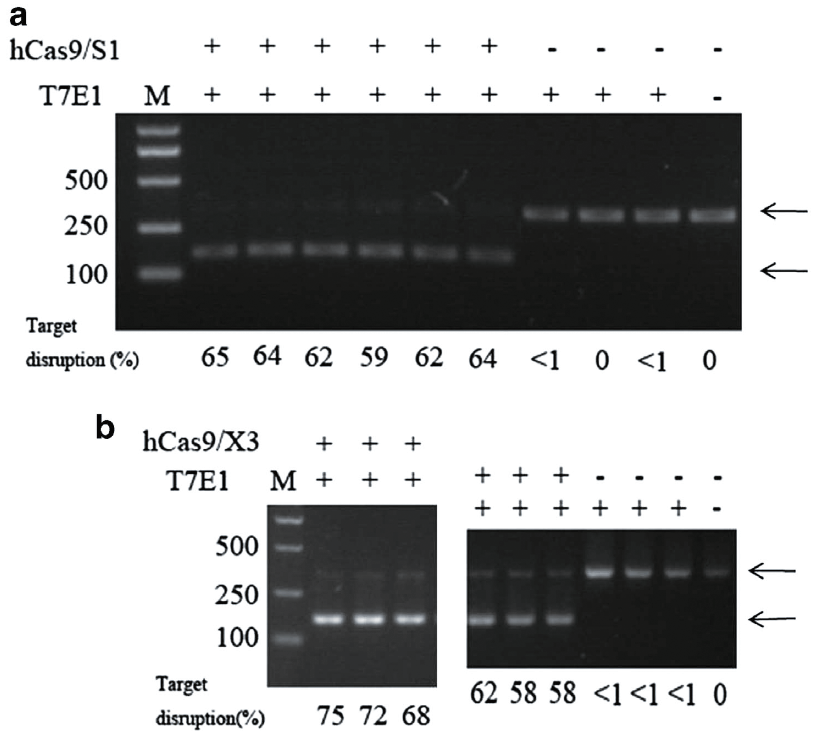
图4.靶向S基因的gRNA-S1和靶向X基因的gRNA-X3介导Cas9对HBV基因组的编辑产生突变,被T7E1错配酶识别
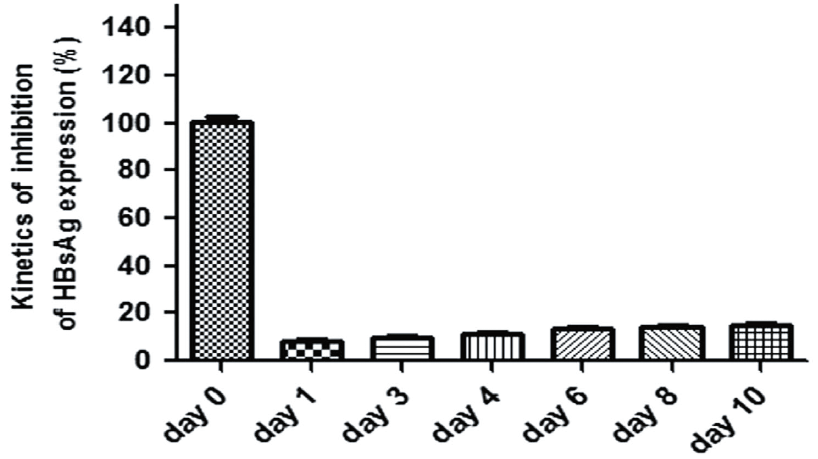
图5.Cas9和gRNA-(S1+X)共转至HBV转基因小鼠模型,能持续抑制血清中乙肝标志性抗原(HBsAg)的含量
2.利用CRISPR/Cas9进行基因治疗(Maeder ML, et al.Nat Med.2019)
莱伯氏先天性黑曚10型是一种单基因遗传病,是由于CEP290基因第26号和第27号外显子之间的突变造成mRNA错误剪接从而导致蛋白质缺失引起的,基因治疗公司Editas利用AAV载体表达SaCas9和靶向突变位点两端的gRNA,在体对CEP290基因进行编辑,删除突变的内含子序列或造成该区域翻转从而破坏错误的剪接位点,帮助形成正确的mRNA。
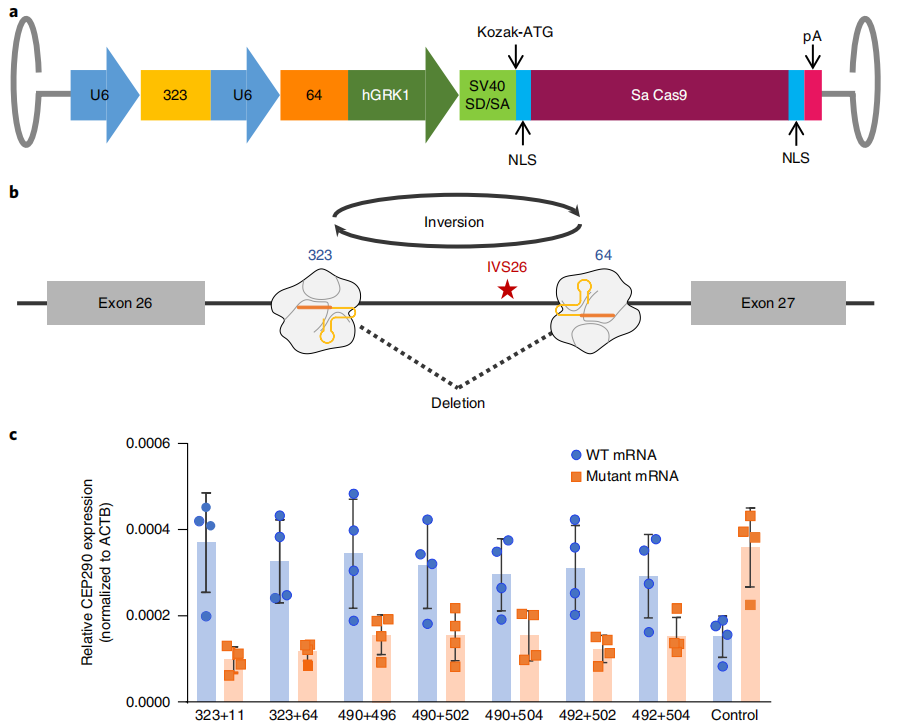
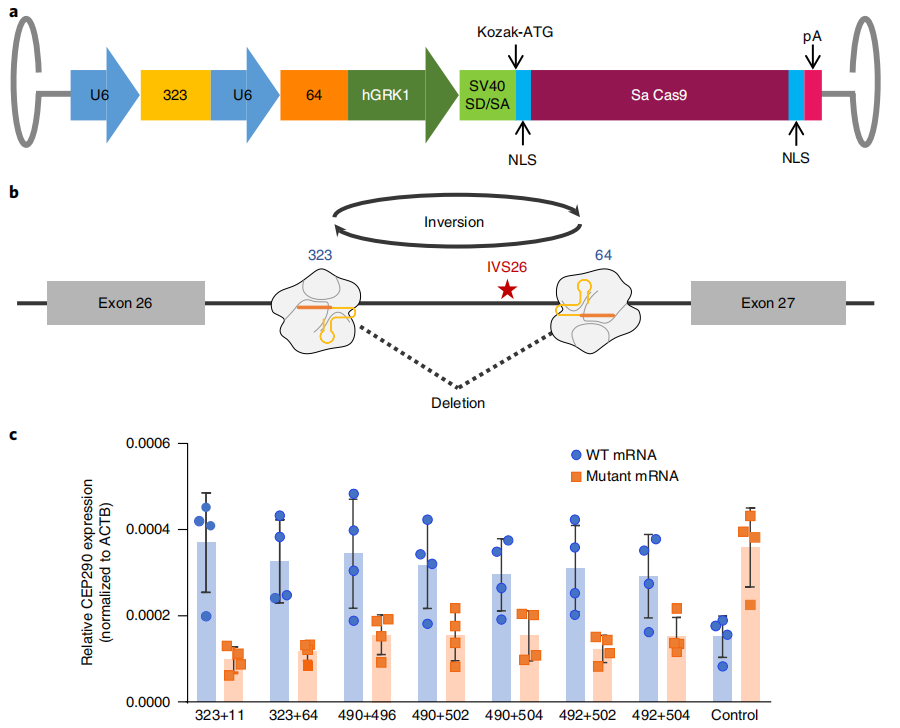
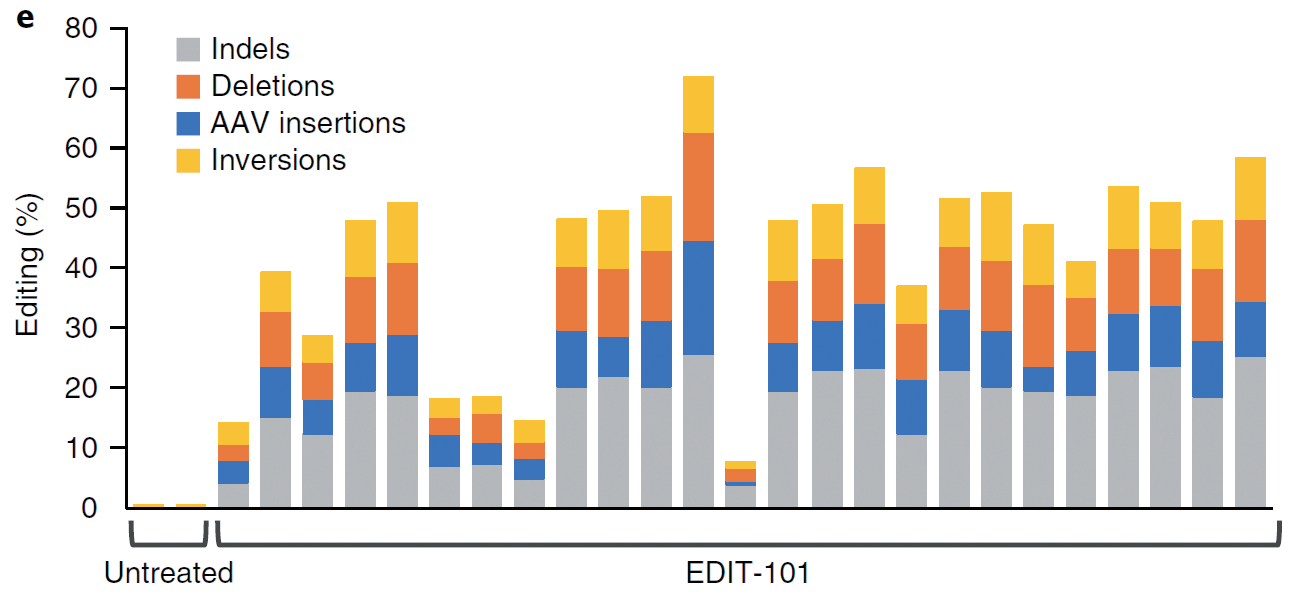
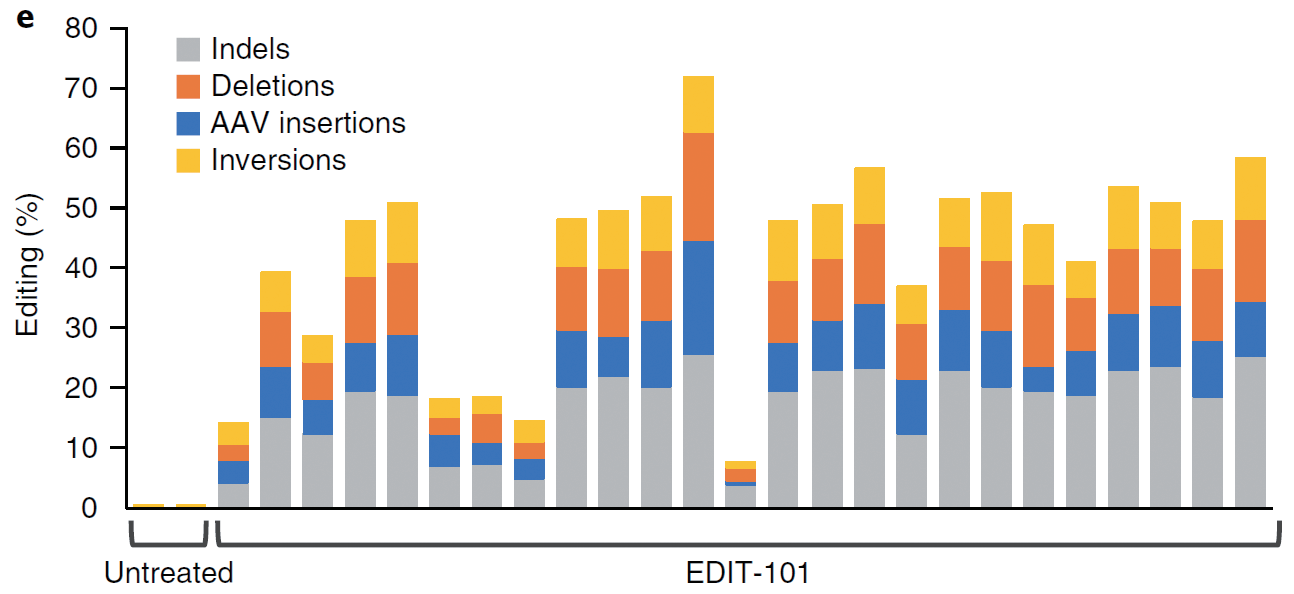
3.利用CRISPR/Cas9技术构建肿瘤模型(Maresch R, et al.Nat Commun.2016)
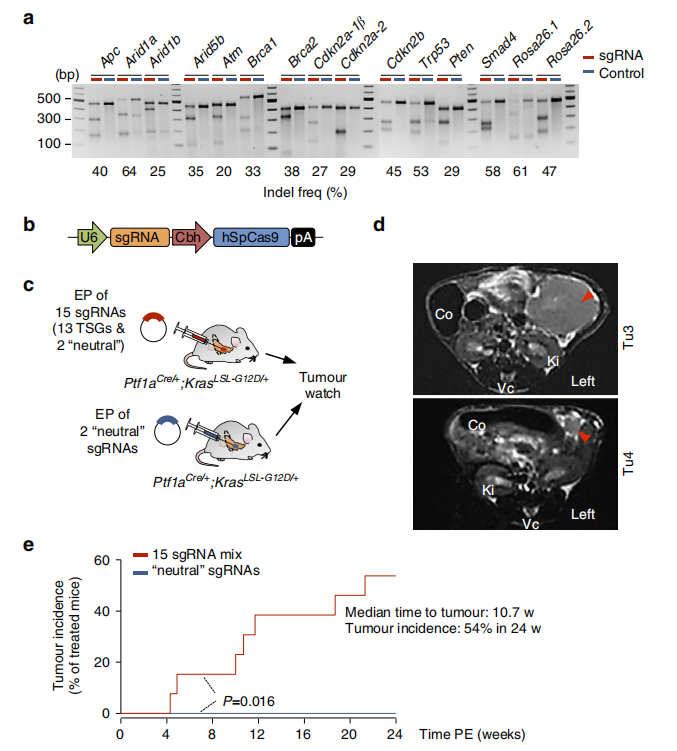
超过90%的人胰腺癌有KRAS突变,利用Ptf1a-Cre在胰腺特异诱导KRAS G12D突变基因表达,能诱导小鼠产生胰腺癌,但所需时间长达数月甚至一年以上。利用CRISPR-Cas9基因编辑在上述小鼠模型体内同时突变15个与胰腺导管腺癌(PDAC)相关的基因,可快速诱导PDAC产生,诱导成瘤中位时间为10周左右,到第24周,约54%的基因编辑小鼠能产生肿瘤。

三、我司提供病毒载体及细胞系构建服务
服务内容
1、sgRNA的设计;
2、细胞内sgRNA剪切活性筛选;
3、敲除载体的构建;
4、依据所要编辑的细胞选择Cas9和sgRNA不同导入方式:
a、脂质体易转染细胞:使用质粒系统(Cas9和sgRNA);
b、脂质体难转染细胞:使用质粒系统电转化、慢病毒或腺相关病毒感染(Cas9和sgRNA);
5、筛选基因敲除单克隆细胞系。
服务流程
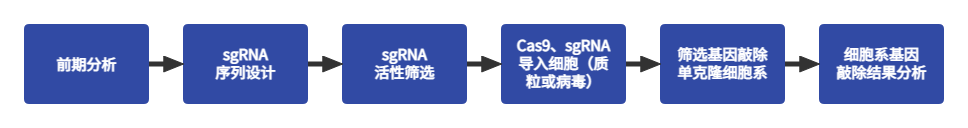
需客户提供:
1、目的基因序列(ID)以及物种来源;
2、需介导基因敲除的细胞(可选);
3、病毒类型选择以及要求;
4、血清型选择。
表1.服务信息及最终交付内容、产品
| 流程分布 |
周期 | 交付内容 | 交付产品 |
| sgRNA序列的设计 | 2-4周 | sgRNA设计分析报告 | - |
| sgRNA的活性筛选 | 获得有活性的sgRNA及筛选报告 | ||
| 基因敲除质粒的构建 | 1周 | 基因敲除质粒报告 | 基因敲除质粒 |
| 病毒包装 | 3周 | 病毒包装报告 | 高纯度病毒 |
| 单克隆细胞分选 | 8周 | 单克隆细胞分选及检测结果报告 | 基因敲除单克隆细胞系 |
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验以最火热的 p53 为例Step1 先找 p53 基因序列1. NCBI--输入 p53 并选择物种 human:tumor protein p53 [Homo sapiens (human)]https://www.ncbi.nlm.nih.gov/gene2. Ctrl+F,输入 sequence,快速定位(当然其实拉下去就是了),点击 Genebank3. 下载 p53 基因序列4. 用 SnapGene 软件打开序列,并简单了解每个元件最好是可以学一下 SnapGene 这个软件的使用
设计了 sgRNA 之后怎么办呢?还是这篇文章先讲一下这里的框架首先是实验设计Experimental design1. Target selection for sgRNA--选择靶点详情见:CRISPR-Cas9 基因敲除 sgRNA 设计 https://www.jianshu.com/p/ 8222f449cb442. Approaches for sgRNA construction and delivery.sgRNA 的合成和投递有两种方式:A)PCR;B)单独的 sgRNA
CRISPR/Cas9 基因敲除实验-- sgRNA 及引物设计
前期记录先确定目标基因CRISPR/Cas9 基因敲除实验 -- 确定目标基因然后对目的基因进行背景调查CRISPR/Cas9 基因敲除实验-- 目标基因背景调查设计 sgRNA 及引物CRISPR-Cas9 基因敲除 sgRNA 设计CRISPR-Cas9 基因敲除 sgRNA 设计好之后对前期文章的补充:设计 sgRNA 之后,需要对结果进行判断:但为什么 0.7044 分数的哪一个没有选,我也不知道为什么,总感觉他们的顺序不是随意的排的。或许有人能解答一下为什么。顺手把设计工具的解说放上
 技术资料
技术资料暂无技术资料 索取技术资料