相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 提供商:
云舟生物科技(广州)股份有限公司
- 服务名称:
提供定制载体
概述
CRISPR / Cas9载体是几种新兴的基因组编辑工具之一,可以在基因组的靶位点快速有效地创建突变(另外两种流行的是ZFN和TALEN)。
Cas9是一类RNA引导的DNA核酸酶的成员,它们是天然原核免疫系统的一部分,可赋予对外来遗传元素(如质粒和噬菌体)的抗性。在细胞内,Cas9酶与引导RNA(gRNA)形成复合物,通过与基因组中同源的18-22nt靶序列直接相互作用提供靶向特异性。gRNA与靶位点的杂交定位Cas9,然后切割基因组中的靶位点。
为了实现CRISPR介导的基因靶向,靶细胞必须同时共表达Cas9和靶位点特异性gRNA。这可以通过表达来自同一载体(又名多合一载体)的Cas9和gRNA序列或使用单独的载体来驱动Cas9和gRNA表达(分别为仅Cas9和仅gRNA载体)来实现。使用一体化载体表达Cas9和gRNA的优势在于,它提供了使用单一载体将CRISPR介导的基因编辑所需的所有组分递送到细胞的机会,这在技术上是直接的。使用单独的载体表达Cas9和gRNA需要将靶细胞与两个单独的载体共转导,这在技术上可能具有挑战性,因为并非所有细胞都会同时使用gRNA和Cas9载体转导。使用单独载体的另一种方法是转导具有所需gRNA序列稳定表达高水平Cas9的细胞或生物体。但是,这种方法可能相当耗时且劳动密集。我们的一体化腺病毒CRISPR载体通过表达来自单个腺病毒载体的Cas9和所需的gRNA序列,有助于规避上述挑战。
腺病毒CRISPR载体是一种高效的病毒载体,用于将腺病毒介导的Cas9和靶位点特异性gRNA序列引入多种哺乳动物细胞类型中,其中载体保持为游离体DNA,而不整合到宿主基因组中。它是体内首要选的基因传递系统,常用于基因治疗和疫苗接种。
腺病毒CRISPR载体首先在大肠杆菌中构建为质粒。在载体构建过程中,在两个倒置末端重复序列(ITR)之间克隆gRNA和Cas9表达盒。人类U6启动子驱动用户选择的gRNA序列的表达,该序列将Cas9引导至感兴趣的DNA靶位点。然后将载体转染到包装细胞中,其中ITR之间的载体区域被包装成活病毒。当病毒被添加到靶细胞中时,DNA货物被传递到细胞中,在那里它进入细胞核并保持为游离体DNA,而不整合到宿主基因组中。在载体构建过程中放置在两个ITR之间的gRNA和Cas9表达盒与病毒基因组的其余部分一起被引入靶细胞中。
我们的腺病毒CRISPR载体可用于表达单gRNA或双gRNA。虽然单gRNA载体广泛用于传统的CRISPR基因组编辑应用,例如产生单基因敲除,但双gRNA载体对于需要同时靶向一对基因组位点的应用是必要的。此类应用的示例包括:1)配对的Cas9切口酶实验,其中hCas9的“切口酶”突变形式(hCas10-D9A)与靶向单个靶位点的两条相反链的两个gRNA结合使用,以在每条链上产生单链切割一个,从而导致DSB的靶向特异性高于单个gRNA;2)在一对gRNA靶向的两个DSB之间产生片段的缺失;3)同时靶向两个不同的基因。单个 gRNA 载体由单个人 U6 启动子组成,驱动两个 ITR 之间的靶位点特异性 gRNA 序列,而双 gRNA 载体由两个连续的 U6 启动子组成,驱动对两个感兴趣的基因组靶位点特异性 gRNA 序列的表达。
根据设计,腺病毒载体缺乏E1A,E1B和E3基因(delta E1 + delta E3)。前两个是生产活病毒所必需的(这两个基因被设计到包装细胞的基因组中)。因此,由载体产生的病毒具有复制不全的重要安全特征(这意味着它们可以转导靶细胞但不能在其中复制)。
宿主基因组破坏风险低: 转导到宿主细胞后,腺病毒载体在细胞核中保留为游离体DNA。缺乏与宿主基因组的整合可能是体内人类应用的理想特征,因为它降低了可能导致癌症的宿主基因组破坏的风险。
非常高的病毒滴度: 在我们的腺病毒载体被转染到包装细胞中以产生活病毒后,病毒可以通过重新感染包装细胞进一步扩增到非常高的滴度。这与慢病毒、MMLV 逆转录病毒或 AAV 不同,后者不能通过再感染扩增。当通过我们的病毒包装服务获得腺病毒时,滴度可以达到>1011每毫升感染单位(IFU/毫升)。
广义向性: 来自常用哺乳动物物种(如人类,小鼠和大鼠)的细胞可以用我们的载体转导,但某些细胞类型已被证明难以转导(见下面的缺点)。
体外和体内有效性: 我们的载体通常用于转导活体动物的细胞,但它也可以在体外有效使用。
安全:我们的载体的安全性是由它缺乏病毒生产所必需的基因(这些基因被工程到包装细胞的基因组中)这一事实来保证的。因此,由我们的载体制成的病毒是复制能力不全的,除非它用于转导包装细胞。
难以转导某些细胞类型:虽然我们的腺病毒载体可以转导许多不同的细胞类型,包括非分裂细胞,但它对某些细胞类型(如内皮细胞、平滑肌、分化气道上皮、外周血细胞、神经元和造血细胞)效率低下。
免疫原性强:来自腺病毒载体的活病毒可以在动物中引起强烈的免疫反应,从而限制了某些体内应用。
技术复杂性: 腺病毒载体的使用需要在包装细胞中产生活病毒,然后测量病毒滴度。这些程序对技术要求很高且耗时。
特异性较低: 据报道,CRISPR/Cas9系统存在一些脱靶活性,一般来说,TALEN系统的脱靶活性低于CRISPR/Cas9。然而,通过将突变的hCas9-D10A切口酶与两个gRNA联合靶向单个靶位点的两条相反链以在每条链上产生单链切割,从而获得比与野生型hCas9核酸酶结合使用的单个gRNA具有更高的靶向特异性的DSB。
PAM 要求: 基于CRISPR/Cas9的靶向依赖于对位于gRNA识别序列3'末端的原间隔相邻基序(PAM)的严格要求。
单gRNA腺病毒CRISPR载体
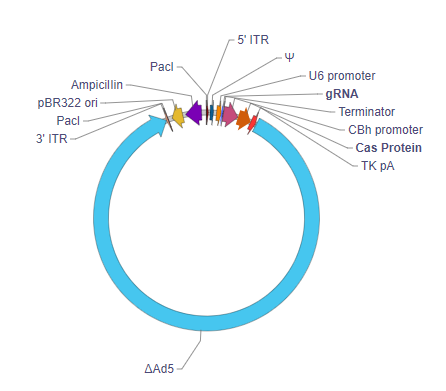
5' ITR: 5' inverted terminal repeat. In wild type virus, 5' ITR and 3' ITR are essentially identical in sequence. They reside on two ends of the viral genome pointing in opposite directions, where they serve as the origin of viral genome replication.
Ψ: Adenovirus packaging signal required for the packaging of viral DNA into virus.
U6 Promoter: This drives high level expression of the downstream gRNA. This is the promoter of the human U6 snRNA gene, an RNA polymerase III promoter which efficiently expresses short RNAs.
gRNA: Guide RNA compatible with Cas9 derived from Streptococcus pyogenes.
Terminator: Terminates transcription of the gRNA.
CBh promoter: Chicken beta-actin promoter. Drives expression of the downstream Cas9 nuclease.
Cas9 protein: The open reading frame of the Cas9 nuclease is placed here.
TK pA: Herpes simplex virus thymidine kinase polyadenylation signal. It facilitates transcriptional termination of the upstream ORF.
ΔAd5: Portion of Ad5 genome between the two ITRs minus the E1A, E1B and E3 regions.
3' ITR: 3' inverted terminal repeat.
pBR322 ori: pBR322 origin of replication. Plasmids carrying this origin exist in medium copy numbers in E. coli.
Ampicillin: Ampicillin resistance gene. It allows the plasmid to be maintained by ampicillin selection in E. coli.
PacI: PacI restriction site (PacI is a rare cutter that cuts at TTAATTAA). The two PacI restriction sites on the vector can be used to linearize the vector and remove the vector backbone from the viral sequence, which is necessary for efficient packaging.

5' ITR: 5' inverted terminal repeat. In wild type virus, 5' ITR and 3' ITR are essentially identical in sequence. They reside on two ends of the viral genome pointing in opposite directions, where they serve as the origin of viral genome replication.
Ψ: Adenovirus packaging signal required for the packaging of viral DNA into virus.
U6 Promoter: This drives high level expression of the downstream gRNA. This is the promoter of the human U6 snRNA gene, an RNA polymerase III promoter which efficiently expresses short RNAs.
gRNA #1: The first guide RNA compatible with Cas9 derived from Streptococcus pyogenes.
gRNA #2: The second guide RNA compatible with Cas9 derived from Streptococcus pyogenes.
Terminator: Terminates transcription of the gRNA.
CBh promoter: Chicken beta-actin promoter. Drives expression of the downstream Cas9 nuclease.
Cas9 protein: The open reading frame of the Cas9 nuclease is placed here.
TK pA: Herpes simplex virus thymidine kinase polyadenylation signal. It facilitates transcriptional termination of the upstream ORF.
ΔAd5: Portion of Ad5 genome between the two ITRs minus the E1A, E1B and E3 regions.
3' ITR: 3' inverted terminal repeat.
pBR322 ori: pBR322 origin of replication. Plasmids carrying this origin exist in medium copy numbers in E. coli.
Ampicillin: Ampicillin resistance gene. It allows the plasmid to be maintained by ampicillin selection in E. coli.
PacI: PacI restriction site (PacI is a rare cutter that cuts at TTAATTAA). The two PacI restriction sites on the vector can be used to linearize the vector and remove the vector backbone from the viral sequence, which is necessary for efficient packaging.
双gRNA腺病毒CRISPR载体
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验有关该矢量系统的更多信息,请参阅以下论文。
| 引用 | 主题 |
|---|---|
| 科学。339:819 (2013) | 使用CRISPR/Cas9系统进行基因组编辑的描述 |
| 细胞。154:1380–9 (2013) | 使用 Cas9 D10A 双切口提高特异性 |
| 国家生物技术.31:827 (2013) | RNA引导的Cas9核酸酶的特异性 |
| 科学代表 9:277 (2019) | 使用一体化腺病毒载体靶向 CRISPR/Cas9 |
Cell Rep:上海科技大学季泉江团队开发出高效微型 CRISPR-SpaCas12f1 基因编辑系统
CRISPR-Cas 系统是目前最常用的基因编辑工具,但是由于传统的 Cas 核酸酶分子量普遍太大,使其在在体基因治疗的应用中受限。近年来,为了解决这一难题,小的 Cas 核酸酶逐渐被发现和探究。其中,Cas12f 核酸酶是目前最紧凑的 CRISPR 效应核酸酶,比传统 Cas9 和 Cas12a 核酸酶小一半以上,在临床治疗应用中具有巨大潜力,然而高效的 Cas12f 基因编辑系统仍旧较少。 2022 年 9 月 27 日,上海科技大学季泉江教授团队在 Cell Reports 发表
诺奖得主 Science 发文:基因编辑诞生 10 年,未来将如何改变世界?
3D)。 目前,存在多种用于哺乳动物系统中 CRISPR 基因编辑的递送方式,广泛划分为进入物理递送、基于病毒的递送,以及基于合成材料的递送。常见的物理递送方法包括显微注射和电穿孔,允许控制剂量,效率递送高,但仅限于离体递送。基于病毒的递送方式包括腺病毒、腺相关病毒和慢病毒,它们以质粒 DNA 的形式通过载体传播,具有良好的效率。基于合成材料的递送方法更安全且有高水平的控制和灵活性,但其效率要低于病毒, 递送效率受到材料的体积和阳离子性质的限制,易导致间质分散不良。 因此,改进当前的递送
最近 CRISPR/Cas9 基因敲除技术可谓风靡全世界的实验室,CRISPR 被称为规律成簇间隔短回文重复,其实际上就是一种基因编辑器,是细菌用以保护自身对抗病毒的一个系统。后来,研究人员发现,它似乎是一种精确的万能基因武器,可以用来删除、添加、激活或抑制其他生物体的目标基因。由于其相对于前几代基因敲除技术而言更为简便高效。所以一经问世便受到科研界的热捧。利用 Cas9 质粒建立 knock-out 细胞系实验过程主要有以下几步:1. 确定待敲除基因的靶位点;2. 设计识别靶位点识别的一对
 技术资料
技术资料暂无技术资料 索取技术资料