万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 提供商:
BrainVTA
- 服务名称:
AAV-Barcode快速筛选病毒定制服务(qPCR法筛选)
AAV衣壳和表达框元件快速筛选
腺相关病毒(Adeno-associated virus,AAV)因其出色的组织特异性、低免疫原性、安全性和稳定性,已成为基因治疗领域极具潜力的病毒载体。由于不同衣壳AAV在组织亲嗜性上各有差异,因此选择合适的衣壳对于基因治疗效果的优化至关重要。此外,AAV表达框的优化也是决定基因治疗成败的核心环节之一。然而,传统的AAV衣壳筛选与表达框优化耗时费力、成本高昂,受实验批次间影响较大,导致结果的不确定性,从而难以实现系统性和标准化的优化流程。
因此,劲帆医药专为AAV设计了一段独特的DNA序列(Barcode),通过基因工程插至AAV基因组中,同时筛选针对各Barcode且经过扩增效率一致性验证的qPCR引物,通过qPCR检测Barcode表达水平来量化不同衣壳AAV的感染效率及表达框效能,为AAV优化提供标准化、高通量的解决方案。
优势

检测方法
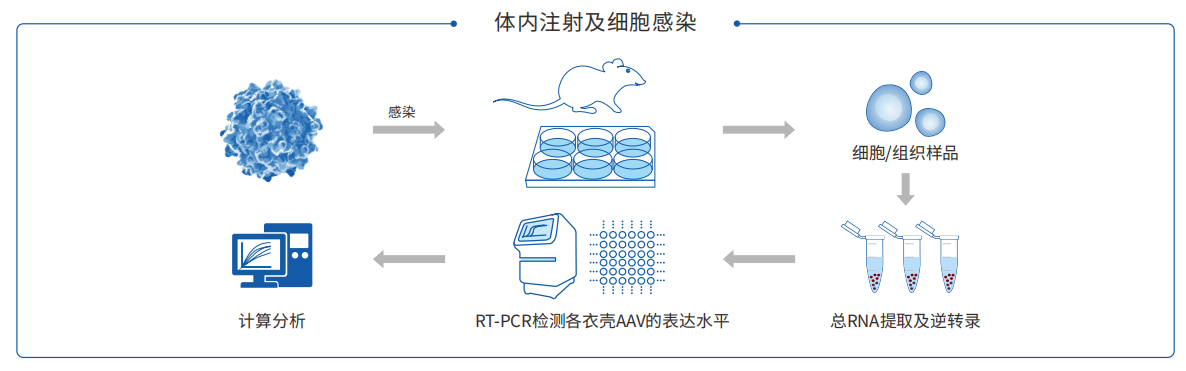
1. AAV衣壳筛选
将候选AAV衣壳1:1(每种衣壳含有不同barcode)混合感染293T细胞或小鼠,取细胞或目标组织样并提取总RNA,通过qPCR检测不同衣壳AAVbarcode的表达水平,筛选最佳AAV衣壳。
2. AAV表达框优化筛选(启动子筛选为例)
将候选启动子(每种启动子对应一种特定的Barcode)与EGFP报告基因使用适合的衣壳AAV载体进行包装,然后将其1:1混合感染293T细胞或小鼠,取细胞或目标组织样并提取总RNA,通过qPCR检测EGFP及各启动子对应Barcode的表达水平,筛选出最佳启动子。
3. RNA提取及qPCR法检测
使用RNA提取试剂盒(需自备)提取细胞或组织样品总RNA,并用逆转录试剂盒(需自备)将1μg RNA逆转录为cDNA,然后通过EGFP及各Barcode引物进行qPCR检测病毒感染后是否表达对应mRNA,模板分别用AAV mix DNA/样品cDNA,反应按下表进行。
|
成分 |
体积(μl) |
|
AAV mix DNA/样品cDNA |
1 |
|
引物 |
0.4 |
|
qPCR mix |
10 |
|
ddH2O |
8.2 |
|
总体积 |
20 |
4. 结果计算及分析
将qPCR实验所得Ct值对应填入下表,并按表中所示计算方式进行计算,最终的占比数值即为AAV mix中不同衣壳病毒相对感染效率,数值越大则表示该种衣壳AAV的感染效率越高/启动子表达效能越高。
|
病毒样品 |
AAV#1/ 启动子#1 |
AAV#2/ 启动子#2 |
AAV#3/ 启动子#3 |
AAV#4/ 启动子#4 |
… |
AAV#9/ 启动子#9 |
AAV mix (总病毒) |
|
引物 |
引物1 |
引物2 |
引物3 |
引物4 |
… |
引物9 |
EGFP引物 |
|
AAV mix DNACt值 |
A |
B |
C |
D |
… |
I |
Y |
|
样品cDNACt值 |
a |
b |
c |
d |
… |
i |
y |
|
效率系数S |
S=(2-A+2-B+2-C+…+2-I)/(2-a+2-b+2-c+…+2-i) |
| |||||
|
相对感染效率 |
2A-a×S |
2B-b×S |
2C-c×S |
2D-d×S |
… |
2I-i×S |
|
产品组分
|
组分 |
内容 |
|
AAV mix |
以EGFP为报告基因,多种含有不同barcode的AAV(可定制) 规格:滴度1E+13vg/ml、体积100µl |
|
Primers |
包括:barcode引物、EGFP引物 规格:浓度10µM/µl、体积10µl/Primer |
应用案例
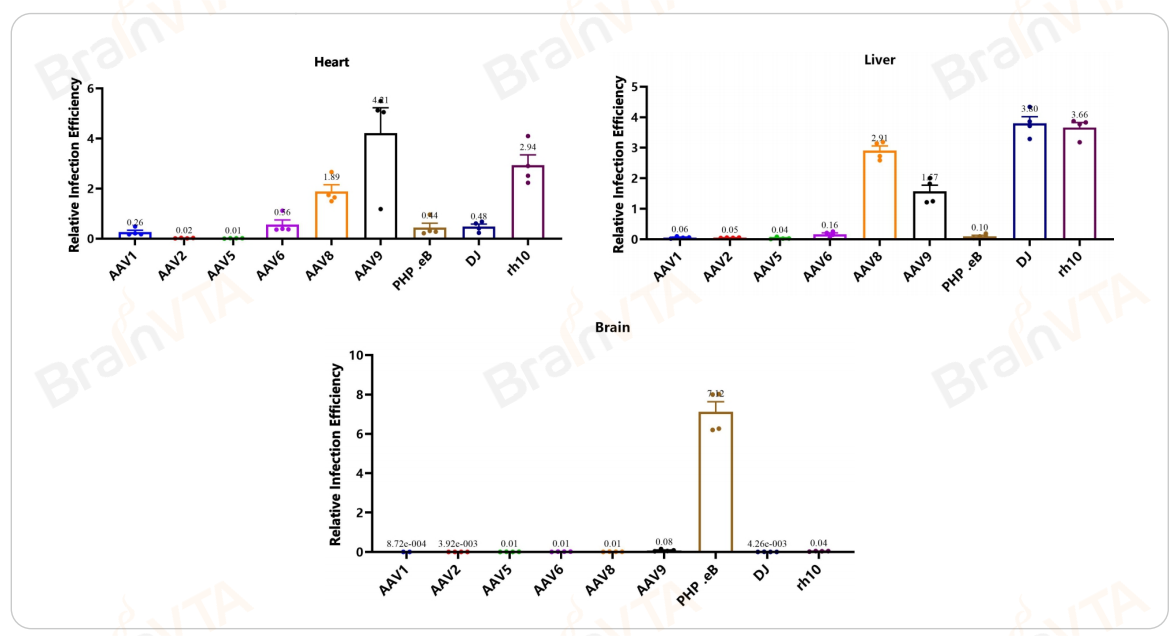
1. 体内注射筛选各组织最佳AAV衣壳:
通过尾静脉注射9种不同衣壳,每种衣壳对应一种特定的Barcode,混合感染C57小鼠,收集小鼠组织并提取总RNA,通过qPCR检测不同衣壳AAV表达水平。实验结果显示,不同组织样本中各衣壳AAV的感染效率排序具有显著组织特异性,其分布特征与预期靶向效率吻合。
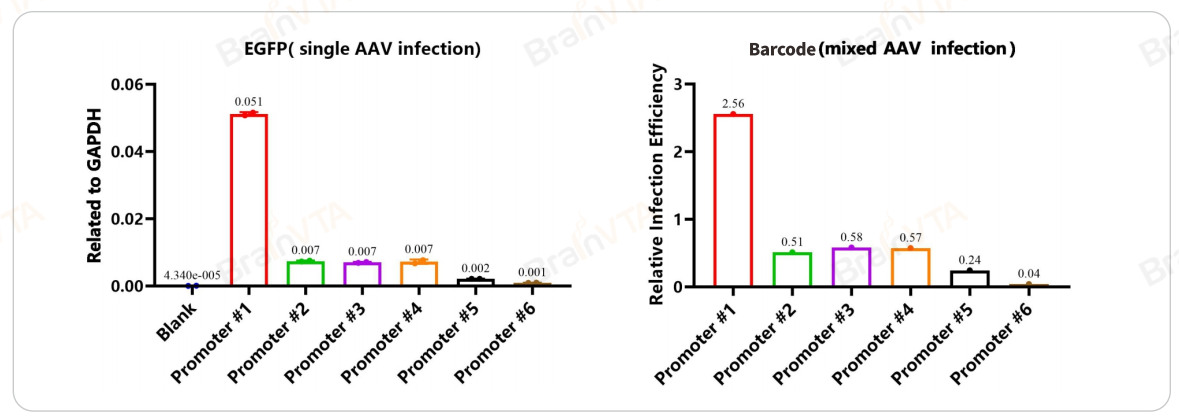
2. 感染293T细胞筛选最佳启动子:
采用AAV9系统构建含六种不同启动子(各对应一种特定的Barcode)及EGFP报告基因的重组载体。梯度稀释将病毒分别实施混合感染或单独感染293T细胞系,收集细胞并提取总RNA,通过qPCR检测EGFP报告基因及Barcode表达水平。校正后混合感染中各启动子Barcode表达水平与单独感染EGFP表达水平趋势基本一致,表明该方法能有效去除混合感染的交叉干扰风险,启动子筛选方法可靠性高。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验产品及服务,生产和质控遵循国际公认的标准流程,所获得的病毒颗粒经过超速密度梯度离心和过滤,并通过壳蛋白免疫法进行滴度测定。MCE 交付的腺病毒滴度超过 1E+10PFU/mL 且无支原体、内毒素等污染,可以满足各类实验的使用要求。 腺相关病毒包装服务 MCE AAV 病毒的生产和质控遵循国际公认的标准流程,所获得的病毒颗粒经过超速密度梯度离心和过滤除菌,并通过 qPCR 对病毒基因拷贝进行滴定。MCE 交付的 AAV 病毒滴度超过 1E+12VG/mL,且无支原体、内毒素等污染
293,CHO-S,DG44和CHO-K1细胞,来源于经筛选转染效率更高的亚细胞系。这些细胞也可用于无血清和限定化学成分培养基。重组蛋白的大规模生产一般在稳定转染的悬浮细胞中进行。这些细胞易于生长到高密度并合成更多蛋白,使用基质珠做为固相支持可以使贴壁细胞悬浮生长。 11转染效率的验证 最有效的验证方式必须是qPCR验证。 荧光观察,使用病毒转染,明白自己病毒的情况,是荧光标记(一般是GFP)还是非荧光标记。质粒转染,可以在载体上添加荧光标记,帮助自己通过荧光观察转染效率。但是荧光并不能完全证明转染
细胞在肿瘤、病毒、细菌、寄生虫、移植组织、过敏原、甚至自身抗原的适应性免疫应答中都发挥着重要的调节作用。大部分 T 淋巴细胞在其细胞表面表达单一的、高度特异性的抗原受体(TCR),与 MHC-抗原肽复合物相结合并识别其中特异的抗原肽,启动获得性/特异性免疫应答机制,比如 T 细胞介导的细胞免疫和 B 细胞介导的体液免疫。由于 TCR 与 MHC-抗原肽复合物之间的亲和力低,半衰期短,相互结合后容易快速脱落,重组的可溶性 MHC-抗原肽复合物单体并不适合用于抗原特异性的 T 细胞检测。1996
 技术资料
技术资料暂无技术资料 索取技术资料