首个 GEP-NETs 国产放射性核素的 III 期试验公布,明年有望获批上市
2025-11-12 18:00点击次数:122
关键词: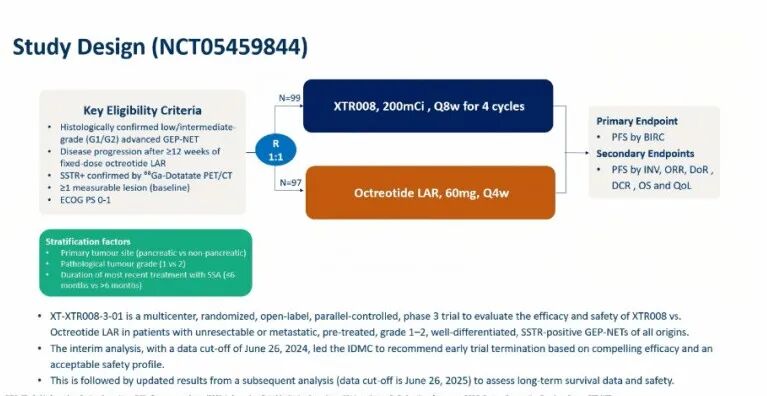
图 1. XT-XTR008-3-01(NCT0545984)临床研究设计(来源:讲者幻灯)
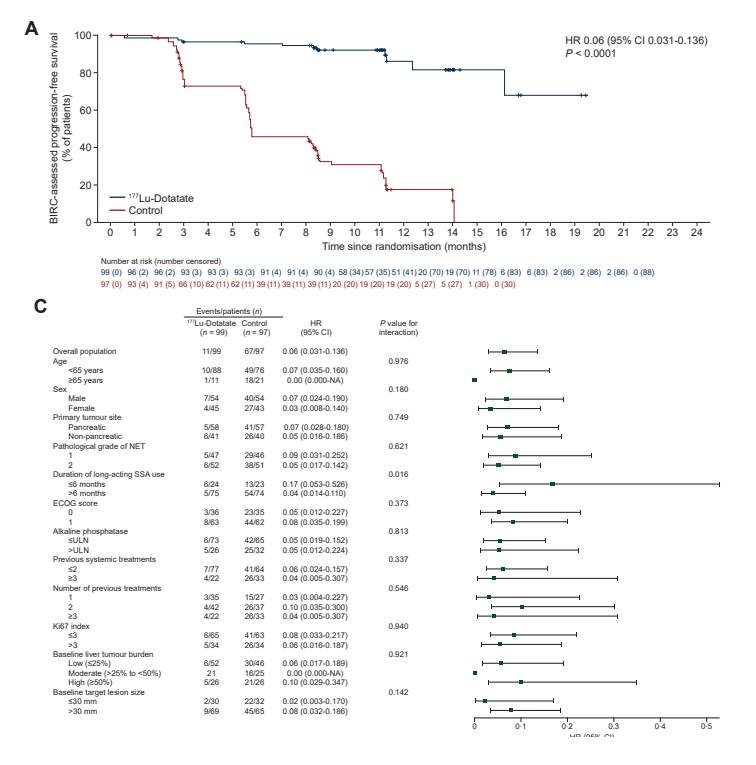
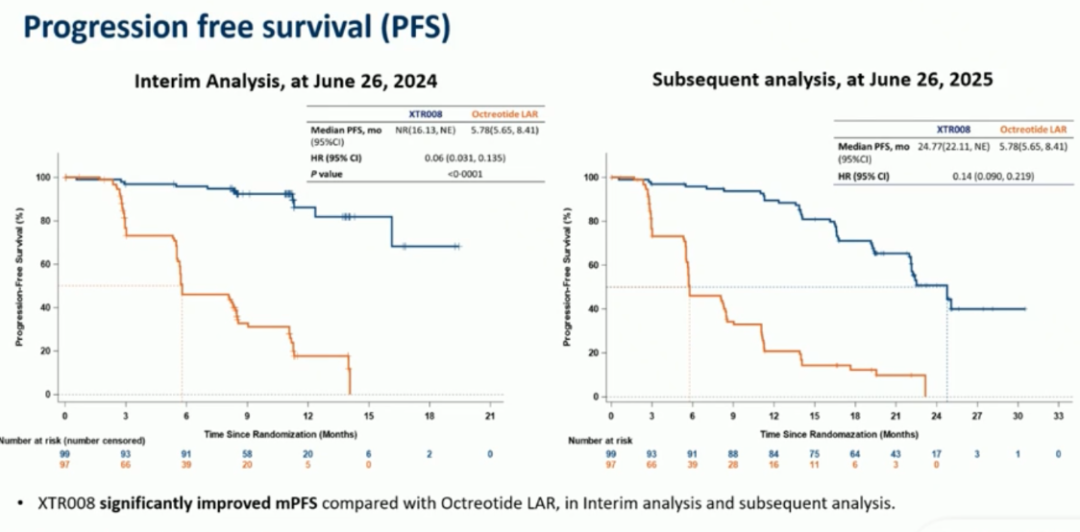
图 3. 截至 2025 年 6 月 26 日 PFS 分析结果(来源:讲者幻灯)
[1]Rongrui Liu.XT-XTR008-3-01: a phase III study of 177Lu-Dotatate versus high-dose octreotide long-acting repeatable (LAR) in patients with advanced grade 1–2, well-differentiated, gastroenteropancreatic neuroendocrine tumours (GEP-NETs).2025ESMO LBA63(Oral)
[2]Xu, J. et al. 177Lu-Dotatate versus high-dose long-acting octreotide for the treatment of patients with advanced, grade 1-2, well-differentiated gastroenteropancreatic neuroendocrine tumours (XT-XTR008-3-01): an open-label, randomised, phase III trial. Annals of Oncology. https://doi.org/10.1016/j.annonc.2025.08.3758
[3]Sedlack AJH, Varghese DG, Naimian A, et al. Update in the management of gastroenteropancreatic neuroendocrine tumors. Cancer. 2024;130:3090-3105.
[4]Das S, Dasari A. Epidemiology, incidence, and prevalence of neuro endocrine neoplasms: are there global differences? Curr Oncol Rep. 2021;23:43.
[5]Dasari A, Shen C, Halperin D, et al. Trends in the incidence, prevalence, and survival outcomes in patients with neuroendocrine tumors in the United States. JAMA Oncol. 2017;3:1335-1342.
[6]Cives M, Strosberg JR. Gastroenteropancreatic neuroendocrine tumors. CA Cancer J Clin. 2018;68:471-487.
[7]Chinese Society of Clinical Oncology. Guidelines for the Diagnosis and Treatment of Neuroendocrine Tumors 2022.
[8]Caplin ME, Pavel M, Cwikła JB, et al. Lanreotide in metastatic enteropancreatic neuroendocrine tumors. N Engl J Med. 2014;371:224-233.
[9]Society of Neuroendocrine Neoplasm of China Anti-Cancer Association. China Anti-Cancer Association guideline for diagnosis and treatment of neuroendocrine neoplasm (2022 edition). China Oncol. 2022;32:545-579.
[10]Strosberg J, El-Haddad G, Wolin E, et al. Phase 3 trial of 177Lu-Dotatate for midgut neuroendocrine tumors. N Engl J Med. 2017;376:125-135.
[11]Strosberg JR, Caplin ME, Kunz PL, et al. 177Lu-Dotatate plus long-acting octreotide versus high-dose long-acting octreotide in patients with midgut neuroendocrine tumours (NETTER-1): final overall survival and long-term safety results from an open-label, randomised, controlled, phase 3 trial. Lancet Oncol. 2021;22:1752-1763.
[12]Singh S, Halperin D, Myrehaug S, et al. [ 177Lu]Lu-DOTA-TATE plus long-acting octreotide versus high-dose long-acting octreotide for the treatment of newly diagnosed, advanced grade 2-3, well-differentiated, gastroenteropancreatic neuroendocrine tumours (NETTER-2): an open-label, randomised, phase 3 study. Lancet. 2024;403:2807-2817.
我们长期为科研用户提供前沿资讯、实验方法、选品推荐等服务,并且组建了 70 多个不同领域的专业交流群,覆盖神经科学、肿瘤免疫、基因编辑、外泌体、类器官等领域,定期分享实验干货、文献解读等活动。
添加实验菌企微,回复【】中的序号,即可领取对应的资料包哦~
【2401】论文写作干货资料(100 页)
【2402】国内重点实验室分子生物学实验方法汇总(60 页)
【2403】2024 最新最全影响因子(20000+ 期刊目录)
【2404】免疫学信号通路手册
【2405】PCR 实验 protocol 汇总
【2406】免疫荧光实验 protocol 合集
【2407】细胞培养手册
【2408】蛋白纯化实验手册
【2501】染色体分析方法汇总
【2502】国自然中标标书模板
【2503】WB 实验详解及常见问题解答
【2504】DeepSeek 论文写作常用口令
【2505】中国科学院期刊分区表(2025 年最新版)
【2506】期刊影响因子(2025 年最新版)
【2507】130 种实验室常用试剂配制方法(附全套资料)
【2508】常见信号通路
【2509】限制性核酸内切酶大全