更多资讯
涡旋混匀基于偏心原理,用于混合试管中的液体组分、重悬细胞。涡旋混匀仪的操作使用步骤:将放置在平稳的工作台上,并确保其电源线接地良好;打开电源开关;根据需要,选择合适的转速;按下启动按钮,开始工作;在混匀过程中,可以根据需要适时监控混匀的程度,并根据需要调整混匀的转速;混匀结束后,按下停止按钮,关闭电源开关。涡旋混匀仪的维护保养方法:使用完毕后,将电源开关关闭,并拔掉电源插头;使用干净的湿布或纸巾擦拭表面,清除残留液体和杂质;定期清理工作室,清除堆积的杂质和污垢;配件如有损坏或磨损,应及时更换;注意避免受到较大的震动或碰撞,以免影响使用效果和寿命;定期检查电源线和插头,确保其安全可靠;如需长时间存放,应尽量放置在干燥、阴凉、通风的地方,避免受潮或受热。
1、离心机离心力与哪些因素有关?离心力与转子角度,转子半径,转速均相关,样品容量影响可忽略。2、离心机具体适配那些管子?15ml塑料管,10ml、5ml采血管,2ml、1.5ml离心管,1.8ml、1.5ml冻存管。3、离心机不同材质转子寿命多久?复合型工程塑料转子一般寿命3年,铝合金或钛合金材质5-7年,不锈钢材质10年,转子使用寿命与使用频次有关,以上时间仅供参考。4、离心机转子怎样消毒?高强塑料转子:有样品泄露的话可以用中性吸液清洗,擦拭,但是不可以使用紫外消毒,会使材料变脆影响寿命;铝合金转子:可反复耐受121度,高温高压灭菌。5、转子是否可以消毒?铝合金转子可以高温高压消毒,高强度塑料转子不可以进行高压灭菌和紫外光照射。6、离心管的容量最多可以装多少?建议不超过离心管最大容量的80%。
离心机原理是通过电机驱动转子旋转,产生离心力,在高速旋转中,实验样本混合物中的组分会受到离心力的影响,使密度较高的颗粒向背离轴心的方向移动,而密度较低的颗粒朝向轴心方向移动,这些密度较大的颗粒会沉积在离心管管底,形成沉淀物,从而实现样本中液体与固体颗粒或液体与液体混合物中各组分分离的效果。操作离心机是实验室工作中常见的一项任务。以下是一些值得注意的操作事项:安全性:- 首先确保使用离心机时遵循实验室安全规定,戴上适当的个人防护装备,如实验手套和护目镜;- 在操作前检查离心机是否良好运行,并确保所有附件(如转子、适配器等)已正确安装;- 为了稳定离心机在运行过程中,请将其放置在平稳坚固的表面上;样品准备:- 在进行任何离心之前,务必仔细阅读并遵循相关样品处理方法和说明书;- 确保样品密封良好且标注清楚,在载体(例如:管式离心管)内加入合适量的溶液,以免溢出或破裂造成伤害或污染设备;转子选择与安装:- 根据所需应用选择适当类型和规格的转子。不同大小、形状和容量的转子可用于不同种类和数量的样本;- 在安装转子之前,确保其干净无损,并且转子通道中没有杂质或残留物;离心机配平:根据离心机配平原则
自离心机 19 世纪诞生以来,因转子不配平造成的威胁一直存在着,轻则造成机器转轴的磨损,减少离心机使用寿命,离心管脱离进而造成样品损失,重则造成人员伤亡。而如何避免转子不配平造成的威胁,最好的办法就是学会正确的配平方法!1、固定角转子配平对于固定角转子的配平,通常只需牢记「中心对称法」即可。以下图 12 孔固定角转子配平为例,可遵循这一原则放置样品:2、水平转子配平在实际应用中,最让实验汪头疼的,是给水平转子配平。因为不单要考虑单个吊篮内的离心管是否对称,又要兼顾对面吊篮内的离心管是否平衡。这种情况,配平时要切记两个原则:放置单个吊篮内的离心管,应保证吊篮的重心在吊篮的中心点上;放置对面吊篮内的离心管,应以第一个吊篮放置位置为基准,严格遵循转子中心点对称原则,再放置合适的位置。以下图 4×14 孔水平吊篮转子配平为例,可遵循上述原则放置样品:3、对于奇数管的配平此外,还经常会遇到奇数管配平的情况,多数同学们遇到奇数管配平时,通常会放置一个空白配平管(装上水),这样简单易行,但对于多频次离心、样品质量和体积往往不同的实验时,这种方法就会显得比较麻烦。那遇到这种情况,到底要怎么配平呢?我们
1、真空控制器工作原理是啥?不借助压力传感器怎么实现压力控制的?当系统内真空压力高于或低于设定压力时,控制器内的压力感应器立即动作,使控制器内的开关触点断开或接通,此时设备停止工作;当系统内的真空压力回到设备设定的压力范围时,控制器的压力立即复位,使控制器内的开关触点接通或断开,此时设备正常工作;不借助压力传感器,无法实现压力控制。2、竖直型冷凝器和倾斜型冷凝器, 哪种比较好?对于应用要求来说两者的冷凝效果相当。这两种冷凝器的冷凝面积和冷却效率是一样的。3、旋转蒸发仪和真空控制器,真空泵怎么连接,起什么作用?真空控制器接在旋蒸和真空泵中间,串联。使用旋蒸时,真空度不合适,试剂会出现突沸和暴沸,通过使用真空控制器,与旋蒸串联,可以精确控制旋蒸内部真空度,尤其针对易挥发试剂浓缩,能够得到最大最理想的回收率。也广泛应用于有机试剂的减压蒸馏,对真空度的逐步控制,溶剂的逐步提取使用。4、冷却循环机的冷媒是什么?冷媒是 R404A。化学成份: 五氟乙烷/三氟乙烷/四氟乙烷 混合物旋转蒸发仪中途加抽真空会有什么影响?抽真空会影响样品的沸点,样品原处于沸腾临界点,突然抽真空降低样品沸点,导致样品爆沸冲
旋蒸的基本原理就是减压蒸馏,在减压的条件下,连续蒸馏大量易挥发性溶剂,以达到分离和纯化的目的。旋蒸是研发及分析实验中用于浓缩干燥回收产物的一款必备的基本仪器。即:在减压条件下,将旋转蒸发瓶置于水浴锅中,边旋转边加热,增大蒸发面积(溶剂在烧瓶内壁形成一层液体薄膜)利于瓶内溶液蒸发,样品旋转产生的作用力可以有效的抑制样品的沸腾。影响旋转蒸发仪蒸发效率的四要素:真空度、转速、水浴温度、冷凝器1、真空度影响系统真空最关键且会变化的因素是:真空泵、密封圈和真空管。密封圈:作为承接蒸发管和冷凝管的关键密封件,其耐磨性和耐腐蚀性是关键。常用作密封圈的材质是:PTFE 和橡胶,然而全氟橡胶和 PTFE 的耐磨性和耐腐蚀性都会更好。加了金属的缓冲弹片,耐磨性更好。真空泵和真空控制器:真空泵极限越低,系统的真空值也越低。在蒸馏的时候,需要通过真空控制器设置合理的真空值,保证蒸馏效率,同时避免爆沸。目前隔膜真空泵的极限真空最低可达 2mbar,循环水泵的极限真空大约 50mbar(0.095kpa)。如果预算允许,真空控制器或真空阀就很有必要,它能控制好蒸馏所需的系统真空值。真空管材质:首选硅胶管,因其老化
磁力搅拌芯选型指南多用途磁力搅拌芯套装
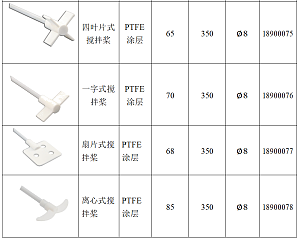
在搅拌黏性液体时,会出现搅拌子突然与容器底部中心脱离,并开始不规则的跳动,这种现象也称“跳子”现象。如果出现跳子的现象,可能是如下几个原因造成:1、磁子类型不适配搅拌过程中应根据样本体积和粘度,选择适配的磁子类型。市面上常见的搅拌子类型有如下几种:2、磁子尺寸不匹配对应容器的大小选择合适尺寸的磁子,一般来说,30mm 的搅拌子适用于大多数普通的烧杯。3、磁子位置偏心不平衡搅拌过程中,容器应该处于盘面的中心位置,而磁子则应放于容器的中心位置。4、转速超过阈值调速必须由低速逐步调至高速,不允许高速档直接起动,以免搅拌子不同步,引起跳动。
一、通过弹簧的伸缩运动,推动活塞,排除部分空气,利用大气压吸入液体,再由活塞推动空气排出液体。空气活塞式移液器是如何工作的?当设定体积时,活塞移动到适当的位置。当操作按钮按到第一停点时,活塞排出的空气量与体积设置上显示的相同。将吸头浸入液体后,松开操作按钮。这将产生部分真空,并将指定体积的液体吸入尖端。再次按压到第一个停点位置,空气排出液体。为了完全清空尖端,将操作按钮按到第二停点(吹出)。二、外置活塞式移液器是通过分液管或吸头内活塞的连续运动来实现吸液和排液外置活塞式移液器是如何工作的?活塞在尖端内向下移动,与样品直接接触。活塞向上移动,将样品吸入尖端。排液时,活塞下降,所选体积被排出DLAB移液器系列dPette, dPette+, HiPette,TopPette, MicroPette, MicroPette Plus等手动、电动移液器为气体活塞式移液器,StepMate连续分配器为外置活塞式移液器。
选择正确的搅拌桨能令您的顶置式搅拌器展现出优越的搅拌效果。选择搅拌桨时需要考量:搅拌桨在搅拌时可以引起的介质流动方向;搅拌桨的应用范围主要取决于转速范围和它所能达到的最大扭矩。如果您需要液体中的气体处理<500 mPas,您可以选择径流式搅拌桨如果您需要均质化或悬浮液处理<500 mPas,您可以选择螺旋桨式或叶片式搅拌桨如果您需要中等粘度样品的处理>500 mPas,您可以选择锚式搅拌桨或扇片式搅拌桨搅拌桨应该放置在容器的什么位置?搅拌桨轴杆在容器中心位置搅拌桨距底部距离(h/d)=0.3 桨叶与底部距离;d:搅拌桨直径)只有位置摆放正确,才能获得良好的搅拌效果叶片式搅拌桨建议用中等速度的搅拌适用于低粘度及中等粘度物料的搅拌离心式搅拌桨桨叶可折叠,适用于细口径容器螺旋式搅拌桨建议用中等速度或高速的搅拌适用于中等粘度或高粘度物料的搅拌推荐用于液体中的均质化或悬浮液处理径流式搅拌桨建议用中等速度或高速的搅拌适用于粘度较小或中等粘度物料的搅拌,粘度不超过 500mPas推荐用于液体中气体的处理锚式搅拌桨建议用低速的搅拌适用于中等粘度和高粘度物料的搅拌选择正确的桨不仅可以充分发挥顶置搅拌的优
1、拧钉/磁吸附金属浴有何异同,是不是通过拧钉,就可以加大转速的设置?拧钉款金属浴主要还是给配套磁珠法的客户前处理使用,拧钉和磁吸都需要通过模块下面的铜块去识别转速,不是拧钉款就可以无下限设置转速。2、金属浴加热块,薄款和非薄款什么区别?薄款升温快,温度过冲稍大;非薄款,升温相对较慢,但温度稳定性好,过冲较小或无过冲。3、金属浴模块都是什么材质?大部分是铝材质,一部分是ABS工程塑料+铝材质。4、金属浴温度不稳定或过高是什么原因?可能是加热器或者温度控制器出现故障,建议检查加热器和温度控制器,及时修理或更换故障部件5、金属浴使用过程中注意事项①每次使用前后,用棉签沾蒸馏水清洗模块的锥孔,保证试管与锥孔壁接触充分;②显示温度(PV)与第三方测量温度相差0.1℃以上时,需要进行温度误差校正;③在使用仪器过程中,禁止按压(校准/ADJ)键;④如果使用在4℃恒温4小时以上的操作,必须清楚模块冷凝水;⑤防止位置需防潮或避免暴露烟尘环境;⑥定期净化设备。
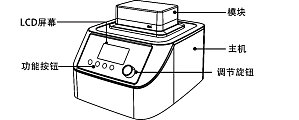
金属浴是产品前处理、生化反应控温的必备选择,可配置多种模块,可广泛应用于样品的保存和反应、DNA 扩增和电泳的预变性、血清凝固等各类生化样品恒温孵育流程。原理是采用微电脑控制,利用高纯度铝材料作为导热介质,以代替传统的水浴装置(水浴锅)。具有使用方便、控温范围大、精度高等特点。可根据试管大小配备不同孔径的加热块,对试管进行加热恒温。DLAB 金属浴系列分为:干式加热金属浴、恒温振荡金属浴、Mini 金属浴干式恒温金属浴干式恒温金属浴可根据试管大小配备不同孔径的加热块,对试管进行加热恒温。为了使热块的温度均匀,需采用高密度铝合金材料,保证优良的导热性。特点优势:控温范围更广,应用范围更广实时监控温度和时间多种承载模块适配更多规格耗材内置过温保护功能,安全稳定保温罩,防止热量散失、防止污染人性化设置旋钮,操作更简洁干式金属浴应用方向:生物分析:裂解、催化、分子生物相关化学分析环境监测消解实验土壤:140℃污水:100℃蔬菜:100℃茶叶:150℃恒温振荡金属浴特点优势:两种模块固定方式:磁吸附模式,无需工具即可快速更换模块;拧钉孔模式,可满足客户对磁珠法的实验需求;多种模块选择,支持程序编
1.手动移液器吸取粘稠或易挥发样品时怎样保证吸液量准确?吸取粘稠样品建议用外置活塞的连续分配移液器。如果使用内置活塞手动移液器,可以采用反向移液法,吸液时按压吸排液按钮至第二停点,排液时按压按钮至第一停点,可以保证吸液量的准确性。2.检查移液器是否漏液的方法?吸液后在液体中停 1-3 秒观察吸头内液面是否下降;如果液面下降首先检查吸头是否有问题。确认吸头没问题,有可能是活塞组件的问题,此时应联系厂家维修人员。3.移液器可以吸取有机溶剂吗?答:移液器不直接接触样品,理论上可以,但是因为有机溶剂的挥发性腐蚀性较强,可能对内部的活塞组件有影响,所以建议有机溶剂用含有过滤芯的吸头。4.移液器出现按压不回弹或者出现漏液和不吸液的现象应该怎么处理?如果是用了一段时间后出现此问题,有可能液体进入移液器内部,腐蚀活塞造成,建议更换活塞。如果是新的移液器,有可能是活塞和O形圈润滑不佳造成,使劲按下去,并多按几次使硅脂均匀涂抹开就可以解决了。5.移液器管嘴推出器按压后不回弹?可能原因:管推弹簧腐蚀,需更换单道管嘴推出器组件6.计数器字轮不齐,跳齿?可能原因:组装不良,齿轮磨损,或者弹片损坏,需更换计数器组
系统误差(不准确度):实际测得(比如10 次)的平均值与设定值的误差。平均测量体积与设定体积之差。系统误差的定性表示为“真实度”。真实度通常称为“准确度”。影响因素:系统误差可以通过移液器校准消除,因此定期地校准移液器并对其进行合理的维护来消除系统误差,从而提高移液器的准确度。随机误差(不精确度):实际测得(比如10 次)的值与平均值的误差,也就是整个移液系统是否准确。移液量与平均体积的偏差,即标准差。随机误差的定性表示为“精度”。影响因素:随机误差无法通过移液器校准消除,只能通过随机误差的产生因素去消除,比如提高移液操作的规范性、选择与移液器匹配的吸头,以及使用电动移液器等。系统误差和随机误差如何影响移液的总体准确度?准确度是真实度和精度的结合,因此系统误差和随机误差是结合在一起的。所以,定期地校准移液器并对其进行合理的维护来消除系统误差;提高移液操作的规范性、选择与移液器匹配的吸头,减小随机误差。根据测量不确定度表示指南(GUM),应根据已知系统误差校正测量结果。对于移液而言,需要从每次的移液量中减去系统误差。这不切实际,几乎没有用户这样做。而与此相对,“单次移液量使用的不确定度”
移液器使用方法1、设定移液体积:从大容量调整到小容量时,逆时针旋转刻度到所需容量;从小容量调整到大容量时,应先顺时针旋转调至超过设定体积刻度,然后再回到所需容量,这样可以保证移液的精度。2、匹配安装吸头:吸头选择原则:低吸附、锥度好、同心度好。对于单通道移液器,将移液器垂直插入吸头,轻轻按压并左右旋转,上紧即可;对于多通道移液器,将移液器的第一通道与第一个吸头对准,稍微倾斜插入,前后轻轻晃动确保安装牢固。注意:请不要重复撞击移液器,因为长期这样操作可能导致移液器的零部件因撞击变松动,甚至损坏刻度调节旋钮。3、吸液和放液:吸液前枪头先在液体中预润洗 2-3 次确保移液的精度和准度;吸液时,要确保移液器垂直且吸头浸没尽量浅一些,具体的浸入深度还应根据盛放液体的容器大小灵活掌握;放液时,吸头尖端靠在容器内壁(特别是对于 20μL 以下的体积),移液器角度 20° - 45°。体积低于 10μL 直接放液到容器底部;吸液和放液时务必要慢吸慢放,以免液体进入吸头过快而冲入到移液器内部腐蚀活塞。4、移液方式:正向移液:推荐用于水溶液,如缓冲液、稀释酸或碱,该技术通常用于移液和将样品或试剂混合到另一
a.根据需要处理样本容量的大小选择合适的量程,移液器最大量程的30%—100 % 是较佳的使用范;不要用小量程的移液器移取大体积的液体,以免影响准确度;同时,如果需要移取量程范围以外较大量的液体, 例如大于10ML以上的液体,建议使用瓶口分液器或大容量移液器工具, 如DispensMate瓶口分液器Levo Plus/Levo Me电动大容量。b.根据样本的性质选择不同的移液工具,空气体活塞式移液器适用常规水性溶液;而外置活塞式移液器适用于高蒸气压、高粘度、易挥发、易气泡的液体。c.根据移液的场景选择合适的移液器,普通试管或者离心管选用单通道移液器即可。对于比较深的试管,可以选用外置活塞式或者大容量移液器配合移液管操作。试剂槽,96/384孔板或者8联排,多通道(8通道/12通道)移液器较单通道款可以明显提高工作效率。
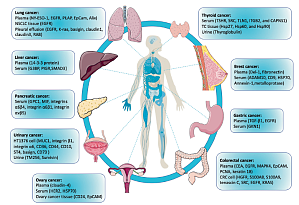
PART.1外泌体蛋白质功能外泌体是由各种活细胞释放的脂质双层膜包裹的小细胞外囊泡(small extracellular vesicle, sEV),外泌体蛋白质被包裹在膜内或包埋在表面。外泌体蛋白作为一种重要的外泌体货物,可以反映母体细胞的生理状态,在细胞间通讯中发挥重要作用。外泌体蛋白可以调节肿瘤发展,包括肿瘤相关免疫调节、微环境重建、血管生成、上皮间充质转换EMT、转移等。外泌体蛋白质的特征可以深入了解外泌体的产生、 ...
带您了解如何利用 iPSC 衍生的类器官进行科学研究