材料与仪器
器材:高速离心机,涡旋振荡器,培养箱,激光共聚焦显微镜
试剂:Aco-600 染料25T_,1 × PBS
耗材:100 KDa 超滤管5T,50 mL 离心管,1.5 mL 离心管
步骤
一、 染料工作液制备
1、 取染料管,加入 25 μL 水性缓冲液(推荐使用 PBS 或 Opti-MEM 溶解),配置成浓度为 25 μM 的储存液;
2、 使用涡旋振荡器充分振荡 1 min 至染料完全溶解;
3、 40°C 水浴 15 min(如有超声设备,可同步开启超声辅助溶解);
4、 取洁净 EP 管,对储存液进行分装;
5、 取适量储存液,用缓冲液稀释至 10 μM 的工作浓度。
二、 外泌体染色
1、 将 纯 化 的 细 胞 外 囊 泡 (EVs) 浓 度 调 整 至 1011 Particles/mL;
2、 按表 1 构建染色孵育体系:
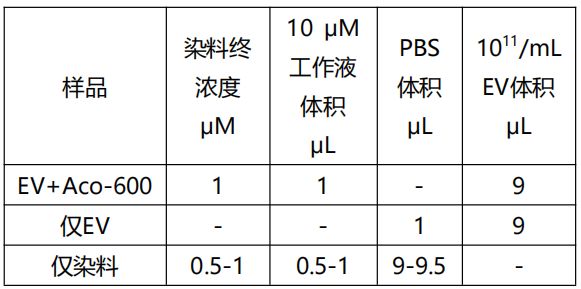
3、 加入染料工作液后,盖紧离心管盖,用枪头轻柔吹吸混匀,放置于 37℃ 环境,避光孵育 2 小时。
三、 去除游离染料
1、 染色完成后,在样品中加入 2 倍体积的 PBS,使用 100KDa 超滤管,以 3000×g 的离心力离心 5 ~10 min,进行超滤置换,去除溶液中游离的染料,将上室样品浓缩至原体积;
2、 重复上述超滤置换步骤 2 次;(完成本次实验后,请丢弃超滤管,切勿留作下次实验重复使用。)
3、 收集超滤管上室的样本,即为染色后的外泌体;
4、 染色后的外泌体建议尽快使用,若在 2 周内使用,可置于 4℃ 环境中避光保存;如需长期保存,可置于-80℃ 冷冻保存,保存时间过长可能影响下游实验效果。
四、 细胞摄取
1、 提前 24 小时铺种目标细胞;
2、 用不含外泌体的细胞培养基将染色样本稀释 5~10 倍,使染色 EV 浓度调整为约 5E+09 Particles/mL(超滤后外泌体得率约为 20%);
3、 吸除待处理细胞原有的培养基;
4、 加入含染色 EV 的新鲜培养基,在细胞培养箱避光孵育 24 小时;
5、 孵育 24 小时后,弃去含有染料的孵育液,用 PBS 清洗细胞 3 次;
6、 根据实验需求选择成像观察方式,可直接进行活体成像,也可固定细胞后成像观察;
7、 若选择固定细胞后成像,使用细胞固定剂在室温下固定 15 min(固定后观察细胞形态是否发生变化,部分固定液渗透压不稳定,可能导致细胞变形);
8、 弃去固定剂,用 PBS 清洗细胞 3 次,每次 5 min;
9、 使用含 DAPI 的封片剂进行封片(或先用 DAPI 进行核染 10 min,PBS 清洗 3 次,每次 5 min,之后进行封片);
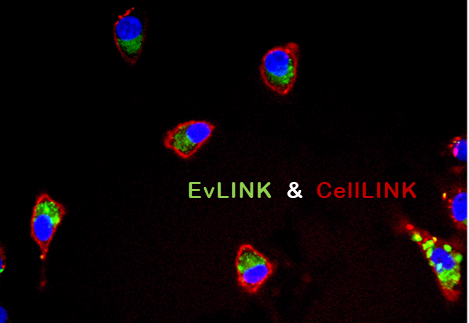
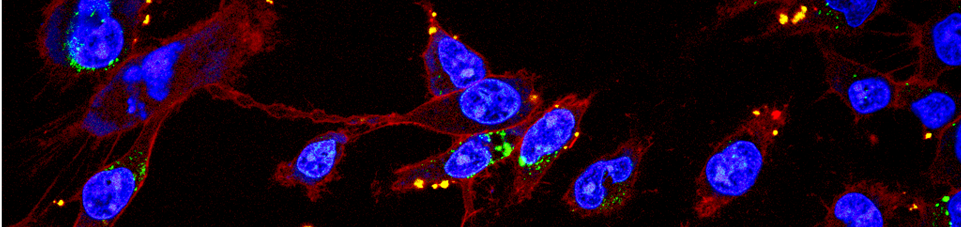
10、共聚焦成像:Aco-600 的荧光信号收集可以使用 488、514、543、559 或 561nm 的激光器,发射波长从 600 nm 开始收集,常用的通道名称是 RFP;
11、在成像时顺序扫描,避免同时扫描。先收集 Aco-600 的荧光信号,再收集 DAPI 信号(DAPI 的激发器也会激发 Aco-600)。
来源:丁香实验