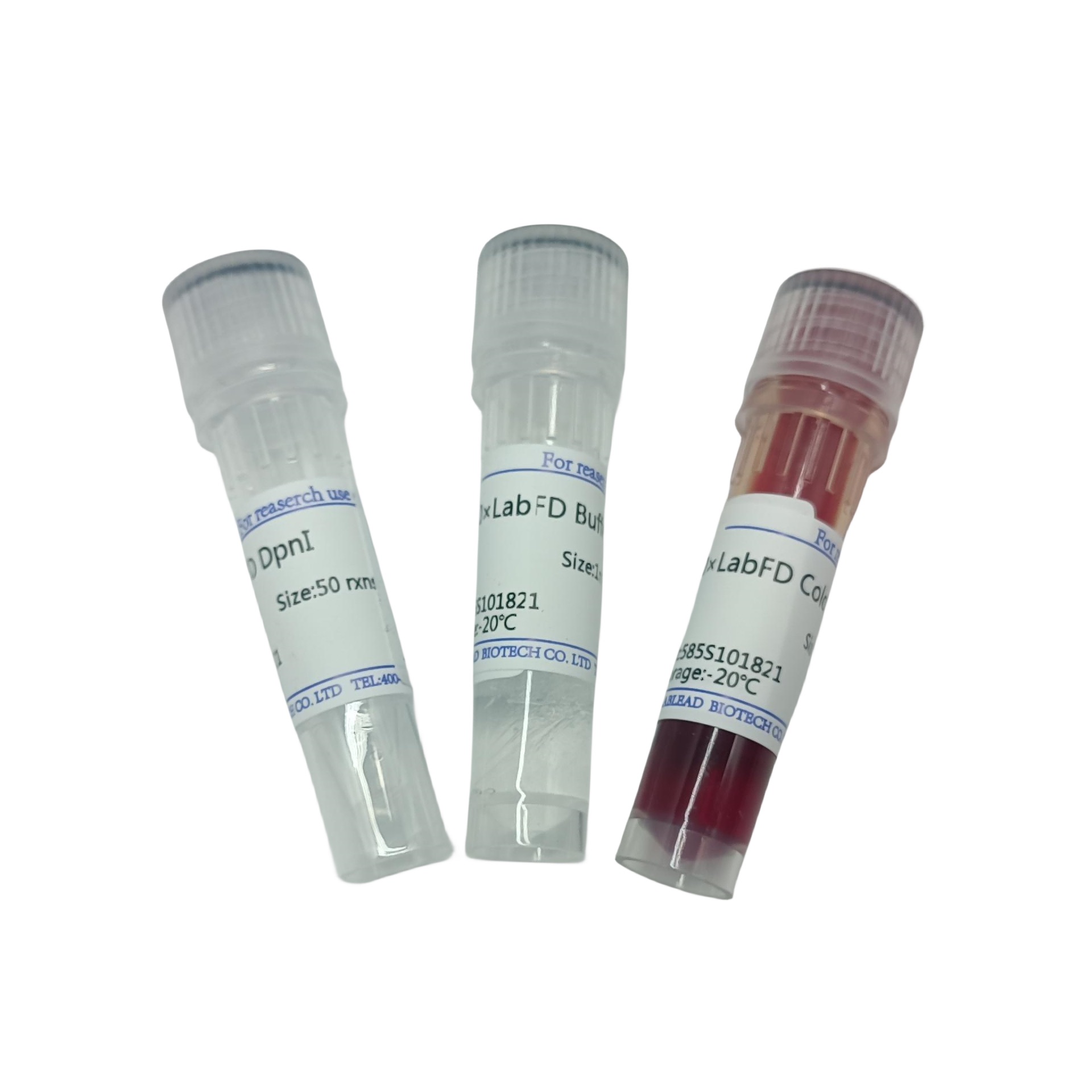
相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 保存条件:
-20℃
- 英文名:
LabFD DpnI
- 供应商:
LABLEAD
- 规格:
50 rxns
产品货号:F5585S
储存条件:-20℃
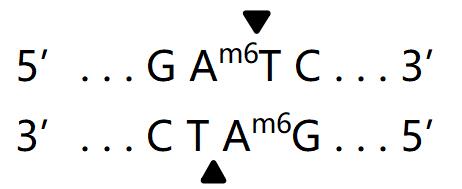
同裂酶:MalI
注:同裂酶对于不同的甲基化修饰可能具有不同敏感性。
产品组成
| 组分 | 规格 |
| LabFD™ DpnI | 50ul |
| 10×LabFD™ Buffer | 1ml |
| 10×LabFD™ Color Buffer | 1ml |
产品简介
LabFD™快速内切酶是一系列经过基因工程重组、能够在5~15 分钟内精确完成 DNA 切割的高保真限制性内切酶,适用于质粒 DNA、PCR 产物或基因组 DNA 等的快速酶切。LabFD™ 快速内切酶具有如下特点:5~15 分钟内即可完成酶切;共用一种酶切Buffer,大大简化酶切反应体系;良好的酶活冗余度,轻松应对底物过量或困难模板酶切。此外,LABLEAD去磷酸化、连接试剂在LabFD™酶切Buffer 中具有100%活性,支持一管化反应,提升“酶切-修饰-连接”的体验。
建议的反应条件:
1× LabFD™缓冲液;
37℃温育;
参照“DNA快速酶切流程”配制反应体系。
失活条件
80℃温育20min。
质量控制
功能活性检测
最适反应温度下,在20ul反应体系中,1ul LabFD™ DpnI能够在15min 内完全消化1ug pUC19 DNA。
超长时间温育检测
最适反应温度下,将1ul LabFD™ DpnI 与 1ugpUC19 DNA共同温育3h,未检测到其他核酸酶污染或星号活性引起的底物非特异性降解,延时酶切可能出现星号活性。
酶切-连接-再酶切检测
最适反应温度下,使用 1ul LabFD™ DpnI消化底物,回收酶切产物。在22℃下使用适量Fast T4 DNA Ligase可以将酶切产物重新连接。将连接产物再次回收后,使用相同的内切酶可以重新切开连接产物。
非特异性内切酶活性检测
最适反应温度下,将1ul LabFD™ DpnI与1ug超螺旋质粒DNA共同温育4h,使用琼脂糖凝胶电泳检测,质粒DNA仍然处于超螺旋状态。
蓝白斑检测
将含有单一lacZα基因的载体以1ul LabFD™ DpnI消化,重新连接后转化入大肠杆菌感受态细胞,涂布在含有对应抗生素、IPTG 和X-gal的LB培养基平板上。连接正确的产物会生长出蓝色菌落,而连接错误(即DNA末端切口不完整)的产物将得到白色菌落。对于LabFD™系列限制酶而言,白色菌落比例应小于1%。
使用方法
1.DNA快速酶切流程
1)在冰上按如下建议的加样顺序配制反应体系:
| 质粒 DNA | PCR 产物 | 基因组 DNA | |
| ddH2O | 15ul | 16ul | 30ul |
| 10×LabFD™ Buffer或10×LabFD™ Color Buffer | 2ul | 3uL注 | 5ul |
| 底物DNA | 2ul(up to 1ug) | 10ul (~0.2ug) | 10ul (5ug) |
| LabFD™ DpnI | 1ul | 1ul | 5ul |
| Total | 20ul | 30ul | 50ul |
注:本体系适用于经过纯化的PCR产物酶切,未纯化的PCR具备一定的离子强度,10xLabFDTMbuffer加入量可适当减少至2ul。但由于DNA聚合酶同时具有外切酶活性,会影响酶切产物,因此如下一步需进行克隆等操作,建议酶切前对PCR产物进行纯化。
2)轻柔吸打或轻弹管壁以混匀(切勿涡旋),然后瞬时离心以收集挂壁液滴;
3)37℃温育15 min(质粒),或15~30 min(PCR 产物),或30~60min(基因组DNA);
4)80℃温育20 min即可使酶失活,停止反应。
2.双酶切或多酶切
1)每种快速内切酶的用量为1ul,并根据需要适当扩大反应体系;
2)所有快速内切酶的体积总和不得超过总反应体系的1/10;
3)如果所用的几种快速内切酶的最适反应温度不同,应先以最适温度低的酶开始酶切,再添加最适温度较高的酶,在其最适反应温度下进行酶切反应。
适用于质粒的扩大反应体系
| DNA | 1ug | 2ug | 3ug | 4ug | 5ug |
| LabFD™ DpnI | 1ul | 2ul | 3ul | 4ul | 5ul |
| 10×LabFD™ Buffer或10×LabFD™ Color Buffer | 2ul | 2ul | 3ul | 4ul | 5ul |
| Total | 20ul | 20ul | 30ul | 40ul | 50ul |
注:如果总反应体系大于20ul,应适当增加温育时间,尽量使用水浴、金属浴或沙浴。
不同 DNA 中的酶切位点数量
| λDNA | ΦX174 | pBR322 | pUC57 | pUC18/19 | SV40 | M13mp18/19 | Adeno2 |
| 116 | 0 | 22 | 15 | 15 | 8 | 7 | 87 |
甲基化修饰影响
| Dam | Dcm | CpG | EcoKI | EcoBI |
| 不切割Dam’DNA | 无影响 | 无影响 | 无影响 | 序列可能重叠 剪切可能受影响 |
在不同反应缓冲液中的活性
| LabFD™ Buffer | Thermo Scientific FastDigest Buffer | NEB CutSmart® Buffer |
Takara QuickCut™ Buffer |
|
| 活性 | 100% | 100% | 100% | 100% |
注:活性数据来自LABLEAD限制酶标准反应体系下的检测
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验基因的体外定点突变是常用的分子实验技术,主要用于研究蛋白质结构与功能关系或者验证 microRNA 与靶基因是否结合。今天为大家介绍下基因突变质粒的构建原理与方法。第一阶段:野生型质粒构建1. 引物设计:根据需要验证的基因序列,设计需要扩增的基因片段引物。引物设计方法如下:(1)引物 F:5’ 端 - 保护碱基序列 + 限制性内切酶 1 酶切位点序列 + 基因正向引物序列 - 3’端(2)引物 R:5’ 端 - 保护碱基序列 + 限制性内切酶 2 酶切位点序列 + 基因反向引物序列 - 3’端
基因的体外定点突变是常用的分子实验技术,主要用于研究蛋白质结构与功能关系或者验证 microRNA 与靶基因是否结合。今天为大家介绍下基因突变质粒的构建原理与方法。第一阶段:野生型质粒构建1. 引物设计:根据需要验证的基因序列,设计需要扩增的基因片段引物。引物设计方法如下:(1)引物 F:5’ 端 - 保护碱基序列 + 限制性内切酶 1 酶切位点序列 + 基因正向引物序列 - 3’端(2)引物 R:5’ 端 - 保护碱基序列 + 限制性内切酶 2 酶切位点序列 + 基因反向引物序列 - 3’端
了一种新技术COMPARE-MS,该法将MBD柱层析法与MS-RE联用,互补了各自单用的弊处,能够快速、敏感的检测DNA甲基化情况,可用于临床标本检测,作为早期诊断和肿瘤分级的依据[56]。其过程是:用非待测区的内切酶和甲基化敏感的限制性内切酶同时消化DNA片段,随后通过MBD柱捕获,保留了含有甲基化区的片段,最后通过实时PCR扩增定量分析(见图9)。 图9:联合甲基化敏感性限制性内切酶的MBD(COMPARE-MS)示意图。用甲基化以外的位点的内切酶(A酶)与甲基化敏感的内切酶(B酶)联用