相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
大量
- 英文名:
Hieff NGS Library Quantification Kit for Illumina®, qPCR Master Mix
- 保质期:
有效期6个月
- 供应商:
翌圣生物科技(上海)股份有限公司
- 保存条件:
-20℃保存
- 规格:
500T
| 产品名称 | 产品编号 | 规格 | 储存 | 价格(元) |
| Hieff NGS® Library Quantification Kit for Illumina®, qPCR Master Mix | 12302ES05 | 500 T | -20℃ | 1526.00 |
| Hieff NGS® Library Quantification Kit for Illumina®, DNA Standard 1-6 | 12307ES09 | 6×96 μL | -20℃ | 2126.00 |
产品描述
本产品是用于lllumina®平台高通量测序文库浓度绝对定量的专用试剂盒,提供定量所需的DNA标准品、qPCR Master Mix、定量扩增引物和参比染料ROX。其中,DNA标准品包含经梯度稀释的六份450 bp的双链DNA片段溶液,浓度为20 pM-0.0002 pM;扩增引物对根据NGS文库接头序列P5和P7设计,可保证特异性扩增双端接头完整的文库分子;qPCR Master Mix是基于抗体法热启动的染料法qPCR预混液,可在不同长度、不同GC或AT含量样本中高效、特异扩增,实现精确定量。
本试剂盒已经过严格的质量和功能检测,试剂盒所有组分均达到DNA污染控制的严格质控要求,应用于NGS文库定量精确灵敏,且批间稳定,结果重现性优异。
产品组分
| 组分编号 | 组分名称 | 规格 | 12302ES05 | 12307ES09 |
| 12302-A | Hieff NGS® SYBR qPCR Master Mix (2×) | 5×1 mL | √ | -- |
| 12302-B | qPCR Primer Mix | 600 μL | √ | -- |
| 12302-C | 50×Low Rox | 200 μL | √ | -- |
| 12302-D | 50×High Rox | 200 μL | √ | -- |
| - | DNA Standards 1-6 | 6×96 μL | -- | √ |
1. 根据仪器类型选择合适的参比染料ROX。
| 类别 | 机型 |
| 不添加ROX | Bio-Rad CFX96™, CFX384™, iCycler iQ™, iQ™5, MyiQ™, MiniOpticon™, Opticon®, Opticon 2, Chromo4™; Cepheid SmartCycler®; Eppendorf Mastercycler®ep realplex, realplex 2 s; Illumina Eco qPCR; Qiagen/Corbett Rotor-Gene®Q, Rotor-Gene®3000, Rotor-Gene®6000; Roche Applied Science LightCyclerTM480; Thermo Scientific PikoReal Cycler. |
| 添加50×High Rox | Applied Biosystems 5700, 7000, 7300, 7700, 7900, 7900HT, 7900HT Fast; StepOne™, StepOnePlus™. |
| 添加50×Low Rox | Applied Biosystems 7500, 7500 Fast, ViiA™7; Stratagene MX4000™, MX3005P™, MX3000P™ |
Primer 1:5'-AAT GAT ACG GCG ACC ACC GA-3'
Primer 2:5'-CAA GCA GAA GAC GGC ATA CGA-3'
运输与保存方法
冰袋运输。所有组分应-20℃保存,qPCR Master Mix与ROX避光保存,有效期6个月;如短期内反复使用,qPCR Master Mix可解冻后于4℃避光暂存,有效期3个月。
注意事项
一、关于操作
1. 为了您的安全和健康,请穿实验服并戴一次性手套操作。
2. 请于使用前确保产品冻融和彻底混匀,短暂离心收集至管底后置于冰上备用。
3. 为保证产品品质,避免反复冻融超过30次!
4. 为避免样品交叉和气溶胶污染,推荐使用带滤芯的枪头,吸取不同样品时请更换枪头。
5. 试剂吸取时应保证枪头适当深入液体,排出时应确认枪头无残留。
二、关于文库稀释
文库需稀释至标准曲线有效Ct范围内进行定量,稀释比例可参照过往经验或使用其他测定方式测定的浓度作为参考(如NanoDrop®,Qubit®或Bioanalyzer)。使用本试剂盒可定量的文库浓度范围参见下表。
由于DNA在非缓冲环境中易降解,因此应使用缓冲稀释液(10 mM Tris-HCl,pH 8.0 [25℃] + 0.05% Tween 20)稀释文库,切勿使用水作为稀释液。测定时,文库应现测定现稀释,置于冰上待测,切勿使用以往配制的储存的稀释后文库。
表1 DNA Standard浓度
| DNA Standard | 摩尔浓度 | 质量浓度 | 拷贝数浓度 |
| Std 1 | 20 pM | 5.5 pg/μL | 12×106 copies/μL |
| Std 2 | 2 pM | 0.55 pg/μL | 12×105 copies/μL |
| Std 3 | 0.2 pM | 0.055 pg/μL | 12×104 copies/μL |
| Std 4 | 0.02 pM | 0.0055 pg/μL | 12×103 copies/μL |
| Std 5 | 0.002 pM | 0.00055 pg/μL | 12×102 copies/μL |
| Std 6 | 0.0002 pM | 0.000055 pg/μL | 12×101 copies/μL |
1. 进行qPCR实验时,应保证良好的实验操作规范,以防对工作区域、试剂、耗材、仪器、DNA标准品等造成污染。推荐将反应体系配制区和模板制备区进行物理隔离,并定时使用0.5%Naclo或10%漂白剂对各实验区域进行擦拭清理。
2. 反应体系配制过程中DNA Standards的加入应按照从低浓度至高浓度(DNA Standard 6至1)的顺序进行,每次移液都应更换新的枪头,以避免气溶胶污染。
3. 每次实验都应平行进行NTC阴性对照反应,配合融解曲线进行扩增特异性和体系污染程度分析。因扩增引物序列为Illumina®平台固定序列而非qPCR专用引物序列,且扩增循环数较多,NTC阴性对照反应出现引物二聚体扩增进而产生Ct属正常情况。正常情况下Ct (NTC) > Ct (DNA Standard 6) + 3。
四. 扩增曲线基线设置
因DNA Standard 1的摩尔浓度远远高于常规qPCR模板,其Ct往往非常小。而大部分qPCR仪器都默认将3-15循环设置为基线(Baseline),有时会将DNA Standard 1的Ct值误认为是测定时的噪声背景,继而影响标准曲线制作。手动设置基线(Baseline)为1-3循环可以有效避免这种情况发生。
五、文库长度矫正
为避免片段长度对文库绝对定量的影响,需要在定量结果计算时,对文库长度进行矫正。根据文库荧光染料SYBR® Green I结合DNA后产生的荧光强度与DNA分子量成正比的原则,根据以下公式进行文库浓度长度矫正。
矫正后的稀释文库浓度(pM)= [450 bp /文库平均长度(bp)] × 稀释文库的浓度(pM)
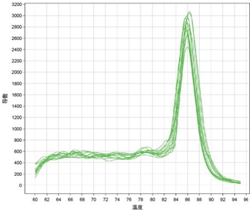
六、融解曲线分析
融解曲线在配合NTC阴性对照进行污染程度分析以及确认标准曲线最大有效Ct时至关重要,推荐每次实验都进行融解曲线采集步骤。本产品,DNA Standards产生的熔解曲线呈现特征单峰。
使用方法
一、解冻试剂
将Hieff NGS® qPCR Mix,Primer Mix,DNA Standards 1-6,文库稀释液(10 mM Tris-HCl, pH 8.0 + 0.05% Tween 20),ROX Dye(如需要)从冰箱中拿出,冰浴解冻。各试剂解冻后,涡旋混匀,短暂离心后置于冰上备用。
二、稀释文库
使用文库稀释液(10 mM Tris-HCl,pH 8.0 [25℃] + 0.05% Tween 20)对待测文库进行适当稀释。推荐稀释度为1:1000-1:100000。对于高浓度文库,可额外设置3个2倍稀释梯度,如按1:1000稀释文库,可额外设置1:2000,1:4000,1:8000稀释比例,以保证测定值在试剂盒所提供的标曲范围内。
三、反应体系配制
于反应管中配制如下体系,上下颠倒或涡旋振荡混匀,并短暂离心将反应液收集至管底。
表2 qPCR反应体系
| 名称 | 体积 |
| Hieff NGS® SYBR qPCR Master Mix(2×) | 10 μL |
| qPCR Primer Mix | 1 μL |
| Diluted DNA Library/DNA Standard 1-6/ddH2O* | 2 μL |
| ddH2O | 7 μL |
| Total | 20 μL |
四、qPCR运行程序
将反应管置于qPCR仪中,按下述条件设置qPCR反应程序,并运行(熔解曲线可根据仪器默认即可)。
表3 qPCR程序
| 步骤 | 温度 | 时间 | 循环数 |
| 预变性 | 95℃ | 5 min | 1 cycle |
| 循环反应 | 95℃ | 10 sec | 40 cycles |
| 60℃ | 45 sec* | ||
| 熔解曲线 | 95℃ | 15 sec | 1 cycle |
| 60℃ | 60 sec | ||
| 95℃ | 15 sec |
五、数据分析
1. 标准曲线制作
1)根据复孔间Ct差异≤0.2的原则,对DNA Standards原始Ct进行过滤,并计算平均Ct。
2)使用有效范围内的Ct(作为纵坐标)和Log[pM](作为横坐标)绘制标准曲线。参照NTC阴性对照Ct确认标准曲线Ct有效范围。
如Ct (NTC) > Ct (DNA Standard 6) + 3,则最大有效Ct为Ct (DNA Standard 6),应使用DNA Standard 1-6所产生的Ct绘制标准曲线;
如Ct (DNA Standard 6) + 3 > Ct (NTC) > Ct (DNA Standard 5) + 3,则最大有效Ct为Ct (DNA Standard 5),应使用DNA Standard 1-5所产生的Ct绘制标准曲线;
如Ct (DNA Standard 5) + 3 > Ct (NTC) > Ct (DNA Standard 4) + 3,则最大有效Ct为Ct (DNA Standard 4),应使用DNA Standard 1-4所产生的Ct绘制标准曲线;
基于定量准确性考虑,请至少使用4个Ct (DNA Standards)绘制标准曲线。如Ct (DNA Standard 4) + 3 > Ct (NTC),提示定量体系存在严重污染,需更换体系中所有组分后重复试验。
3)绘制的标准曲线相关系数R2应不低于0.99,斜率应位于-3.1至-3.6之间(表示扩增效率位于90%-110%之间)。如标准曲线参数不佳,应重复试验。
2. 文库浓度计算
稀释文库的Ct只有位于标准曲线有效Ct范围之内才可用于浓度计算,同时应对文库进行长度矫正。可根据下述公式计算原始文库浓度(nM):
原始文库浓度(nM)= [450 bp /文库平均长度(bp)] × 稀释文库的浓度(pM)× 稀释倍数/1000
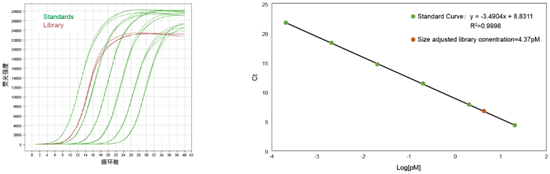
六、使用案例
用Hieff NGS® DNA Library Quantification Kit for Illumina®定量嗜盐杆菌基因组DNA文库,文库GC含量为70%,长度450 bp。将文库稀释10000倍上机检测,结果如下图所示。根据标曲及公式,文库终浓度=4.37 pM × 稀释倍数10000=43.7 nM。
常见问题
| 问题 | 可能原因与解决方法 |
| 扩增效率不在90%-110% | 1. 如Ct (NTC) - Ct (DNA Standard 6) < 3或者Ct (DNA Standard 6) - Ct (DNA Standard 5) < 3.1,且计算扩增效率超过100%,提示反应体系有污染。应根据NTC阴性对照的融解曲线确认污染源(文库污染或DNA Standards污染)。 2. 不恰当的基线基线(Baseline)设置。手动调整基线(Baseline)为1-3循环。 3. 移液精确度差,重复实验,确保所有试剂使用前完全溶解并混匀。 |
| 相关系数R2 < 0.99 | 1. 移液精确度差,重复实验,确保所有试剂使用前完全溶解并混匀。 2. 仪器相关问题,确保仪器与ROX匹配使用。 |
| 标曲扩增曲线分布不均一 | 1. Ct (DNA Standard 6) - Ct (DNA Standard 5) < 3.1,提示反应体系有污染。根据NTC 阴性对照的融解曲线确认污染源(文库污染或DNA Standards污染)。 2. Ct (DNA Standard 2) - Ct (DNA Standard 1) < 3.1,提示基线基线(Baseline)设置不当。手动调整基线基线(Baseline)为1-3。 3. DNA Standards之间的ΔCt > 3.6,提示扩增效率差。确认所有试剂在使用前都已充分解冻并彻底混匀;确认所有组分浓度正确以及反应程序无误。 4. 长时间强光照射会导致qPCR Master Mix荧光值下降,进而造成ΔCt > 3.6。应按照推荐方式避光贮存试剂。 |
| 复孔重复性差 | 1. 移液精确度差,重复实验,确保所有试剂使用前完全溶解并混匀。 2. 仪器相关问题,确保仪器与ROX匹配使用。 |
| 文库稀释液ΔCt不在合理范围(如2倍稀释文库,ΔCt为0.9-1.1) | 1. 移液精确度差,重复实验,确保所有试剂使用前完全溶解并混匀。 2. 文库难于扩增。GC/AT含量过高或长度超过1 kb的文库扩增效率较差。 3. 文库降解。文库应现用现稀释,稀释好的文库应置于冰上备用。 |
| 文库各稀释度计算的初始文库浓度差异超过10% | 1. 移液精确度差,重复实验,确保所有试剂使用前完全溶解并混匀。 2. 文库难于扩增。GC/AT含量过高或长度超过1 kb的文库扩增效率较差。 3. 文库降解。文库应现用现稀释,稀释好的文库应置于冰上备用。 |
| 稀释文库Ct值不在标曲Ct的有效范围 | 1. 使用有效范围内的Ct值计算文库浓度。当Ct (稀释文库) < Ct (DNA Standard 1),提示文库稀释度不够,应提高文库稀释倍数重复实验。 2. Ct (稀释文库) > Ct (DNA Standard 6),提示文库稀释度过高,应减少稀释倍数重复实验。 3. 推荐稀释度为1:1000-1:100000。对于高浓度文库,可额外设置3个2倍稀释梯度,如按1:1000稀释文库,可额外设置1:2000,1:4000,1:8000稀释比例,以保证测定值在试剂盒所提供的标曲范围内。 |
| DNA Standard 1扩增曲线异常 | 不恰当的基线基线(Baseline)设置。手动调整基线(Baseline)为1-3循环。 |
| DNA Standards有扩增,而文库没有或Ct很大 | 1. 文库接头序列错误。核对文库末端序列与试剂盒提供的引物序列是否匹配。 2. 稀释度过高。减少稀释倍数,重复实验。 3. 文库降解。文库应现用现稀释。 |
相关产品
| 建库试剂盒 | 产品编号 | 规格 |
| Hieff NGS® MaxUp II Dual-mode mRNA Library Prep Kit for Illumina® | 12300ES08/24/96 | 8/24/96 T |
| Hieff NGS® Ultima DNA Library Prep Kit for Illumina® | 12199ES08/24/96 | 8/24/96 T |
| Hieff NGS® MaxUp II DNA Library Prep Kit for Illumina® | 12200ES08/24/96 | 8/24/96 T |
| Hieff NGS® OnePot DNA Library Prep Kit for Illumina® | 12203ES08/24/96 | 8/24/96 T |
| Hieff NGS® OnePotTM II DNA Library Prep Kit for Illumina® | 12204ES08/24/96 | 8/24/96 T |
| Hieff NGS® Fast Tagment DNA Library Prep Kit for Illumina® (for 1 ng) | 12206ES08/24/96 | 8/24/96 T |
| 文库构建磁珠 | 产品编号 | 规格 |
| Hieff NGS® cfDNA Clean Beads(100~200 bp) | 12599ES03/08/56 | 1/5/60 mL |
| Hieff NGS® Smarter DNA Clean beads (50 bp以上) | 12600ES03/08/56/75 | 1/5/60/450 mL |
| Hieff NGS® DNA Selection Beads(Superior AMPure XP alternative) | 12601ES03/08/56/75 | 1/5/60/450 mL |
| Hieff NGS® RNA Cleaner | 12602ES03/08/56/75 | 1/5/60/450 mL |
| Hieff NGS® mRNA Isolation Master Kit | 12603ES24/96 | 24/96 T |
| 建库接头 | 产品编号 | 规格 |
| Hieff NGS® Complete Adapter Kit for Illumina®, Set 1 | 12615ES04/16 | 12×4/12×16 T |
| Hieff NGS® Complete Adapter Kit for Illumina®, Set 2 | 12616ES04/16 | 12×4/12×16 T |
| Hieff NGS® Complete Adapter Kit for Illumina®, Set 3 | 12617ES04/16 | 12×4/12×16 T |
| Hieff NGS® Complete Adapter Kit for Illumina®, Set 4 | 12618ES04/16 | 12×4/12×16 T |
| Hieff NGS® Tagment Index Kit for Illumina®,(96 Index) | 12610ES96 | 96 T |
| 建库模块 | 产品编号 | 规格 |
| Hieff NGS® Fast-Pace DNA Fragmentation Reagent | 12609ES24/96 | 24/96 T |
| Hieff NGS® Fast-Pace End Repair/dA-Tailing Module | 12608ES24/96 | 24/96 T |
| Hieff NGS® UltimaTM DNA Ligation Module | 12604ES24/96 | 24/96 T |
| 2×Super Canace®Ⅱ Uracil High-Fidelity Mix for Library Amplification | 12620ES24/96 | 24/96 T |
| 2×Super Canace® II High-Fidelity Mix for Library Amplification | 12621ES24/96 | 24/96 T |
| Hieff NGS® MaxUp rRNA Depletion Kit (Human/Mouse/Rat) | 12253ES08/24/96 | 8/24/96 T |
| 文库定量 | 产品编号 | 规格 |
| Hieff NGS® Library Quantification Kit for Illumina®, qPCR Master Mix | 12302ES05 | 500 T |
| Hieff NGS® Library Quantification Kit for Illumina®, DNA Standard (1-6) | 12307ES09 | 6×96 μL |
| dsDNA HS Assay Kit for Qubit® | 12640ES60/76 | 100/500 T |
| 1×dsDNA HS Assay Kit for Qubit® | 12642ES60/76 | 100/500 T |
| 多重PCR | 产品编号 | 规格 |
| Hieff® Multiplex PCR Kit | 13279ES60/76 | 100/500 T |
| 2×Hieff NGS® HG Multiplex PCR Master Mix 2×高GC多重PCR预混液 | 13283ES03/08/50/60/76 | 1/5×1/50/250/500mL |
HB200628
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验[3];但如果您是做等位基因分型或者法医相关应用,可以根据实际情况,通过合理设置基线、适当调整模板及 PCR 反应体系其他组分的浓度、降低反应循环数以及进行不对称 PCR 的方式来改善结果。 最后,我们回到文章开头的那个案例,沟通后我们发现客户采用的是 SYBR Green I 染料法对 NGS 文库进行绝对定量,NGS 文库构建过程中,需要在测序片段两端加上可以被测序仪识别的「接头」序列,而这些「接头」大部分序列是一致的,导致文库中存在大量异质但又相互关联的 DNA 序列,在定量过程中形成异质双链,进而引发
文献速递:全面液体分析循环肿瘤DNA和蛋白质生物标志物为评估预后带来新的可能
,可在2h内处理24个样品。 QIAseq cfDNA All-in-One Kit能够用于将任何液体活检样本的ccfDNA从血浆转换为NGS文库,让文库制备更加方便和高效,以满足外显子组或全基因组测序的需求。这个过程包括两个主要步骤:从血浆中提取ccfDNA,以及NGS的文库制备。提取出的ccfDNA通常约为170 bp,故文库制备之前不需要片段化。洗脱液可直接用于文库制备。 参考文献: [1] Zhixiong Cai, et al. Comprehensive liquid profiling
NGS已成为生命科学领域中基因组学和转录组学研究的金标准。虽然它与桑格测序等方法有某些核心相似之处,但NGS所能实现的绝对的高通量水平使它与其他方法截然不同,并彻底改变了科学家的工作方式。 RNA测序(RNA-seq)尤其处于NGS功能应用的前言沿。RNA-seq最简单的形式允许我们在取样时确定样本中的RNAs的丰度。转录组是一个高度动态的细胞特征,并打开了一个巨大发掘潜力的世界。对药物、各种疾病状态、转录后修饰和选择性剪接转录本的反应变化只是 RNA-Seq 使其能够发现的一些例子
 技术资料
技术资料暂无技术资料 索取技术资料