相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 规格:
50次/200次
| 规格: | 50次 | 产品价格: | ¥798.0 |
|---|---|---|---|
| 规格: | 200次 | 产品价格: | ¥2568.0 |
碧云天研发生产的5D微卫星不稳定性检测试剂盒(荧光PCR-毛细管电泳法),即5D Microsatellite Instability Assay Kit by Fluorescent PCR and Capillary Electrophoresis,简称MSI Assay kit,也被称为5D微卫星不稳定性分析试剂盒或MSI Analysis System,是一种通过荧光PCR和毛细管电泳,快速、高灵敏地检测人类细胞微卫星不稳定性的试剂盒。
微卫星(Microsatellite)是普遍存在于人类基因组中长度为1-6个碱基对的短串联重复(Short tandem repeat, STR) DNA序列,重复次数为10-50次,包括单核苷酸、双核苷酸或多核苷酸重复序列[1]。微卫星不稳定性(Microsatellite instability, MSI)是指由于基因组中短重复核苷酸序列的缺失或插入导致DNA序列长度改变,可以用于衡量DNA复制错误发生频率。根据出现的MSI的程度,可将MSI分为高频微卫星不稳定性(MSI-high, MSI-H)和低频微卫星不稳定性(MSI-low, MSI-L)。MSI主要由四种错配修复(Mismatch-repair, MMR)蛋白(MLH1、MSH2、MSH6、PMS2)修复。MMR基因的遗传和表观遗传学(如甲基化等)改变会导致MMR蛋白功能缺失,从而导致错配修复缺陷(MMR deficiency, dMMR)发生,引起MSI [2]。MSI与肿瘤的发生密切相关,但在不同肿瘤中的发生率存在较大差异,已知发生率较高的实体瘤包括子宫内膜癌、结直肠癌和胃癌等。MSI的检测具有重要的临床意义。林奇综合征(Lynch syndrome)是一种常染色体显性遗传病,与结直肠癌(Colorectal cancer, CRC)和子宫内膜癌(Endometrial cancer)的发生有高度相关性,可通过MSI检测进行排查;MSI检测可用于辅助肿瘤的诊断和分类;作为结直肠癌预后和治疗的重要参考指标;肿瘤免疫治疗的疗效预测[3]。此外,MSI还可用于dMMR导致的生殖系统缺陷患者的临床诊断[3]。
检测MSI的方法主要包括免疫组化法(IHC)、检测组织切片中MMR蛋白(MLH1、MSH2、MSH6、PMS2)的表达情况、PCR法比较正常样品和肿瘤样品中特定的微卫星序列扩增片段大小等。免疫组化法检测中,在某些情况下,MMR蛋白虽失去修复错配的能力但仍可以与抗体结合,可能导致假阳性结果。相比之下,PCR法得出的结果更为可靠,具有更高的准确度、灵敏度和特异性。
通常情况下,MSI分析需至少检测5个微卫星位点。目前国内外权威指南推荐的Panel有两个:一个是2B3D Panel,包含两个单核苷酸位点(BAT25和BAT26)以及3个双核苷酸位点(D2S123、D5S346和D17S250);另一个是5D Panel,包含五个单核苷酸位点(BAT25、BAT26、NR21、NR24和NR27)[4]。上述两个MSI检测Panel在检测特异性、灵敏度虽有细微差异,但均已经过大量研究数据验证,具有参考性。碧云天同时提供基于5D Panel (D8501)及2B3D Panel (D8503)的MSI检测试剂盒,用户可根据研究需要自行选择相应的试剂盒。
本试剂盒是基于5D Panel的MSI检测试剂盒,提供5对荧光标记引物的混合物,可用于上述5个单核苷酸位点的多重扩增,且其特异性经过实验验证,具体信息如下表所示。
| Marker Name | Gene | GenBank ID | Size Range | Fluorescent Marker |
| BAT25 | c-kit | X06182 | 150-154bp | HEX |
| BAT26 | hMSH2 | U04045 | 179-184bp | FAM |
| NR21 | SLC7A8 | Y18483 | 108-112bp | FAM |
| NR24 | Zinc finger 2 | X60152 | 127-132bp | TAM |
| NR27 | Inhibitor of apoptosis protein-1 | AF070674 | 83-87bp | HEX |
注:表中所列出的等位基因片段大小为使用本试剂盒提供的引物及试剂进行多重扩增,然后使用3730xl DNA Analyzer与50cm毛细管分析所得。当使用不同的扩增试剂或仪器时,等位基因片段的大小可能略有变化。
使用本试剂盒进行多重荧光PCR及毛细管电泳分析的结果请参考图1。
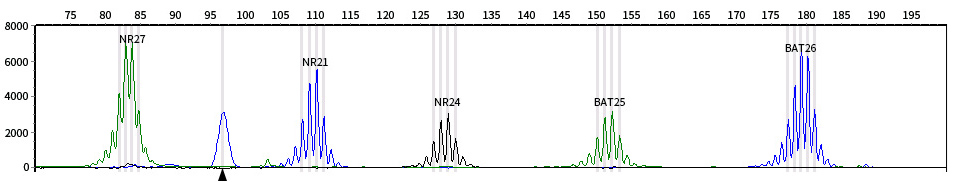
图1. 碧云天5D微卫星不稳定性检测试剂盒(荧光PCR-毛细管电泳法) (D8501)用于HEK293T细胞基因组DNA的检测效果图。以100ng HEK293T细胞基因组DNA为模板使用本试剂盒进行多重PCR扩增,产物使用ABI测序仪(3730xl DNA Analyzer)与50cm毛细管分析。x轴代表产物及内标GeneScan™ -500 LIZ的碱基数,y轴代表相对荧光强度。从左始依次为NR27 (HEX标记,绿色峰)、NR21 (FAM标记,蓝色峰)、NR24 (TAM标记,黑色峰)、BAT25 (HEX标记,绿色峰)、BAT26(FAM标记,蓝色峰)5个单核苷酸位点对应的峰。黑色三角形所标记峰为杂峰,不影响最终样品结果分析。实际检测结果会因样品、检测仪器等的不同而存在差异,图中检测结果仅供参考。
本试剂盒采用PCR法,提供了扩增上述微卫星位点序列所需试剂,用户可在扩增完成后通过毛细管电泳分析待测样品及对应正常样品的扩增产物生成的等位基因图谱,并进行对比。当测试样品相较于正常样品呈现波峰的移动或数目改变,即等位基因移动或出现新的等位基因,则称为微卫星不稳定。通常微卫星位点中40%及以上的位点出现不稳定时为高频微卫星不稳定(MSI-H),小于40%的微卫星位点出现不稳定时为低频微卫星不稳定(MSI-L)。对于本试剂盒,出现2个及2个以上的微卫星不稳定位点则可判定为MSI-H,具体可参考图2。
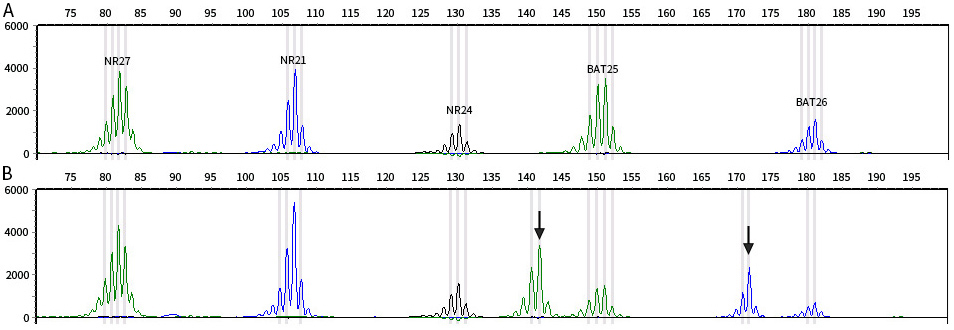
图2. 碧云天5D微卫星不稳定性检测试剂盒(荧光PCR-毛细管电泳法) (D8501)进行微卫星不稳定性分析示意图。使用本试剂盒分别对正常样品(图A)和MSI阳性的测试样品(图B)进行MSI检测及分析。测试样品中出现了正常样品中不存在的新等位基因(黑色箭头所示),表明测试样品在该位点存在MSI。从图中可以看出,测试样品中BAT25及BAT26这两个位点均出现MSI,因此该样品可判定为MSI-H。实际检测结果会因样品、检测仪器等的不同而存在差异,图中检测结果仅供参考。
本试剂盒同时提供包含上述5个微卫星位点标记基因的PCR对照模板(Control Template),可辅助判断试剂盒是否能正常工作,结果请参考图3。
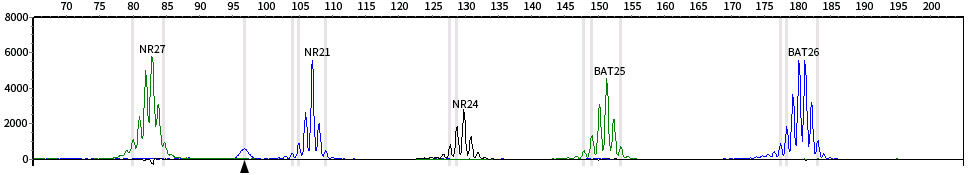
图3. 碧云天5D微卫星不稳定性检测试剂盒(荧光PCR-毛细管电泳法) (D8501)用于对照模板(Control Template)的检测效果图。对照模板用量为5ng,其它条件和图1相同。实际检测结果会因样品、检测仪器等的不同而存在差异,图中检测结果仅供参考。
总体积为10µl的扩增体系时,本试剂盒的小包装和中包装分别可以进行50次和200次反应。
包装清单:
| 产品编号 | 产品名称 | 包装 |
| D8501S-1 | MSI PCR Mix (2X) | 250μl |
| D8501S-2 | 5D MSI Primer Pair Mix (10X) | 50μl |
| D8501S-3 | Control Template | 25μl |
| D8501S-4 | Ultrapure Water | 200μl |
| — | 说明书 | 1份 |
| 产品编号 | 产品名称 | 包装 |
| D8501M-1 | MSI PCR Mix (2X) | 1ml |
| D8501M-2 | 5D MSI Primer Pair Mix (10X) | 200μl |
| D8501M-3 | Control Template | 100μl |
| D8501M-4 | Ultrapure Water | 800μl |
| — | 说明书 | 1份 |
保存条件:
-20ºC保存,一年有效。其中5D MSI Primer Pair Mix (10X)须避光保存。
注意事项:
建议使用带滤芯的吸头配制PCR体系,这样可以最大限度的避免污染导致的假阳性。推荐BeyoGold™无菌滤芯盒装吸头(FTIP631/FTIP635/FTIP638)。
5D MSI Primer Pair Mix (10X)中含有荧光染料,保存本产品或设置荧光PCR反应时应避免强光照射,以尽量避免荧光淬灭问题。
经测试,本试剂盒反复冻融10次对使用效果无显著影响,但仍需尽量避免反复冻融。反复冻融可能使产品性能下降。
本试剂盒提供的5个微卫星位点标记基因的PCR对照模板(Control Template),仅用于辅助判断试剂盒是否能正常工作,不能作为正常样品的标准品。
样品进行多重荧光PCR后,需要使用毛细管电泳仪进行分离基因分析。当使用不同的聚合酶或仪器组合时,等位基因的大小可能会有所不同。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验相关专题 贾蕊 朱若华* (首都师范大学 化学系 北京 100037) 摘 要 毛细管电泳法以其进样量少、操作简便、分辨率高、易于分离和定量、试剂消耗量少、分析时间短等优点,越来越广泛地应用于酶体系的动力学研究中。本文介绍了近三年来毛细管电泳法在酶反应动力学研究中的应用,包括酶反应动力学参数的测定、抑制动力学以及蛋白质-药物和蛋白质-蛋白质络合常数的测定三个部分。 关键词 毛细管电泳 酶 动力学 抑制剂 络合常数
大多是采用琼脂糖凝胶电泳法,首先检测CAMV-35S启动子和NOS终止子进行筛选,然后检测EPSPS抗草甘膦基因,操作烦琐、费时。本研究利用双重PCR技术同时扩增上述基因片段,用激光诱导荧光-毛细管电泳高效、快速检测PCR产物,显著提高了检测效率,并使灵敏度大为增加。本方法所需样品量少(nl级),快速、灵敏和准确,已成功用于实际转基因大豆样品的分析。1 材料和方法1.1 仪器与试剂毛细管电泳-激光诱导荧光检测装置(自行组装),其中氦氖激光器(543.5nm,JDS Uniphase,USA)参数
摘要: 毛细管电泳法以其进样量少、操作简便、分辨率高、易于分离和定量、试剂消耗量少、分析时间短等优点,越来越广泛地应用于酶体系的动力学研究中。本文介绍了近三年来毛细管电泳法在酶反应动力学研究中的应用,包括酶反应动力学参数的测定、抑制动力学以及蛋白质-药物和蛋白质-蛋白质络合常数的测定三个部分。 1967年Hjerten最早提出毛细管电泳技术,并在3mm内径的管子中使用高场强进行自由溶液的区带电泳(CZE)。到了20世纪80年代,毛细管电泳技术取得了突破性的进展,Jorgenson等用75
 技术资料
技术资料暂无技术资料 索取技术资料