万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 提供商:
北京诺禾致源科技股份有限公司
- 服务名称:
翻译后修饰蛋白质组学
motif分析
分析修饰位点上下游固定长度(7个氨基酸)的氨基酸出现频率,可以统计特定的修饰位点的基序(motif),进而研究调控修饰的酶。
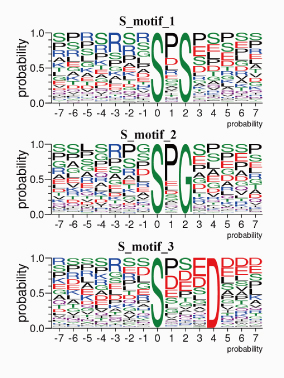
磷酸化激酶统计图
图中纵向代表样品名称,横向为每个样品预测到激酶类型的个数。
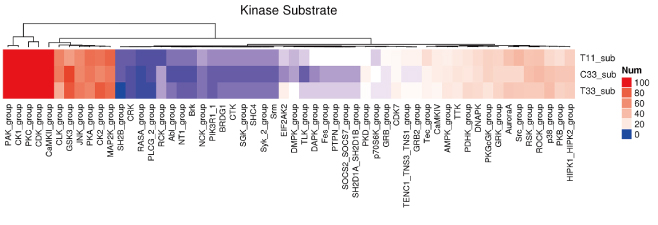
差异蛋白火山图
横坐标表示差异蛋白的差异倍数(log2值),纵坐标表示P-value(-log10值),黑色代表差异不显著的蛋白,红色代表上调蛋白,绿色代表下调蛋白。
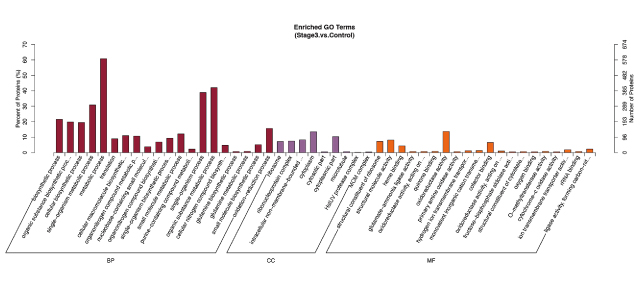
GO富集分析
横坐标表示GO三个大类(细胞组分、分子功能、生物过程)的富集结果,纵坐标为与该GO相关的差异蛋白数目占GO注释的所有差异蛋白数目的百分比。
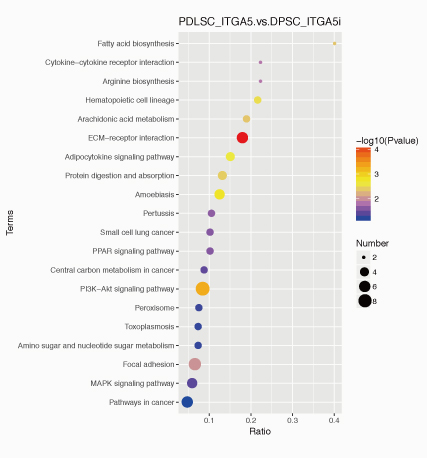
差异蛋白KEGG富集气泡图
横坐标为相应通路中差异蛋白的数目与鉴定出的总蛋白数目的比值,值越大,说明在该通路中差异蛋白富集程度较高。点的颜色代表超几何检验的P-value值,值越小,说明检验的可靠性越大、越具统计学意义。点的大小代 表相应通路中差异蛋白的数目,越大,该通路中差异蛋白就越多。
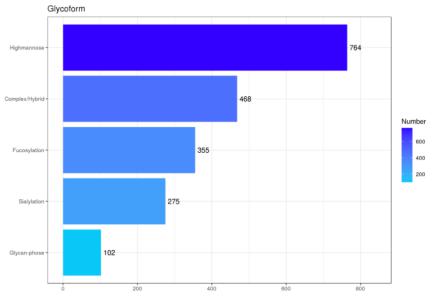
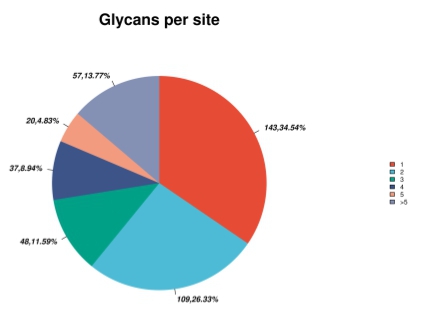
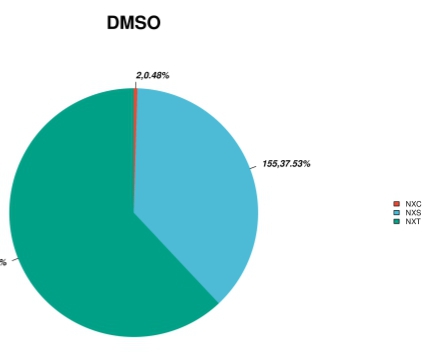
糖型分布统计
每个蛋白发生糖基化修饰的位点分布
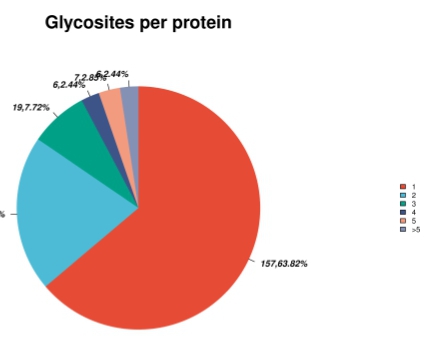
每个糖基化位点所对应的糖蛋白分布
修饰位点的序列基序分布
丙二酰化蛋白质组
蛋白质丙二酰化(malonylation)是指在酶的催化下把丙二酰基团(如丙二酰辅酶A等供体)共价结合到底物蛋白质的赖氨酸残基上的过程,此过程是可逆的。赖氨酸本身是带有正电荷的,丙二酰化发生后,将正电荷改变成负电荷,这种对蛋白带电性的改变会影响蛋白构象和蛋白间相互作用。
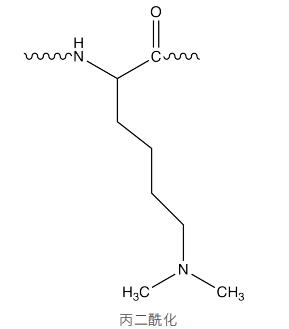
丙二酰化作为近些年新发现的酰化修饰类型,在代谢过程方面有着重要作用,尤其是能量代谢和光合作用方面,可影响脂肪酸的合成、线粒体呼吸、糖酵解、植物抗逆、炎症反应、2型糖尿病等。
磷酸化蛋白质组
蛋白质的磷酸化(Phosphorylation)是指由蛋白激酶(protein kinase, PK)催化的把 ATP 或 GTP γ位的磷 酸基转移到底物蛋白质的特定位点(氨基酸残基 Ser、Tyr、Thr)上的过程,其逆转过程是由蛋白磷酸酶 (protein phosphatase, PPase)催化的,称为蛋白质的脱磷酸化(去磷酸化)。
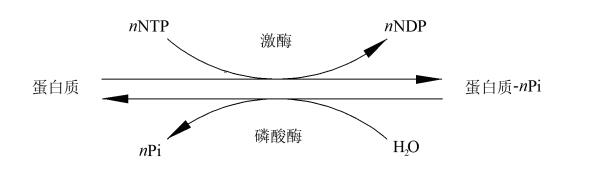
蛋白质的磷酸化和去磷酸化是调节和控制蛋白质活力和功能的最普遍、也是最重要的调控机制,具有重要的研究价值,广泛应用于微生物、植物和动物的研究中。磷酸化参与各种生理和病理过程,调控细胞的增殖、发育、分化、凋亡等生命活动,广泛运用在抗逆境抗胁迫,细胞自噬,细胞周期,信号通路,昼夜节律,生长发育和癌症机理等研究领域。癌症相关研究中,对于肿瘤的分子分型、致病机制研究和治疗靶点选择,都有着非常重要的意义。

泛素化蛋白质组
蛋白质泛素化(Ubiquitination)是指一个或多个泛素分子在一系列酶的作用下与底物蛋白质分子共价结合的翻译后修饰过程。泛素(Ubiquitin)是一种由76个氨基酸构成,在真核生物中广泛存在并具有高度保守性的多肽。
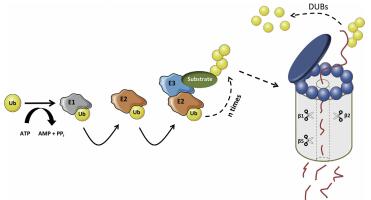
泛素-蛋白酶体降解途径(ubiquitin-pro-teasomepathway, UPP)作为泛素化的基础功能介导了真核生物体内80%~85%的蛋白质降解,在新合成蛋白的质控与蛋白行使完功能后的降解再循环利用中发挥着至关重要的作用。通过对蛋白质稳定性、定位、活性以及相互作用的调控,泛素化修饰广泛参与了诸如转录调节、DNA 损伤修复、细胞周期、细胞凋亡、囊泡运输等生理过程,在细胞的增殖与分化,细胞周期,细胞凋亡;肿瘤的发生发展,神经性退行性疾病;植物非生物胁迫、功能基因挖掘、植物细胞器发育等方面具有广泛的应用。

N/O糖基化
糖基化修饰
糖基化是非模板合成过程,单糖及其衍生物通过糖苷键相互连接成糖链,再由酶催化与蛋白质或酯类等非糖物质的特定部位共价结合形成糖复合物(糖蛋白、蛋白聚糖和糖脂等)。根据糖链与蛋白连接方式的不同,糖基化可分为N-糖基化和O-糖基化,前者是糖链与蛋白Asn-X-Ser/Thr 序列子(X为除脯氨酸以外的氨基酸)中Asn残基上的-NH2相连,而后者则是糖链与蛋白Ser/Thr残基上的-OH相连。糖链中寡糖残基的种类、个数以及糖苷键的类型/位点构成了糖链长度和构型差异并形成糖链的多样性。
糖基化修饰的作用
糖基化修饰是一个复杂多样的修饰,通过对不同蛋白、不同位点进行修饰,糖链结构的不同,发生糖基化的蛋白能发挥的功能也就不同。
首先通过对蛋白进行复杂糖基化修饰,蛋白质类型得到了极大的丰富,功能应用得到了极大拓展。其次糖基化修饰在机体发育、炎症、肿瘤等多种生理病理过程中发挥重要作用,包括免疫监视、细胞粘附、细胞-基质相互作用,细胞内信号转导,细胞代谢等进程。同时目前已经在肝癌、大肠癌、胰腺癌等多种癌症和类风湿性关节炎等AID的多种疾病中均发现异常糖基化形式的存在,为临床开发包括肿瘤在内的多种疾病标志物的开发和应用提供了重要方向。

应用方向
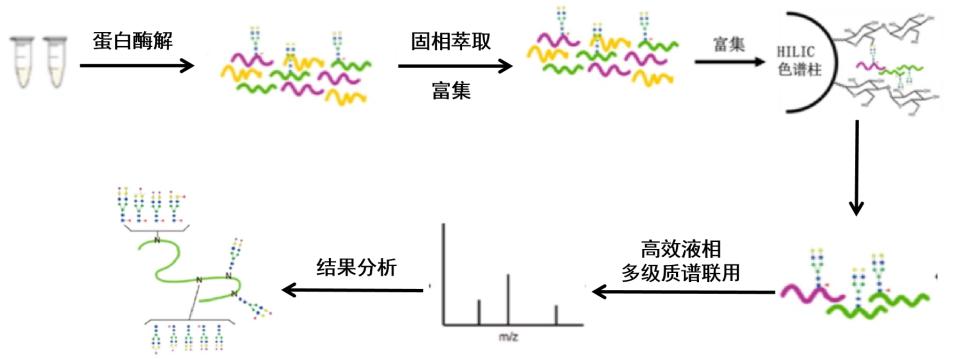
富集方式
产品优势
1.使用HILIC富集,富集特异性中等,富集得到的糖肽数量最多,重复性最好,易于与MS联用
2.使用pGlyco软件搜库,无需区分糖库与普通库,修饰位点可直接在库中确认,省时省力
3.生信分析深度挖掘:针对糖基化特性进行糖型信息分析,深度挖掘糖基化特性。
乙酰化蛋白质组
蛋白质乙酰化(acetylation)是指在乙酰基转移酶(HATs/KATs)的催化下把乙酰基团(如乙酰辅酶A等供
体)共价结合到底物蛋白质的赖氨酸残基上的过程,主要发生在蛋白质赖氨酸残基的ε-NH2位。蛋白质去乙酰
化是在去乙酰化酶(HDACs/KDACs)作用下的可逆性修饰过程。蛋白质乙酰化修饰由乙酰基转移酶和去乙酰化酶共同调节。
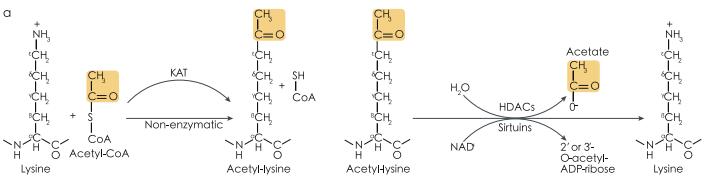
乙酰化可影响到生命活动的各个过程,包括:基因转录调控,DNA复制、损伤修复,RNA稳定性,蛋白合成、折叠、聚集,细胞周期、分裂、凋亡、自噬,细胞骨架重排,新陈代谢,脂质储存和分解,线粒体裂变,信号转导,离子转运,氧化还原调节等。在动植物的免疫应答,抗逆抗胁迫,生长发育,代谢和衰老过程,肿瘤发生发展,神经退行性疾病等方面都有广泛应用。

琥珀酰化蛋白质组
蛋白质琥珀酰化(succinylation)修饰是指琥珀酰基团供体(如琥珀酰辅酶A)通过酶学或者非酶学的方式将琥珀酰基团共价结合到底物蛋白质的赖氨酸残基的过程。
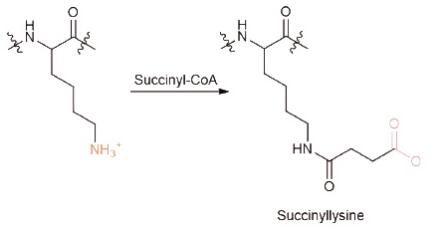
琥珀酰化修饰赋予赖氨酸基团2个负电荷,能够引发更多蛋白质特性的改变,且琥珀酰基团空间结构较大,对于蛋白质结构和功能的影响更为显著。在真核和原核生物中,琥珀酰化是一种保守的修饰类型。琥珀酰化和乙酰化具有非常强的相关性,在已有的研究中,大量发生琥珀酰化的位点同时也能检测到乙酰化修饰。琥珀酰化参与了很多核心能量代谢途径(包括三羧酸循环、糖代谢等),影响线粒体中的代谢过程,对线粒体失调相关的疾病的研究具有重要价值。

丙酰化蛋白质组
蛋白质丙酰化(Propionylation)修饰是指在酰基转移酶(如乙酰基转移酶)的作用下催化丙酰基团(如丙
酰辅酶A等供体)共价结合到底物蛋白质中赖氨酸残基上的过程。
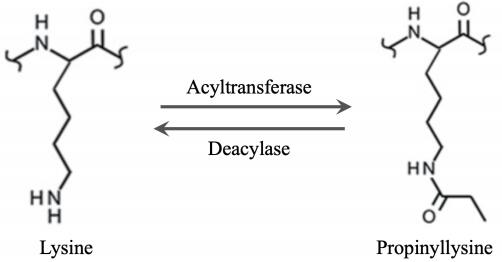
赖氨酸丙酰化在真核生物和原核生物中均起重要的调控作用,作为一种新发现的可逆修饰,其功能仍有待深入研究,具有很大的研究潜力。已有研究发现丙酰化在细菌的整体代谢调控网络和代谢酶的活性调控,细菌和哺乳动物的细胞应激反应,真核生物和原核生物的表观遗传调控,光合作用调控等方面有重要作用。
戊二酰化蛋白质组
蛋白质戊二酰化(glutarylation)是指在酶的催化下把戊二酰基团(如戊二酰辅酶A等供体)共价结合到底物蛋白质的赖氨酸残基上的过程,此过程是可逆的。赖氨酸本身带有正电荷,戊二酰化发生后,将正电荷改变成负电荷,这种对蛋白带电性的改变会影响蛋白构象和蛋白间相互作用。
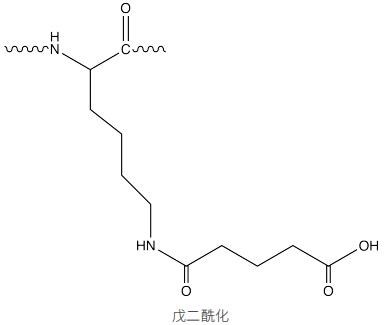
戊二酰化作为近些年新发现的酰化修饰类型,对核小体组装、染色质结构、基因表达、DNA损伤修复、细胞周期有重要调控作用,和其他酰化修饰类似,在代谢过程中也起到重要作用,已有的研究表明,其对核小体动态结构和精子运动都有一定影响。
甲基化蛋白质组
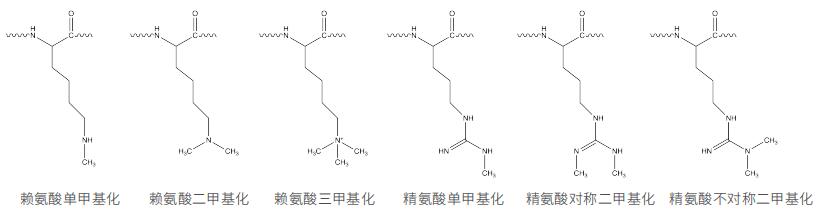
蛋白质甲基化修饰(methylation)最常见的发生位点是赖氨酸和精氨酸。在赖氨酸位点上,赖氨酸甲基转移酶可催化赖氨酸ε-氨基集团发生单甲基化、二甲基化、三甲基化;在精氨酸位点上,精氨酸甲基转移酶可催化精氨酸侧链上发生单甲基化、对称二甲基化、不对称二甲基化。对于甲基化的研究一般需要确定修饰类型或修饰位点,诺禾致源质谱事业部目前可承接赖氨酸泛甲基化和精氨酸单甲基化的修饰类型。
甲基化在基因表达、DNA损伤修复、转录调控、蛋白合成、染色体组装、信号转导方面都有着重要作用,在表观遗传,癌症,老年痴呆、衰老方面得到广泛研究。

乳酸化蛋白质组
蛋白质乳酸化(Lactylation)是一种新发现的蛋白质翻译后修饰形式,指在组蛋白或其他蛋白质的赖氨酸残基上共价添加乳酸基团的化学修饰过程。
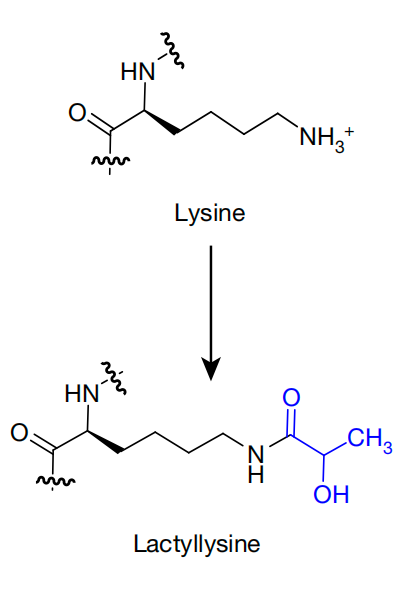
乳酸化修饰由芝加哥大学赵英明团队于2019年首次报道,其发生依赖于细胞内乳酸浓度,直接将代谢产物乳酸与表观遗传调控联系起来。乳酸化修饰通过改变蛋白质结构或功能,参与基因表达调控、免疫应答和肿瘤微环境适应等生理病理过程。
技术路线
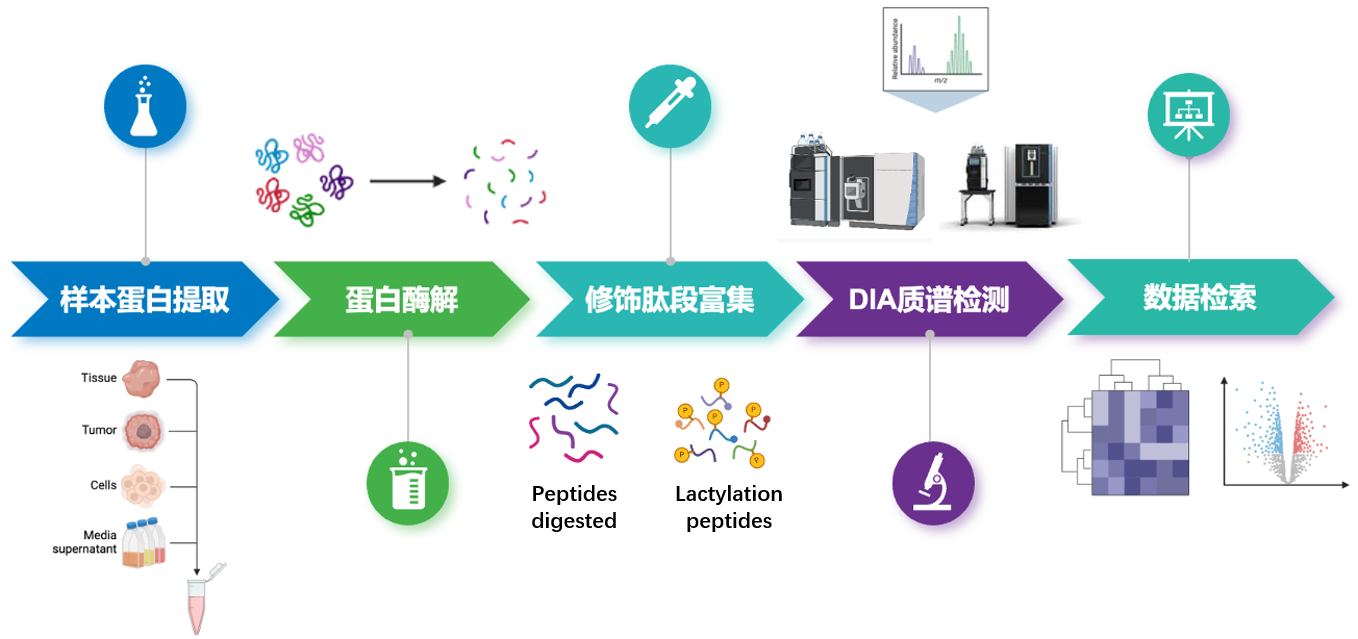
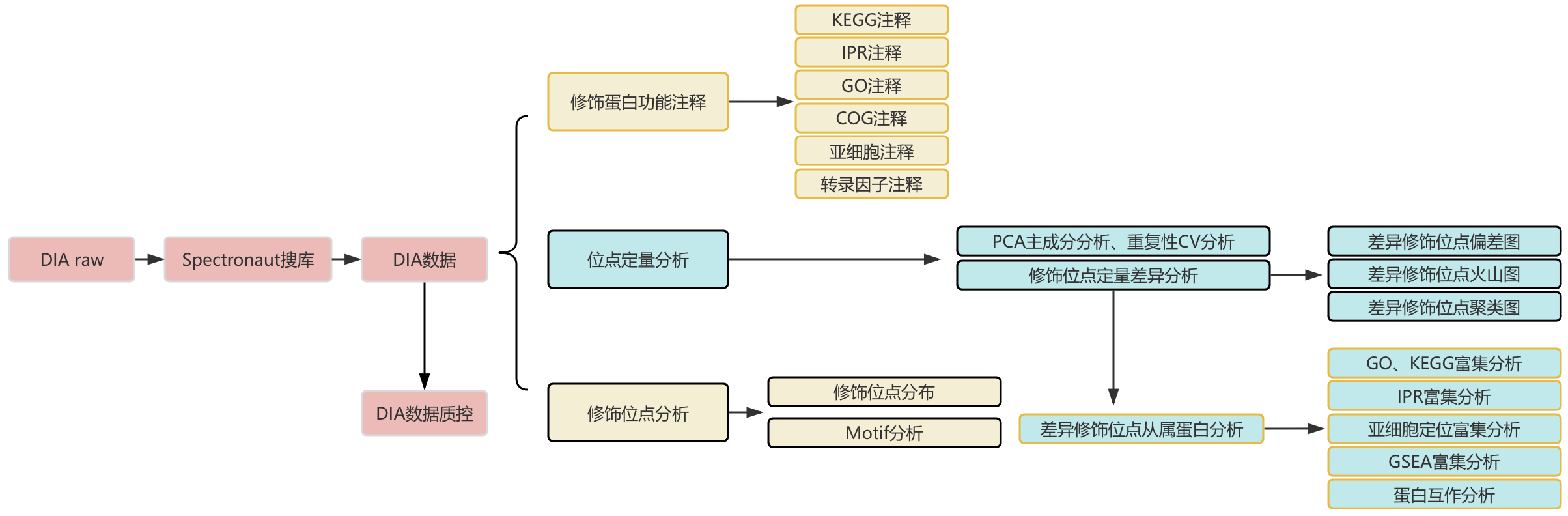
信息分析内容
技术优势
1.鉴定深度突破现有文章报道水平,实现2w+乳酸化肽段的鉴定深度,且一类位点占比超过80%
2.蛋白和位点双维度报告解析
3.实现多组学联合分析
4.打造高性价比产品
应用方向

风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验蛋白质翻译后修饰 (Protein translational modifications,PTMs) 通过功能基团或蛋白质的共价添加、调节亚基的蛋白水解切割或整个蛋白质的降解来增加蛋白质组的功能多样性。这些修饰包括磷酸化、糖基化、泛素化、亚硝基化、甲基化、乙酰化、脂质化和蛋白水解,几乎影响正常细胞生物学和发病机制的所有方面。因此,识别和理解 PTM 在细胞生物学和疾病治疗和预防的研究中至关重要。 看到一篇 Thermo Fisher的文章,关于翻译后修饰Post
【求助】P53的翻译后修饰都有哪些? 怎样验证其修饰后与靶标启动子的结合活性的变化?
xiaozhangwei2 P53的翻译后修饰都有哪些?听说有磷酸化和乙酰化。还有其他的吗? 怎样找出P53是发生了哪种修饰变化? 如何设计实验验证P53修饰后,与靶标启动子结合时,有没有产生结合活性的变化啊? 谢谢! 大鹏鸟 p53的修饰 正常细胞在非应激状态下p53的水平和活性都较低,受到应激作用时,p53通过一系列的翻译后修饰被活化,并能结合特异的DNA序列。翻译后修饰是调节
组织样本进行蛋白质组学分析,对 213 个差异蛋白进行亚细胞定位、COG 和 GO 分析。差异蛋白质中的大多数在翻译后修饰、蛋白质周转、伴侣和氨基酸转运以及代谢中起作用。 代谢组学分析:同时对糖尿病仓鼠的血清进行代谢组学分析,并对差异代谢物进行 KEGG 分析,谷胱甘肽代谢、苯丙氨酸、酪氨酸和色氨酸生物合成以及精氨酸和脯氨酸代谢通路发生显著异常。 组学联合分析:KEGG 关联分析揭示甘氨酸、丝氨酸和苏氨酸代谢途径表现为甘氨酸、高丝氨酸、色氨酸、前列腺素 AM1、磷酸葡萄糖脱氢酶、磷酸丝氨酸转氨酶、CTH
 技术资料
技术资料暂无技术资料 索取技术资料










