万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 提供商:
江苏集萃药康生物科技股份有限公司
- 服务名称:
BALB/cJGpt-Pdcd1em1Cin(hPDCD1)Cd274tm1(hCD274)Tnfrsf9em1Cin(hTNFRSF9)/Gpt
BALB/c-hPD1/hPDL1/hCD137
品系名称:BALB/cJGpt-Pdcd1em1Cin(hPDCD1)Cd274tm1(hCD274)Tnfrsf9em1Cin(hTNFRSF9)/Gpt
品系类型:Knock-in
品系编号:T007056
背景:BALB/cJGpt
品系描述
PDL1是细胞程式死亡配体1(Programmedcell death 1 ligand 1,PDL1),也称为表面抗原分化簇274(clusterof differentiation 274,CD274)或B7同源体1(B7homolog 1,B7H1),由CD274基因编码,是大小为40kDa的一型跨膜蛋白[1]。正常情形下免疫系统会对聚集在淋巴结或脾脏的外来抗原产生反应,促进具有抗原特异性的T细胞增殖。而细胞程式死亡受体1(PD1)与细胞程式死亡配体1(PDL1)结合,可以传导抑制性信号,减少抗原特异性T细胞增殖[2]。
研究表明,肿瘤细胞通过高表达PDL1,与T细胞表面的PD1结合,传递抑制信号,从而逃逸免疫清除,阻断这一通路将解除T细胞抑制,活化T细胞,实现对癌细胞的杀伤[3]。目前针对PD1/PDL1通路的上市药物已达5种,国内针对此通路的抗体药物研发也在如火如荼的进行中。
CD137(4-1BB,TNFRSF9)属肿瘤坏死因子受体超家族成员,I型跨膜蛋白。在活化的CD4+T、CD8+T细胞表面表达,与CD137L结合构成T细胞共刺激信号[4]。CD137主要在T细胞的免疫应答中发挥作用,可以协同CD28在免疫后期提供共刺激信号以及T细胞的存活信号,在维持免疫应答、抵抗免疫细胞凋亡、减少抗原特异性免疫细胞的清除以及增强免疫记忆方面发挥重要作用。
CD137能够刺激NK细胞增殖及IFNγ产生[5],通过促进细胞因子产生及B7上调表达介导DC活化[6];同时,CD137能够保护T细胞免于活化诱导的细胞死亡(activation-inducedcelldeath,AICD)[4]。另外,CD137表达于肿瘤组织血管壁,CD137L表达于多种人体肿瘤组织细胞表面,则CD137/CD137L在肿瘤微环境中发挥重要作用。
BALB/c是广泛应用于免疫学、肿瘤学等研究的近交系小鼠,来源于BALB/c背景的同源肿瘤细胞系众多,如结肠癌细胞CT26,乳腺癌细胞4T1,肝癌细胞H22及B淋巴癌细胞A20等。
应用领域
-
人CD137激动剂药效评价或人PD1/PDL1抑制剂药效评价。
-
人CD137激动剂及人PD1/PDL1抑制剂联合用药药效。
-
人CD137激动剂及人PD1/PDL1抑制剂毒理学评价。
-
抗肿瘤研究。
验证数据
-
蛋白表达检测

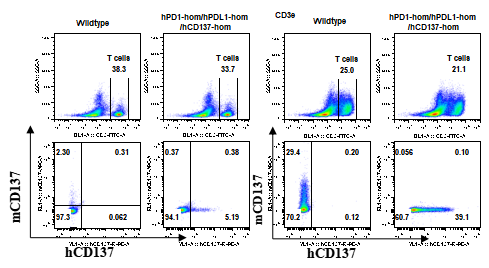
图1BALB/c-hPD1/hPDL1/hCD137小鼠蛋白表达检测
未刺激的条件下,BALB/c-hPD1/hPDL1/hCD137纯合小鼠能够表达人源PD1蛋白;CD3抗体刺激后,在BALB/c-hPD1/hPDL1/hCD137纯合小鼠脾脏中检测到hPDL1和hCD137的蛋白表达。
-
T/B/NK细胞比例检测
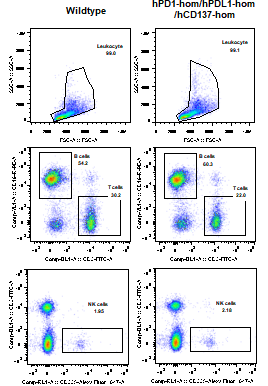
图2BALB/c-hPD1/hPDL1/hCD137小鼠T/B/NK细胞比例检测。
野生型小鼠与BALB/c-hPD1/hPDL1/hCD137纯合子小鼠在外周血及脾脏中的T/B/NK细胞比例接近。
-
体内药效实验

图3BALB/c-hPD1/hPDL1/hCD137的体内药效试验(Urelumabanalogue)
基于BALB/c-hPD1/hPDL1/hCD137小鼠药效实验。对数生长期的结肠癌细胞CT26-hPDL1-mPDL1(KO)皮下接种至BALB/c-hPD1/hPDL1/hCD137小鼠。待肿瘤平均体积生长至80-120mm3时,随机分为PBS组,Keytruda单药组、Urelumabanalogue单药组、Urelumabanalogue与Keytruda联合给药组(n=8),每周给药2次,共给药6次。数据以Mean± SEM形式呈现。
结果显示:Keytruda治疗组和Urelumabanalogue治疗组,其肿瘤体积的抑制率(TGI)分别为69.68%、72.21%,显示对肿瘤的生长有一定的抑制作用;联合用药组Keytruda+Urelumab analogue联合给药组显示出更为显著的肿瘤抑制作用,TGI为87.22%。
结果证明:BALB/c-hPD1/hPDL1/hCD137小鼠是筛选和评价人源CD137、PD1抗体及联合用药的理想动物模型。
参考文献
-
Flemming, A. "Cancer: Pd1 Makes Waves in Anticancer Immunotherapy."Nat Rev Drug Discov 11 8 (2012): 601.
-
Migden, M. R., et al. "Pd-1 Blockade with Cemiplimab in Advanced Cutaneous Squamous-Cell Carcinoma." N Engl J Med 379 4 (2018): 341-51.
-
Zhou, Q., et al. "Coexpression of Tim-3 and Pd-1 Identifies a Cd8+ T-Cell Exhaustion Phenotype in Mice with Disseminated Acute Myelogenous Leukemia." Blood117 17 (2011): 4501-10.
-
Cannons JL, et al. 4-1BB ligand induces cell division, sustains survival, and enhances effector function of CD4 and CD8 T cells with similar efficacy. J. Immunol. 2001; 167:1313–1324. [PubMed: 11466348]
-
Wilcox RA, Tamada K, Strome SE, Chen L. Signaling through NK cell-associated CD137 promotes both helper function for CD8+ cytolytic T cells and responsiveness to IL-2 but not cytolytic activity. J. Immunol. 2002; 169:4230–4236. [PubMed: 12370353]
-
Wilcox RA, et al. Cutting edge: expression of functional CD137 receptor by dendritic cells. J. Immunol. 2002; 168:4262–4267. [PubMed: 11970964]
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验(+/-)以及 1/4 同窝野生型对照小鼠(WT)。繁育流程如下图所示:该路径同样也适用于基因敲入(KI)小鼠。需要指出的是,对于利用 CRISPR/Cas9 介导的 NHEJ 途径获得的 KO 小鼠,情况有所不同,方案类似于转基因小鼠的繁育。由于 NHEJ DNA 修复的结果是随机发生的,所以每一只 KO Founder 小鼠、甚至一只 Founder 中每个细胞的基因型都可能是不同的。因此,KO Founder 要与野生型小鼠(比如:C57BL/6J)交配,获得基因型明确的 F1 子代 KO 杂合子(+/-)小鼠
9 系统,在受精卵的目标基因的编码区两侧分别切断,然后受精卵在连接断口的过程中,会丢失掉断口之间的序列(即编码区)。该受精卵移植到受体母鼠输卵管内,发育成为小鼠个体,该小鼠将无法表达目标基因,导致目标基因将完全失去活性,表现为全身性基因敲除。 (3)基因敲入(KI)首先构建打靶载体:包含同源臂和外源基因,然后将表达载体通过显微注射的方法注入到受精卵的细胞核内,同时利用 Crispr/Cas9 系统,在受精卵目的基因位置切断基因组 DNA,受精卵会通过同源重组将外源基因定点整合到基因组内。该受精卵移植
随着生命科学技术的不断发展,各种小鼠模型(转基因、基因敲除、基因敲入、人源化等)被广泛的开发和应用,如江苏集萃药康生物科技股份有限公司目前拥有自主品系数量已高达 22000+,覆盖代谢、免疫、肿瘤、神经、发育等领域,保存这些模型需要大量的人力、财力和空间,而冷冻保存技术的出现,给科研学者提供了安全和经济保存种群资源的方法。此外精子冷冻在动物育种上可加速遗传改良,保存珍稀物种品系,防止遗传漂变,节省饲养空间等诸多优点,本文将简要介绍小鼠精子冷冻技术发展重要的几个历程。 第一道困境 也是故事
 技术资料
技术资料暂无技术资料 索取技术资料










