全球首例 | 安徽医科大学实现猪-人活体肝移植,基因编辑供肝存活 171 天
2025-10-24 18:00点击次数:62
关键词:全球器官短缺危机持续加剧,世界卫生组织数据显示每年数万患者在等待移植期间死亡。异种移植作为潜在解决方案,近年来在心脏与肾脏领域取得突破 —— 美国 FDA 已批准基因编辑猪器官的临床试验。肝脏因其复杂的代谢与免疫调节功能,成为异种移植的最后堡垒。2024 年,中美团队先后在脑死亡受体中实现猪肝体外灌注(3 天)及异种移植(10 天),但活体移植始终未能突破。
2025 年 10 月 8 日,安徽医科大学第一附属医院孙倍成、魏宏江团队在肝病学顶刊 Journal of Hepatology (IF: 25.7)发表题为「Genetically engineered pig-to-human liver xenotransplantation」的里程碑研究。团队通过 CRISPR-Cas9 技术构建 10 基因修饰猪模型,成功将 514 g 猪肝移植至 71 岁肝癌合并肝衰竭患者体内,实现三大突破:
全球首例活体功能性存活:移植物持续分泌胆汁(峰值 400 ml/d)并合成凝血因子
排斥控制:基因编辑有效规避超急性排斥反应
生存纪录:患者总生存期达 171 天,显著超越既往记录
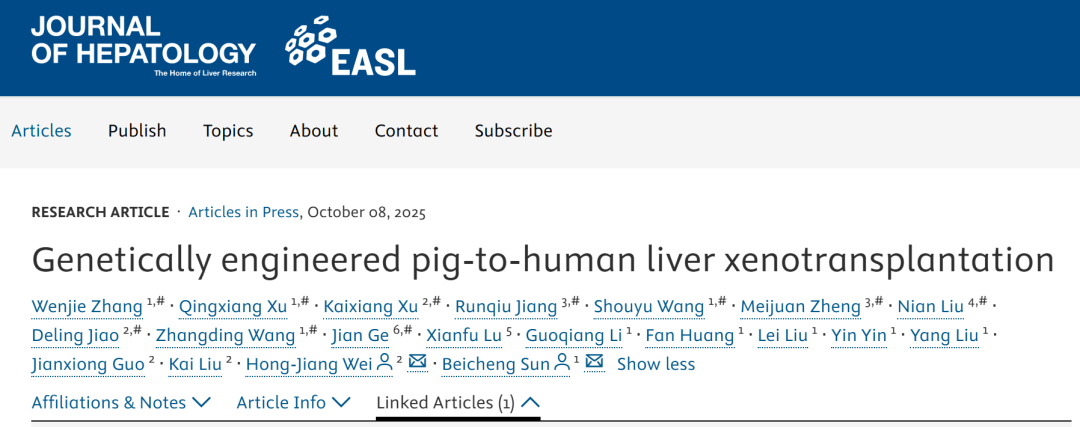
手术方案与早期响应
患者因乙肝肝硬化合并巨块型肝癌(肿瘤直径 >15 cm,AFP>100,000 ng/mL),残肝体积仅 41.79%,无法耐受肝切除或常规肝移植。
经多学科团队评估并获伦理批准,实施急诊肿瘤切除+辅助性异种肝移植:
供肝:10 基因编辑猪肝(514 g),异位植入右肝窝并行胆管外引流(图 1C)
术后响应:移植物即刻分泌胆汁,第 16 天达峰值 400 ml/d(图 1F, 图 2),肝肾功能指标趋稳
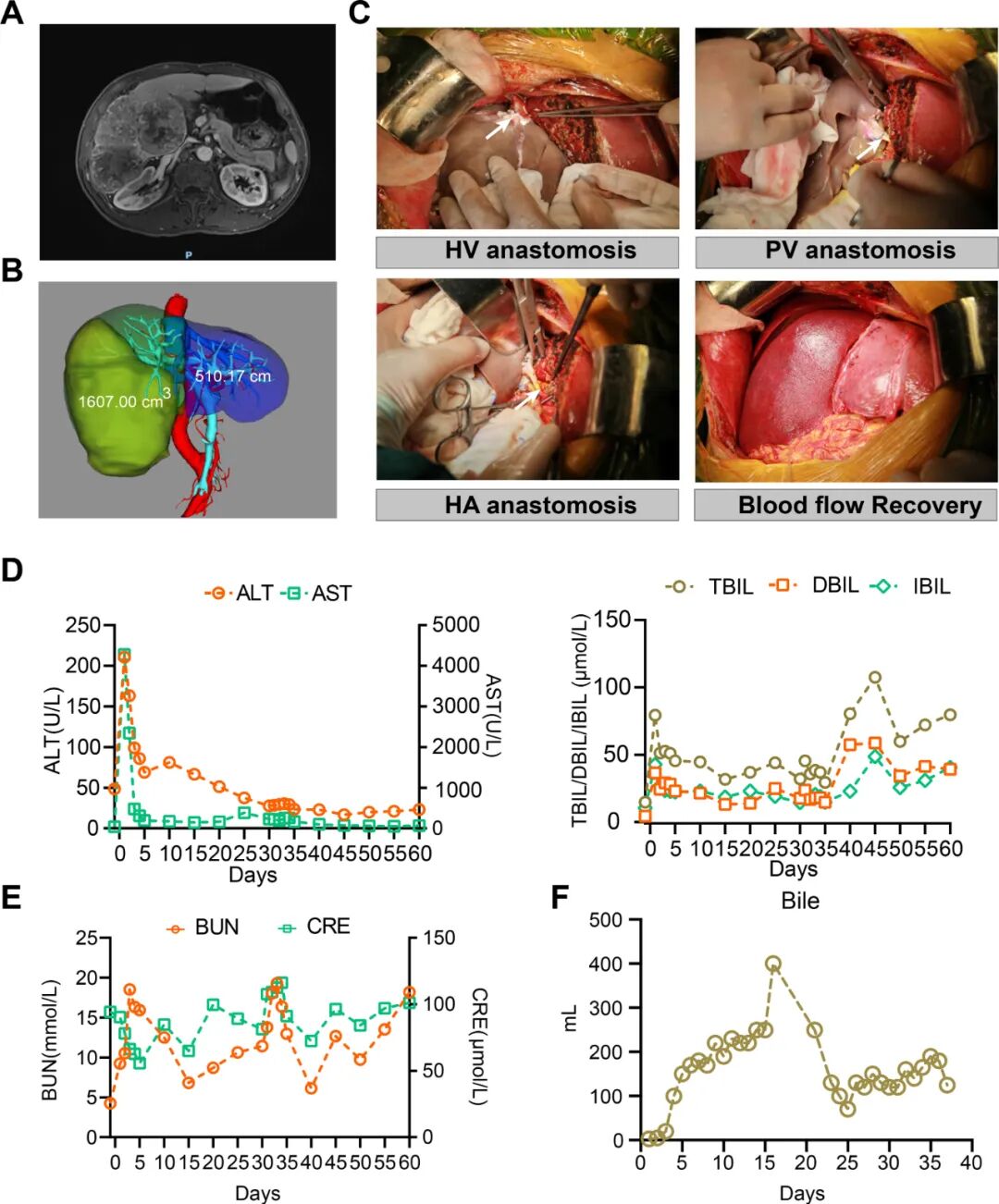
图:围手术期信息
为评估移植猪肝的代谢功能,研究者系统监测了术后 45 天内患者胆汁酸谱及白蛋白动态。数据显示:
猪源性胆汁酸(HCA、GHCA 等)术后第 1 天即显著升高,第 3 天达峰值 7004 nM,反映移植物早期代谢活性。虽在第 5 天降至 3452 nM,但经巴利昔单抗干预后第 9 天恢复至 13309 nM。第 19-21 天出现短暂下降(最低 2893 nM),干预后第 31 天复升至 10013 nM。
人源性胆汁酸呈同步波动趋势:血清糖胆酸(GCA)第 9 天达 5087 nM,第 21 天降至 1755 nM 后逐渐恢复。
胆汁酸比例变化:术后第 1 天猪/人初级胆汁酸比值从 0.014 骤增至 1.811,证实移植物有效代偿肝功能。
白蛋白分析:术后第 1 天即检测到猪白蛋白,且猪/人白蛋白比值较胆汁酸更稳定(图 3D-E),提示其作为肝功能指标的可靠性。
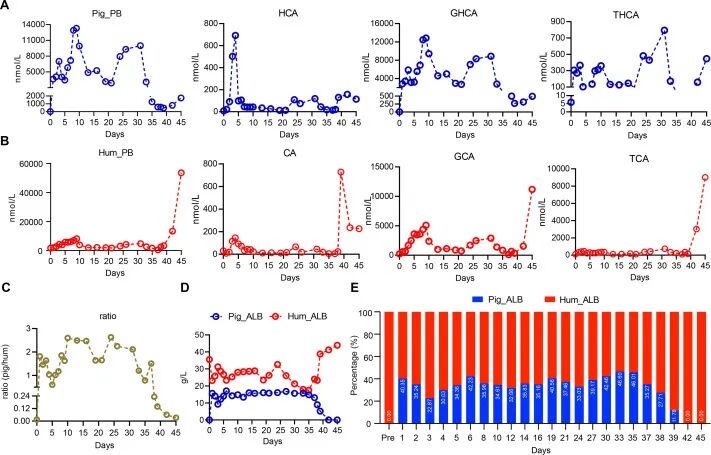
图:异种移植患者的胆汁酸和白蛋白测量值
移植肝功能评估显示,猪源性凝血因子在术后第 1 天即呈现高表达状态,其中凝血因子 VIII(FVIII)血浆浓度达 350,972 pg/mL,经巴利昔单抗干预后第 27 天维持在 323,957 pg/mL。值得注意的是,猪 FVIII 峰浓度超人源基准达 340 倍,显著破坏凝血稳态。
凝血系统呈现多重紊乱:凝血酶原时间(PT)与活化部分凝血活酶时间(APTT)显著缩短,纤维蛋白(原)降解产物(FDP)和 D-二聚体持续升高,血小板计数 24 小时内锐减。伴随持续高凝状态,CT 影像发现辅助肝肝静脉末端结节性血栓,虽经依诺肝素抗凝治疗未进展。
上述证据表明,猪源性凝血因子的超高表达引发跨物种凝血失衡,构成异种肝移植的核心管理挑战。
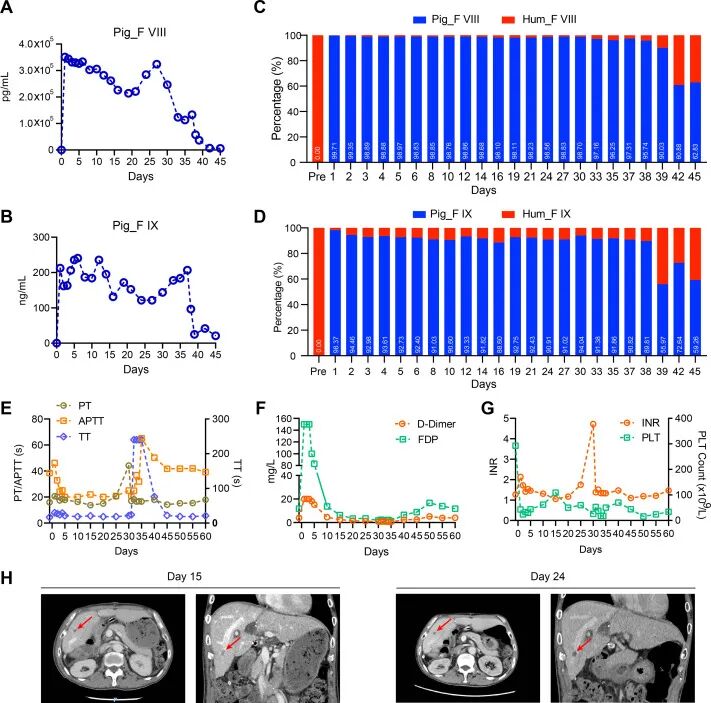
图:凝血系统与血栓的形成
移植后第 10 天,对辅助异种猪肝进行活检。病理评估显示,移植肝门脉区仅见稀疏淋巴细胞浸润(RAI 持续为 1),免疫荧光检测提示中度 IgM 沉积伴弱 C4d 阳性,补体成分(C1q/C3c/C4c/C5b)呈轻度沉积,证实基因编辑有效控制排斥反应。
影像学动态监测发现:自体左肝体积由 510.17 cm³ 增至 610.6 cm³(增长 19.7%),而辅助猪肝体积术后早期扩张至 1286.92 cm³ 后回缩至 995.9 cm³,且血流灌注正常,印证双肝功能性共存。
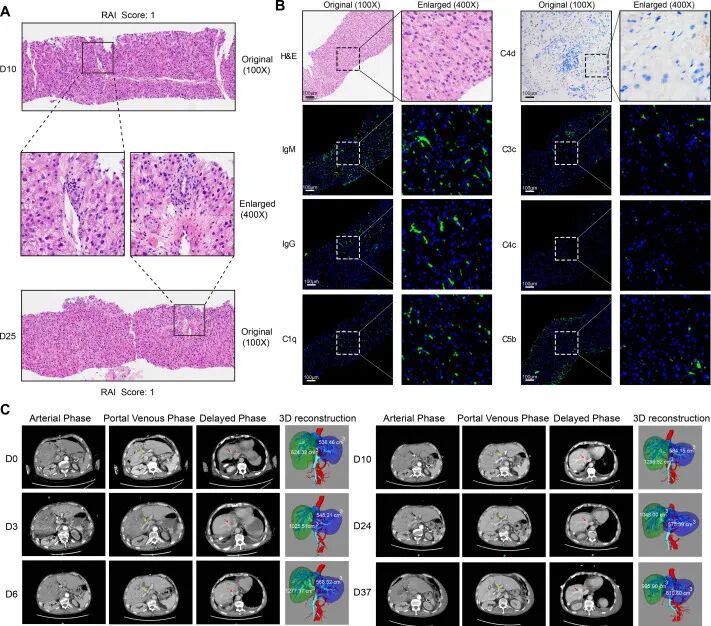
图 : 超急性或急性排斥反应,伴有左肝再生
术后第 25 天患者出现心肌损伤征象,肌钙蛋白水平 8 天内由 0.0679 ng/ml 急剧升至 0.9496 ng/ml,心脏 MR 显示急性炎症改变。至第 31 天病情恶化:血小板骤降至 17×10⁹/L,血红蛋白 <90 g/L,裂红细胞比例达 4.0%,伴持续蛋白尿及 LDH 升高。
实验室确诊异种移植相关血栓性微血管病(xTMA):
终末补体复合物 sC5b-9 = 353 ng/ml
血清补体活性 CH50 峰值 1514 U/ml
补体旁路途径激活(Bb/C4b↑)
治疗立即调整免疫抑制方案(停用西罗莫司/他克莫司,换用巴利昔单抗),并予依库珠单抗(900 mg×2 次)抑制膜攻击复合物。但干预无效:血小板持续下降(11×10⁹/L),乳酸升高伴意识障碍,多器官功能进行性衰竭。鉴于持续补体激活及左肝代偿性增生(体积增加 19.7%),团队于第 38 天行急诊移植物切除。
术后病理证实 xTMA 特征:
微血管广泛纤维蛋白血栓
补体沉积显著增加(C5b↑/C4d↑)
血管性血友病因子(vWF)强表达伴免疫浸润
移植物移除后 sC5b-9 迅速复常,猪源凝血因子消失,AFP 降至 19.88 ng/ml,证实自体肝功能恢复。
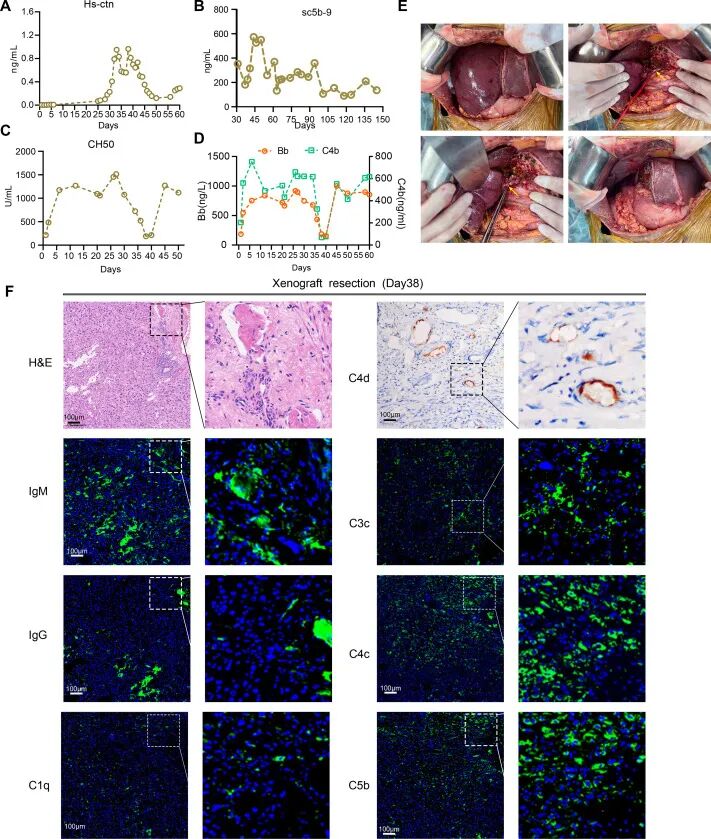
图 : xTMA 和异种移植物切除的证据
术后第 135 天,患者出现上消化道突然出血,保守措施无效后需紧急内镜下止血。再出血发生在第 138 天和第 148 天,每次都需要重复内镜止血。
术后第 142 天,数字减影血管造影(DSA)勾勒出两条从脾静脉干产生的胃底静脉曲张支流,在眼底形成一个大的、连通的静脉曲张丛(PTVE 前,左侧和中部)。然后对胃底静脉曲张进行经皮经肝静脉曲张栓塞术(PTVE)。脾静脉干完成血管造影(PTVE 术后,右)显示完全闭塞,宫底静脉曲张丛无混浊。
尽管采取了这些干预措施,但随后还是反复出血,患者在术后第 171 天死亡。
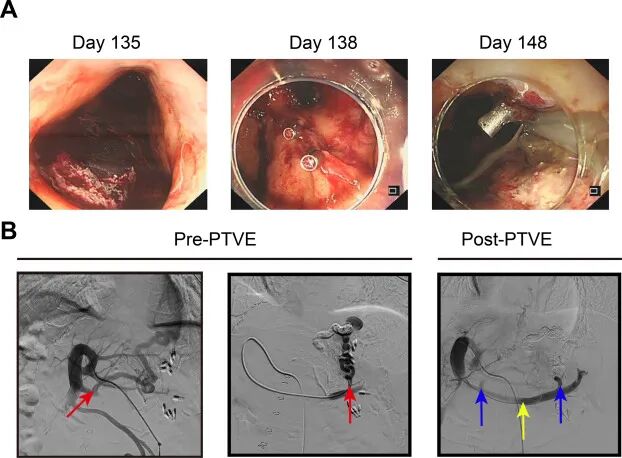
图 : 复发性上消化道出血和静脉曲张处理
本研究首次实现活体基因编辑猪肝移植,成功规避超急性排斥反应并维持 31 天功能存活,但 xTMA 的难治性揭示需基因层面优化。此突破跨越了异种移植从脑死亡模型到活体应用的鸿沟(生存期 171 天),锁定凝血-补体轴为长期存活关键靶点。
来源:丁香通研选
我们长期为科研用户提供前沿资讯、实验方法、选品推荐等服务,并且组建了 70 多个不同领域的专业交流群,覆盖 CAR-T 工艺、肿瘤免疫、基因编辑、外泌体、类器官等领域,定期分享实验干货、文献解读等活动。




