局灶性节段性肾小球硬化和肾脏病学的未来
2019-08-16 16:04点击次数:288
关键词:一篇关于局灶性节段性肾小球硬化(一种进展性肾病)的新文章今天发表在BMC医学杂志上。我们采访了该领域的专家、芝加哥拉什大学的医学主席Jochen Reiser,以了解更多关于FSGS的信息,以及这些最新的结果对我们的理解有何帮助。
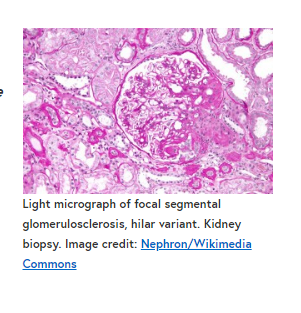
一篇关于局灶性节段性肾小球硬化(一种进展性肾病)的新文章今天发表在BMC医学杂志上。我们采访了该领域的专家、芝加哥拉什大学的医学主席Jochen Reiser,以了解更多关于FSGS的信息,以及这些最新的结果对我们的理解有何帮助。
原发性局灶性节段性肾小球硬化(FSGS)到底是什么?
FSGS是一种进展性肾脏瘢痕性疾病。其发展的原因可能有几个,并从内部或外部的肾脏。30%或更多的肾移植后FSGS会复发。由于FSGS疾病的迅速复发,科学家和临床医生怀疑受体血液中存在一种所谓的“循环因子”,这种因子会损害新肾脏。
FSGS早期损伤的主要靶细胞是足细胞。足细胞是肾脏滤过屏障的中心部分,如果它们不能正常工作,就会失去它们典型的“章鱼状”结构,让血浆蛋白从血液进入尿液(蛋白尿)。
蛋白尿的临床后果是多方面的,包括心血管疾病的高风险,以及进行性肾脏疾病,最终导致肾功能丧失,需要透析或肾移植。
suPAR作为FSGS标记的历史背景是什么?当前这项工作的相关性是什么?
我的实验室多年来一直在研究足细胞的行为。我们发现它们是动态的而不是静态的细胞。控制它们的过程动态的程序是通过整合素来调节的,整合素是细胞基质的锚,可以是活动的,也可以是非活动的。
整合素可以与尿激酶受体结合,并与整合素在同一细胞中表达,也可以从血液中到达足细胞,其可溶性形式称为suPAR。
描述尿激酶受体(uPAR)与整合素相互作用的最初论文来自加州大学旧金山分校的哈罗德•查普曼(Harold Chapman)团队,并于1996年发表在《科学》(Science)杂志上。后来,我们发现足细胞中的uPAR与整合素有关。
在本实验室进行后续研究,确定苏帕尔为FSGS的循环因子。它结合并激活足细胞alphavbeta3整合素受体,从而导致足细胞运动障碍和早期FSGS。
还需要做哪些进一步的研究?
我们在FSGS患者的血液中发现了高水平的suPAR。考虑到suPAR在其他一些情况下也会升高,例如炎症和某些癌症,很明显,商业化的ELISA(一种检测方法)并不适合在不同人群中进行单一或筛选测试。
对于肾功能正常或轻度下降的患者,以及那些已经被诊断为FSGS的患者,该检测是有帮助的。在大多数但不是所有的研究中,血液中的suPAR与肾功能有关,但目前的ELISA不能区分晚期肾衰竭中FSGS的单纯积累和病理产生。
造成这种困境的原因还在于,ELISA能够识别糖基化苏帕尔,但不能识别(或差)糖基化程度较低且/或以片段形式出现的苏帕尔。
我们现在还知道不同的suPAR类型对整合素有不同的影响。我们可以用新的细胞模型来测试这一点,希望不久就可以用一种针对FSGS的特殊的suPAR ELISA来测试。这些详细研究的一部分将很快发表。
黄等人在BMC医学上的论文有什么新发现?
本文介绍了目前在尿液中使用的ELISA方法,结果令人震惊。分析了64例肾小球疾病患者的尿suPAR水平。大部分FSGS患者的suPAR升高,提示FSGS与肾功能无关。

我怀疑FSGS中suPAR-type的生化特性是这样的,它们要么允许优先的suPAR排泄,要么缺乏再吸收。它真正建立了这样一种理念,即FSGS中的suPAR不仅是提升的,而且是不同的。因此,它不同于其他疾病,可以出现高suPAR和没有相关的肾脏疾病。
本文的研究结果表明,我们可以利用尿液作为肾脏排出毒性最大的suPAR的方法来使用目前的ELISA方法。此外,作者还发现FSGS尿液中的suPAR可以激活足细胞整合素,这表明所测到的suPAR与疾病的病因有关。
这项工作将如何影响临床实践?
首先,它将刺激更多的研究,并允许生物标志物与病理学的结合,这是一个非常需要的肾病学的新方向。
第二,一种移除所有suPAR形式的设备正在临床开发中,计划在2015年底进行测试。对于复发性FSGS患者,对suPAR的特异性切除将对suPAR是肾脏疾病的原因还是后果给出最明确的答案。
第三,肾病研究是一个非常保守的领域。多样化的想法,发展和接受新概念并不总是那么容易。我很高兴地看到,suPAR和FSGS现在是自己的领域,有近50份出版物。只有通过他人的共同努力,我们才能实现新的目标,发展更好的治疗方法。
20年后肾脏学会是什么样子?
这是一个很难回答的问题。病理学、分子途径和遗传学将结合在一起,产生高度特异性和针对性的治疗。我们可能会谈到类似于' FSGS活组织检查,在1型糖尿病患者中,阿波罗1阴性,苏巴尔阳性,NPHS2隐性突变。那时的治疗将包含多种成分,而且可能比现在更有效。



