更多资讯
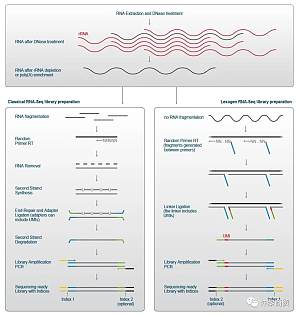
NGS已成为生命科学领域中基因组学和转录组学研究的金标准。虽然它与桑格测序等方法有某些核心相似之处,但NGS所能实现的绝对的高通量水平使它与其他方法截然不同,并彻底改变了科学家的工作方式。RNA测序(RNA-seq)尤其处于NGS功能应用的前言沿。RNA-seq最简单的形式允许我们在取样时确定样本中的RNAs的丰度。转录组是一个高度动态的细胞特征,并打开了一个巨大发掘潜力的世界。对药物、各种疾病状态、转录后修饰 ...
一、目的研究基因的表达和调控时,需要从组织或细胞中分离纯化 RNA。RNA 质量的高低经常影响 RT-PCR、cDNA 库构建和 Northern Blot 等分子生物学实验的成败。 二、主要试剂Trizol 是一种新型总 RNA 抽提试剂,内含异硫氰酸胍等物质,能迅速破碎细胞,抑制细胞释放出的核酸酶。 1. Trizol 试剂含有苯酚,具有毒性和刺激性,注重操作。 2. RNase 污染的主要来源是操作过程中手和空气中的浮沉,注重配带手套,样品尽可能盖严。 3. 细胞裂解必需充分且操作迅速。裂解不完全会降低最后得率,因为一部分 RNA 会残留在未裂解的细胞中。细胞裂解之后要看不见颗粒状物质(结缔组织和骨除外)。在清洗和裂解细胞时最好在低温下操作,防止在操作过程中释放的内源 RNase 降解了 RNA。 4. 酵母和一些细菌由于细胞壁的特别结构,可以加入 Trizol 试剂同时加入无 RNase 的玻璃珠并剧烈振荡,使细胞裂解充分。2-8℃ 避光保存一年。 三、预备工作RNA酶(Rnase)是导致 RNA 降解最主要的物质。此酶非常稳定,在一些极端的条件下只可暂时失活,但限制因素去除
RNA的提取准备试剂:氯仿,异丙醇,75%乙醇,无RNase的水或0.5%SDS(溶液均需用DEPC处理过的水配制) 操作步骤: 1. 匀浆处理: ① 组织 将组织在液氮中磨碎,每50-100mg组织加入1ml TRIzol,用匀浆仪进行匀浆处理。样品体积不应超过TRIzol体积10%。 ② 单层培养细胞 直接在培养板中加入TRIzol裂解细胞,每10cm2面积(即3.5cm直径的培养板)加1ml,用移液器吸打几次。TRIzol的用量应根据培养板面积而定,不取决于细胞数。TRIzol加量不足可能导致提取的RNA有DNA污染。 ③ 细胞悬液 离心收集细胞,每5-10×106 动物、植物、酵母细胞或1×107细菌细胞加入1ml TRIzol,反复吸打。加TRIzol之前不要洗涤细胞以免mRNA降解。一些酵母和细菌细胞需用匀浆仪处理。 2. 将匀浆样品在室温(15-30℃)放置5分钟,使核酸蛋白复合物完全分离。 3. 可选步骤:如样品中含有较多蛋白质,脂肪,多糖或胞外物质(肌肉,植物结节部分等)可于2-8℃10000×g离心10分钟,取上清。离心得到的沉淀中包括细胞外膜,多糖,高分子量DNA
在收集到生物材料之后,最好能即可进行RNA制备工作。若需暂时储存,则应以液氮将生物材料急速冷冻后,储存于-80℃冷冻柜。在制备RNA时,将储存于冷冻柜的材料取出,立即以加入液氮研磨的方式打破细胞,不可以先行解冻,以避免RNase的作用。1. 提取组织RNA时,每50~100mg组织用1ml Trizol试剂对组织进行裂解:提取细胞RNA时,先离心沉淀细胞,每5~106个细胞加1ml Trizol后,反复用枪吹打或剧烈震荡以裂解细胞;2. 将上述组织或细胞的Trizol裂解液转入EP管中,在试问15~30℃下放置5分钟;3. 在上述EP管中,按照每1ml Trizol后加0.2ml氯仿的量加入氯仿,盖上EP管盖子,在手中用力震荡15秒,在室温下(15~30℃)放置2~3分钟后,12000g(2~8℃)离心15分钟;4. 去上层水相置于新EP管中,按照每1ml Trizol加0.5ml异丙醇的量加入异丙醇,在室温下(15~30℃)放置10分钟后,12000g(2~8℃)离心10分钟;5. 弃上清,按照每1ml Trizol加1ml 75% 乙醇进行洗涤,涡旋混合,7500g(2~8℃)离心
一、引言在许多的细胞生命活动中,例如 DNA 复制、mRNA 转录与修饰以及病毒的感染等都涉及到 DNA 与蛋白质之间的相互作用的问题。重组 DNA 技术的发展,人们已分离到了许多重要的基因。现在的关键问题是需要揭示环境因子及发育信号究竟是如何控制基因的转录活性。为此需要:1. 鉴定分析参与基因表达调控的 DNA 元件。2. 分离并鉴定这些顺式元件特异性结合的蛋白质因子。这些问题的研究都涉及到 DNA 与蛋白质之间的相互作用。研究 DNA-蛋白质相互作用的实验方法主要包括:1. 凝胶阻滞实验。2. DNase1 足迹实验。3. 甲基化干扰实验。4. 体内足迹实验。5. 拉下实验。 二、凝胶阻滞实验1. 概念:凝胶阻滞实验(Gelretardationassay),要叫做 DNA 迁移率变动试验(DNAmobilityshiftassay)或条带阻滞实验(Bandretardationassay)是在八十年代初期出现的用于在体外研究 DNA 与蛋白质相互作用的一种特殊的凝胶电泳技术。2. 原理:在凝胶电泳中,由于电场的作用,裸露的 DNA 分子向正电极移动距离的大小是同其分子量的对数成反
转染的定义是“将具生物功能的核酸转移或运送到细胞内并使核酸在细胞内维持其生物功能”。其中,核酸包括DNA (质粒和线性双链DNA ),反义寡核苷酸及RNAi(RNA interference)。基因转染技术已广泛应用于基因组功能研究(基因表达调控,基因功能,信号转导和药物筛选研究)和基因治疗研究。基因转染需要一定的转染试剂将带有目的基因的载体运送到细胞内。早期的磷酸钙转染法转染效率很低,且对很多细胞株无效,因此不能满足很多科研工作的需要。目前,最常用的转染试剂是阳离子脂质体和阳离子聚合物,它们在克服细胞屏障方面跟病毒有很相象的特征,容易透过细胞膜。其中,阳离子脂质体在体外基因转染中有很高的效率,然而在体内,它迅速被血清清除,在肺组织内累积,诱发强烈的抗炎反应,这将导致高水平的毒性,因此,在很大程度上限制了其应用。由于阳离子脂质体的局限性,阳离子聚合物转染试剂日益受到重视。转化特指将质粒DNA 或以其为载体构建的重组DNA 导入细菌体内,使之获得新的遗传特性的一种方法。它是微生物遗传、分子遗传、基因工程等研究领域的基本实验技术之一。受体细胞经过一些特殊方法(如:电击法,CaCl2等化学试
Purpose Materials10ml 6% dextran + 7ml citrate/citric acidDextran: T500 --> 6g+100ml PBSCitrate solution: 25g Na Citrate + 8g citric acid + 500 ml PBS 43 ml blood 12 ml RT Histopaque 107718 ml cold H2 O2 ml 10x PBSM199 for HUVECs: 1L powder pocket M199 + 35g NaHCO3 + 25mM Hepes + 5 mM glutamine + 50 ug/ml Gentamycin.1M Hepes: 119.1 g Hepes + 500 ml dH2 O.Media A: 1X HBSS (10X:50ml) + 10 mM Hepes (1M: 5 ml) + 5 mM EDTA (0.5M: 5ml) + 2.5 % FBS (12.5 ml) in 500 ml.Media B: RPMI1640 470 ml + Ge
一、环境和液流的消毒1、准备足量的无菌1×PBS(3L左右)和去离子水(10L左右)。PBS和去离子水可高压灭菌,sheath桶和装DI水的5L小桶依次用75% 医用酒精和无菌去离子水各涮洗三次,然后将无菌PBS和去离子水分别注入相应桶内即可。2、房间在分选前紫外灯照射15-20分钟;用1:50新洁尔灭拖地;用75% 医用酒精擦拭工作台和收集架;用75% 医用酒精喷洒分选细胞收集区和上样区。二、开机和管道的消毒1、将Sheath液换为活性氯浓度为0.5% 的次氯酸钠溶液(不要用75% 的酒精),开机。开机前,先掀起流动室和分选室的罩盖,开启电源,打开计算机并等计算机进入WINDOWS系统后,打开激光电源,运行FACSDiva软件,联机成功后,执行Fluidics startup命令。然后从FACSDiva的sort菜单进入sort setup,选择合适的液流压力(high、 middle、low)。一般来说,100 μm的喷嘴选用Low,而70 μm的喷嘴选用middle。2、打开breakoff window,点击显示窗上的液流开关,检查液流是否正好流入废液槽中间和液流的形态是否正常
1. 原理RT—PCR 是一种将 cDNA 合成与 PCR 技术结合分析基因表达的快速灵敏的方法,主要用于对表达信息进行检测或定量分析, 还可以用来检测基因表达差异而不必构建 cDNA 文库克隆 cDNA。 RT-PCR 的模板可以为总 RNA 或 poly(A) 选择性 RNA 。逆转录反应可以使用逆转录酶,以随机引物、oligo(dT) 或基因特异性的引物(GSP)起始。 在实际应用中,RT—PCR 又常常分为一步法 RT—PCR 和两步法 RT—PCR。2. 特点一步法 RT—PCR 反应更加快速、灵敏,操作简便,污染率低,RNA 二级结构减少,并且因为聚合酶有校正活性,从而降低了 PCR 反应的错配率。而在两步法中,反应的精确度高,人为的误差相对较小,并且由于在第一步中将 RNA 反转录为 cDNA,从而更易于保存。 另外,两步法的整个过程比一步法更节省费用。传统检测方法的样品用量一般在 ug 级,而在 RT—PCR 检测系统中样品用量陡降至 pg 级。这就在很大程度上降低了实验操作的难度,特别是 mRNA 样品制备的过程得以简化。3. 应用对基因转录产物进行定性与定量的检测,
聚合酶链式反应 (Polymerase Chain Reaction,PCR) 可对特定核苷酸片断进行指数级的扩增。在扩增反应结束之后,我们可以通过凝胶电泳的方法对扩增产物进行定性的分析,也可以通过放射性核素掺入标记后的光密度扫描来进行定量的分析。 无论定性还是定量分析,分析的都是 PCR 终产物。但是在许多情况下,我们所感兴趣的是未经 PCR 信号放大之前的起始模板量。例如我们想知道某一转基因动植物转基因的拷贝数或者某一特定基因在特定组织中的表达量。在这种需求下荧光定量 PCR 技术应运而生。 实时荧光定量 PCR 技术(Real-time quantitative Polymerase Chain Reaction 简称 Real Time PCR)是在定性 PCR 技术基础上发展起来的核酸定量技术。 实时荧光定量 PCR 技术于 1996 年由美国 Applied biosystems 公司推出,在 PCR 反应体系中加入荧光基团,利用荧光信号积累实时监测整个 PCR 进程,使每一个循环变得「可见」,最后通过 Ct 值和标准曲线对样品中的 DNA(or cDNA) 的起始浓度进行
由于 Real-time qPCR 的众多优点,现在已经是生命科学领域的一项常规技术。越来越多的研究文章中涉及 RT-PCR 的实验,也基本上被 real-time qPCR 所代替。由于 real-time aPCR 输出的数据不同于常规的 PCR 电泳检测,很多没有做过 real-time qPCR 的研究者常常感到高深莫测,不知从何入手;甚至一些做过次实验的研究者也会对数据处理分析感到迷惑,不知所措。 本文就从 real-time qPCR 的发展史说起,包括 real-time qPCR 的原理,实验设计,实际操作,数据分析,常见问题解答五个方面,手把手教你从各个方面了解 real-time qPCR,彻底的从菜鸟到高手! 一、Real-time qPCR发展史 Real-time qPCR 就是在 PCR 扩增过程中,通过荧光信号,对 PCR 进程进行实时检测。由于在 PCR 扩增的指数时期,模板的 Ct 值和该模板的起始拷贝数存在线性关系,所以成为定量的依据。由于常规的PCR的缺点,real-time qPCR 由于其操作简便,灵敏度高,重复性好等优点发展非常迅速。现在已经
内参就是内部参照,一般是指管家基因编码表达的蛋白,它们在各个组织和细胞中的表达相对恒定,在检测蛋白的表达水平变化时常用它来做参照参。内参则可以校正蛋白质定量、上样过程中存在的误差,保证实验结果的准确性。此外,内参可以作为空白对照,还可以检测蛋白转膜情况是否完全、整个 WB 显色发光体系是否正常。内参抗体种类很多,比如 β-Actin、β-Tubulin、GAPDH 等,下面简单介绍下如何选择内参。 一、目的蛋白分子量选择内参抗体时,应该考虑目的蛋白分子量的大小。通常应该保证目的蛋白与内参蛋白分子量相差 5KDa 以上。比如检测目的蛋白分子量为 45KDa,此时不适宜选择 β-actin(42KDa)作为内参,可以考虑选择 GAPDH(36KDa)作为内参。二、种属不同种属的样本内参蛋白不同。如哺乳动物的组织或者细胞样本,通常选择 β-actin、β-tubulin、GAPDH;植物来源实验样本,则可以选择 Plant actin、Rubisco等。 三、定位不同表达部位内参蛋白不同 四、样品前处理(常常被忽略的内参选择因素)内参的选择还需要考虑实际的实验环境和样品的前处理。在某些特
基因工程的诞生基因工程是分子水平对生物遗传作人为干预,要认识它,我们先从生物工程谈起:生物工程又称生物技术,是一门应用现代生命科学原理和信息及化工等技术,利用活细胞或其产生的酶来对廉价原材料进行不同程度的加工,提供大量有用产品的综合性工程技术。生物工程的基础是现代生命科学、技术科学和信息科学。生物工程的主要产品是为社会提供大量优质发酵产品,例如生化药物、化工原料、能源、生物防治剂以及食品和饮料,还可以为人类提供治理环境、提取金属、临床诊断、基因治疗和改良农作物品种等社会服务。 生物工程主要有基因工程、细胞工程、酶工程、蛋白质工程和微生物工程等 5 个部分。其中基因工程就是人们对生物基因进行改造,利用生物生产人们想要的特殊产品。随着 DNA 的内部结构和遗传机制的秘密一点一点呈现在人们眼前,特别是当人们了解到遗传密码是由信使 RNA 转录表达的以后,生物学家不再仅仅满足于探索、提示生物遗传的秘密,而是开始跃跃欲试,设想在分子的水平上去干预生物的遗传特性。如果将一种生物的 DNA 中的某个遗传密码片断连接到另外一种生物的 DNA 链上去,将 DNA 重新组织一下,不就可以按照人类的愿望,设
随着人类基因组计划取得巨大的成功和许多物种基因组测序的完成,仅仅靠基因组的序列来试图阐明生命现象是远远不够的,因此,研究重心已经开始从揭示生命的所有遗传信息转移到在分子整体水平对功能的研究上,生命科学已实质性地跨入了后基因组时代。尽管现在已经有多个物种的基因组被测序,但这些基因组中通常有一半以上基因的功能是未知的。目前功能基因组研究中所采用的策略,如微阵列法(microarray)(Wodicka et al.,1997)、基因芯片(gene chips)(Ramsay et al.,1998)、基因表达序列分析(SAGE)(Velculescu et al.,1995)等,都是从细胞中mRNA的角度来考虑的。但事实上,从DNA、mRNA到蛋白质存在三个层次的调控,mRNA自身也存在着贮存、转运和降解等问题,从mRNA角度考虑,实际上仅包括了转录水平调控,并不能全面代表蛋白质表达水平。实验也证明,组织中mRNA丰度与蛋白质丰度的相关性并不好,尤其对于低丰度蛋白质来说,相关性更差。蛋白质复杂的翻译后修饰,蛋白质的亚细胞定位或迁移,蛋白质-蛋白质相互作用则几乎无法从mRNA水平来判断(曾嵘
多元PCR(多重PCR,Multiplex PCR,MPCR) 是指在一个 PCR 反应中使用一个模板和几对引物同时扩增多个目的片段的 PCR 反应。这项技术非常有用,他不仅可以提高 PCR 的产率还能提高?DNA?样品的利用率。另一种形式的 MPCR 是组合 PCR, 组合 PCR 是在同一 PCR 反应中使用几个不同的模板和几对引物。多元 PCR 和组合 PCR 往往被当作同义词使用。设计策略MPCR 要求所有的引物对在同一条件下扩增其各自的特异序列。大多数多元 PCR 反应 局限于扩增 5~10 个目的片段,原因之一是反应中,每另加入一对引物会导致一定程度的灵活性的丢失。引物数量的增加也使引物二聚体和非特异扩增出现的概率增加。因此,进行多元 PCR 要求周密计划,且需多次尝试,使反应条件优化。理论上,一个多元反应中,所有引物扩增其特异序列的效率应该是一样的,但通常是很难预测一对引物的效率。在相似条件下,退火温度几乎相同的寡核苷酸可更好地工作。多元 PCR 引物设计和优化的一般规律当设计 MPCR 引物时,除了引物设计的一般规律外,其他一些因素也必须考虑。一般 来说,一个多元反应中
开始之前:其实非常简单,不需要你下载任何软件,但是你得有一台电脑能上网。当然,最重要的是,你要很清楚用于做引物的模板序列,至于怎么找模板序列,不再本次讨论范围。另外,要先对PCR目的序列的长度有个大致估计,好了,马上开始吧:第一步:找到Primer3的站点。 你不用记住这个站点,但是要记住“Primer3”这个词,然后打开GOOGLE首页,输入Primer3,跳出来的第一个项目就是了“Primer3 Input 0.4.0 ” 。第二步:贴上模板序列。 进入Primer3站点,可以看到一个引物设计的界面。(如下图)在“Paste source sequence below (5'->3'…”下面的大空框里面把你的模板序列粘帖进去。注意是5'->3'方向的,数字或者空格都没关系,软件会自动过滤的。第三步:重要参数设定。 首先是“ Product Size Ranges ”,如果你不希望软件给你随便做的话,首先要调整的就是这个参数。默认的参数实际上是从100到1000,这个你得自己改,如果你希望产物的大小符合你的预期,尽可能把范围改小,比如480-500,具体看情况调整。第二个
在体外将两个或多个来源相同或不相同的 DNA 片段连接成新的重组 DNA 分子,再转到特定宿主细胞中进行自主复制并表达。这是分子生物学中的基本技术。DNA 重组技术的基本程序包括:(1)获得外源 DNA:外源 DNA 是进行 DNA 重组的目的 DNA 片段,一般采用 DNA 聚合酶链式反应 (PCR) 或逆转录-DNA 聚合酶链式反应 (RT-PCR)、基因组文库或 cDNA 文库筛选等方法获得。(2)载体的构建或选择:分子生物学中用的载体是指能在特定宿主细胞中自主复制的 DNA 分子,例如细菌的质粒、噬菌体、病毒等,常用的载体一般为质粒;根据需要可直接从公司购买合适的载体,也可以自己构建。(3)连接:目的 DNA 片段和适当载体的连接, 一般采用核酸内切酶分别消化 DNA 片段和载体,使它们的末端能够连接到一起构成重组 DNA 分子。由于所用内切酶的切割特点不同,产生三种连接方式:粘端连接、平端连接和不相配的连接。(4)转化:将连接的重组 DNA 产物导入合适的宿主细胞,使其在宿主细胞内复制扩增或表达,赋予宿主细胞新的生物特征。(5)克隆化:重组 DNA 分子转化大肠杆菌后,在平板
一、热启动 PCR热启动 PCR 是除了好的引物设计之外,提高 PCR 特异性最重要的方法之一。尽管 Taq DNA 聚合酶的最佳延伸温度在 72℃,聚合酶在室温仍然有活性。因此,在进行 PCR 反应配制过程中,以及在热循环刚开始,保温温度低于退火温度时会产生非特异性的产物。这些非特异性产物一旦形成,就会被有效扩增。在用于引物设计的位点因为遗传元件的定位而受限时,如 site-directed 突变、表达克隆或用于 DNA 工程的遗传元件的构建和操作,热启动 PCR 尤为有效。 限制 Taq DNA 聚合酶活性的常用方法是在冰上配制 PCR 反应液,并将其置于预热的 PCR 仪。这种方法简单便宜,但并不能完成抑制酶的活性,因此并不能完全消除非特异性产物的扩增。 热启动通过抑制一种基本成分延迟 DNA 合成,直到 PCR 仪达到变性温度。包括延缓加入Taq DNA 聚合酶在内的大部分手工热启动方法十分烦琐,尤其是对高通量应用。其他的热启动方法使用蜡防护层将一种基本成分,如镁离子或酶,包裹起来,或者将反应成分,如模板和缓冲液,物理地隔离开。在热循环时,因蜡熔化而把各种成分释放出来并混合在一
DNA 序列的改变称为突变, 这将导致相关蛋白质的序列变化。 DNA 上特定核苷的取代技术称作基因定位突变法 (site directed mutagenesis)。 通过病酶动物将突变的基因导入微生物体内即可产生非天然蛋白. 这种方法在研究蛋白质中特定氨基酸的功能上极为有价值。与定位突变不同, 在 PCR 中增加 Mg2 离子可产生随机点突变; 高盐度降低了 DNA 聚合酶的再现精度。突变频率可由离子浓度控制。这种方法称作"易错 PCR"。将突变基因重组在加速产生多样性方面较定位突变效率更高。这种方法称作 DNA 改组技术 (shuffling)。
实验原理核酸分子杂交是通过配对碱基对之间的非共价键(主要是氢键)结合,从而形成稳定的双链区。杂交分子的形成并不要求两条单链的碱基顺序完全互补,所以不同来源的核酸单链只要彼此之间有一定程度的互补顺序(即某种程度的同源性)就可以形成杂交双链。分子杂交可在 DNA 与 DNA、RNA 与 RNA 或 RNA 与 DNA 的二条单链之间进行。由于 DNA 一般都以双链形式存在,因此在进行分子杂交时,应先将双链 DNA 分子解聚成为单链,这一过程称为变性,一般通过加热或提高 pH 值来实现。用分子杂交进行定性或定量分析的最有效方法是将一种核酸单链用同位素或非同位素标记成为探针,再与另一种核酸单链进行分子杂交。随着基因工程研究技术的迅猛发展,新的核酸分子杂交类型和方法在不断涌现和完善。核酸分子杂交可按作用环境大致分为固相杂交和液相杂交两种类型:一、固相杂交将参加反应的一条核酸链先固定在固体支持物上,一条反应核酸游离在溶液中。固体支持物有硝酸纤维素滤膜、尼龙膜、乳胶颗粒、磁珠和微孔板等。由于固相杂交后,未杂交的游离片段可容易地漂洗除去,膜上留下的杂交物容易检测和能防止靶 DNA 自我复性等优点,所以