代谢组+重测序联合分析
- 询价
- 代谢组+重测序联合分析
- 全国
- 2025年07月15日
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 提供商:
武汉迈特维尔生物科技公司
- 服务名称:
代谢组+重测序联合分析
1.产品简介:
全基因组关联分析(Genome-wide association study,GWAS)是指利用全基因组重测序或外显子测序技术获取数以百万计的SNP分子标记,与表型数据进行联合分析,从中筛选出与疾病相关的SNP,发现影响复杂性状的基因变异。GWAS已经识别了大量相关的基因组变异位点,并在实践中发现了许多关联基因,但却仅能解释遗传性状的一小部分,因为表型获取的数据有限,且大部分不能量化,大大局限了GWAS在基因定位和功能研究上的应用。
2013年,高通量的“广泛靶向代谢组”方法的建立使得准确定性定量的大队列代谢组学研究成为可能。群体重测序数据结合群体代谢组数据开展的mGWAS(metabolome Genome-wide association study,mGWAS)研究方法的建立,为大批量、高精度、高遗传效应的基因定位以及基因功能研究提供了新的思路。与GWAS相比,mGWAS以代谢物替代表型,可获得更多、可量化的数据,广泛靶向代谢组技术联合基因组重测序技术,在数据挖掘上有明显优势:
| 特点 |
GWAS |
mGWAS |
| 表型数量 |
少 |
数据量大 |
| 定量 |
大多不能量化 |
可以定量 |
| 定位的未知SNP |
少 |
多 |
| 假阳性率 |
高 |
低 |
| 定位的准确性 |
低 |
高 |
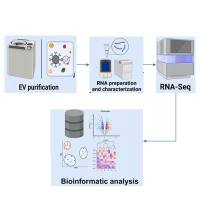
2.技术路线:
3.部分分析内容:
代谢物遗传力分析
曼哈顿图
4.样本要求
① 代谢组样本要求
血清/血浆:200ul/sample,液氮速冻后-80℃保存。
组织/粪便:200mg/sample,液氮速冻后-80℃保存
细胞:≥1×107/sample,液氮速冻后-80℃保存
注:干冰寄送;避免反复冻融;尽量避免溶血。
② 重测序样本要求
组织样本,≥300 mg,液氮速冻后-80℃保存;
血液样本,新鲜的全血≥2ml;
其他样本类型请咨询相关工作人员。
5.文章案例
Genetic architecture of human plasma lipidome and its link to cardiovascular disease
期刊:Nat Commun
影响因子: 11.878
发表时间:2019.09
研究背景
心血管疾病(CVDs)是全世界死亡率较高的疾病之一,需要由好的预防和预测策略。血脂是公认的心血管病遗传危险因素,常规监测以评估CVD风险。传统的血脂如总胆固醇和甘油三酯通常被监测以评估心血管疾病的风险。传统脂质与脂类的遗传相关性较低,而且这些传统脂质的测量方法并不能检测到人体血浆中所包含的数百种同样称为脂质的分子成分,这其中许多脂质是心血管疾病的危险因素。使用基因组学和脂质组学方法获得全基因组数据,以改善对CVD病理生理的了解。
研究思路:
首先在2181名受试者中对141种脂类进行全基因组关联分析,然后在511700个个体中对25种与心血管疾病相关的表型进行全基因组分析。
研究结果:
1.脂质种类的遗传力
使用遗传关系矩阵对所有研究参与者确定了每种脂质种类和传统脂质的基于SNP的遗传力。神经酰胺(CERs)显示出最大的遗传度,磷脂酰肌醇(PIs)显示出最小的遗传度。
2.脂质的全基因组关联分析
对141个脂质物种进行了全基因组关联分析。确定了11个基因组位点(1MB区间)内的518个变异与来自10个脂质类别的42个脂质种类之间的2817个关联。
3.脂质与CVD风险之间的关系
在发现的35种脂质物种变体中有10种与CVD风险有关联性,并且鞘脂(包括CER和SM)在CVD的发病机理中具有重要作用。
4.脂质组学较传统脂质有更高的统计能力
使用先前为传统脂质确定的变体评估脂质物种是否有助于检测比传统脂质具有更大能力的遗传关联。结果显示,在相同样本量的情况下,分子脂质物种比传统脂质具有更强的相关性。这表明类脂组学提供了更高的机会来识别脂质调节变异体,特别是直接作用于脂质代谢的变异体,其样本量比传统脂质小得多。
研究结论:
研究整合了脂质体、基因组和表型,揭示了脂质体的遗传调控及其与心血管疾病风险的关系的详细描述。除了加强对循环脂质遗传决定因素的了解,该研究强调了脂质组学在脂质和心血管疾病基因定位方面的潜力,而非传统脂质。该研究还建立了一个公开可用的知识库,该知识库是关于分子脂质种类的遗传关联及其与数千种临床结果的关系的。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验GUT:国家癌症中心崔巍联合多组学技术团队发表血清代谢组肠癌早筛新机制
的诊断标志物应具有非侵入性和诊断准确的特点,本研究提出的 8 个 GMSM 标志物组就符合上述特点。虽然该发现还需进行更严格的验证,但已经展现出让人振奋的临床应用前景。而这篇文章使用非靶代谢组-肠道菌群宏基因组整合分析寻找潜在标志物、靶向代谢组学技术验证发现结果、AFADESI-MSI 空间代谢组技术从另一维度对结果进一步确认,一整套“宏基因组+代谢组技术组合拳”打得行云流水,不仅最大程度发掘了代谢组学技术的应用潜力,多组学联合分析的思路也非常值得相关研究者借鉴。本文作为临床生物标志物发掘的典型案例
本节课介绍了多种类型修饰组学的联合分析。
实验或组学技术联合分析,再涉及到多组学分析的环节,把课题联合分析做完善是关键。 研究思路文章参考: 中文标题:人参固本对甲状腺素毒症小鼠的抗衰老作用:改善免疫衰老、低蛋白血症、脂毒性和肠道菌群 研究对象:小鼠 发表期刊:Frontiers in Immunology 影响因子:8.786 发表时间:2022 年 10 月 25 日 合作单位:鲁南制药集团,山东大学齐鲁医院 运用组学技术:流式细胞技术、蛋白质组学,粪便代谢物学、植物代谢组学和微生物组学,其中蛋白组学和代谢组学由鹿明生物提供检测和支持
 技术资料
技术资料暂无技术资料 索取技术资料