相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 规格:
1mL
Protein L Magnetic Beads
本产品4℃运输;保存于4℃,禁止产品冻结,长期存放请保证试剂管竖立向上,保质期24个月。
货号规格
goodYJ004 1 mL
产品简介
good本产品采用新一代纳米表面生物技术,将Protein L高密度共价偶联在超顺磁性纳米微球表面,是纯化大多数免疫球蛋白的理想工具。与传统的Protein L免疫沉淀琼脂糖凝胶相比,Protein L磁珠具有更大的特异性表面区域及更多的表面抗体结合位点,非特异性结合低,并且每次IP和Co-IP可以节省40%的时间,使用起来简便高效。
goodProtein L磁珠可应用于多种样品,细胞裂解液、细胞分泌液上清、血清、动物腹水以及其它的免疫抗原等均可适用。
产品参数
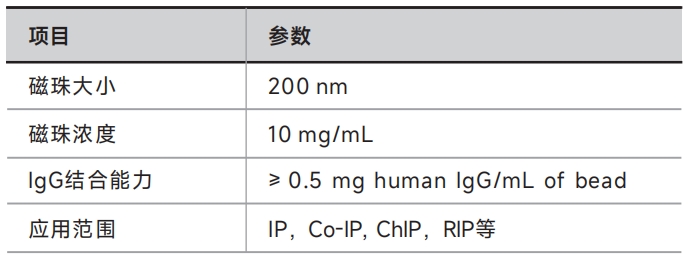
自备试剂

操作步骤
good◆gg1. 根据样品种类选择相应的处理方法:
good◆ 样1. 根A. 血清样品:若目标蛋白丰度较高,建议用 结合缓冲液 或1×PBS(货号:PS110)稀释血清样品至目标蛋白终浓度为10~100 µg/mL,置于冰上备用(或置于-20℃长期保存);
good◆ 样1. 根B. 悬浮细胞:离心收集细胞(4℃,500×g,10 min),弃上清后称重,按每毫克细胞50 µL的比例用1×PBS(货号:PS110)洗涤2次;按每毫克细胞5~10 µL的比例加入 结合缓冲液 ,同时加入蛋白酶抑制剂(货号:GRF101),混匀后置于冰上孵育10 min;离心收集上清液(4℃,14000×g,10 min),置于冰上备用(或置于-20℃长期保存);
good◆ 样1. 根C. 贴壁细胞:移去培养基,按每1.0×105个细胞150 µL的比例用1×PBS(货号:PS110)洗涤两次;用细胞刮刀刮落细胞,收集至1.5 mL离心管内,按每1.0×10个细胞20~30 µL的比例加入 结合缓冲液 ,同时加入蛋白酶抑制剂(货号:GRF101),混匀后置于冰上孵育10 min;离心收集上清液(4℃,14000×g,10 min),置于冰上备用(或置于-20℃长期保存);
good◆ 样1. 根D. 大肠杆菌:离心收集大肠杆菌(4℃,12000×g,2 min),弃上清后称重,按每克菌体(湿重)10 mL的比例用1×PBS(货号:PS110)洗涤2次;按每克菌体(湿重)5~10 mL的比例加入 结合缓冲液 ,同时加入蛋白酶抑制剂(货号:GRF101),重悬菌体,超声裂解细胞,离心收集上清(4℃,12000×g,10 min)。
good◆ 磁珠预处理
good◆gg2. 用移液器轻柔吹打 Protein L磁珠 ,使其充分混悬,取25~50 µL磁珠悬液置于1.5 mL 离心管中;
good◆gg3. 加入500 µL 结合缓冲液 或1×PBS,用移液器轻柔吹打重悬磁珠,接着在磁力架上静置1 min,待磁珠吸附到离心管侧壁上后,吸弃上清;
good◆gg4. 重复步骤3两次;
good◆ 抗体与磁珠结合
good◆gg5. 稀释:用 结合缓冲液 或1×PBS稀释抗体样品至终浓度为5~50 µg/mL,置于冰上备用;
good◆gg6. 结合:将500 µL上步稀释好的抗体加入预处理后的磁珠中,置于翻转混合仪上孵育(常温2 h,4℃ 4~6 h或过夜),接着在磁力架上静置1 min,待磁珠吸附到离心管侧壁上后,把上清液转移到新的离心管中备用(上清液可用于检测抗体是否存在残留),离心管中剩余的即为 抗体-磁珠复合物 ;
good◆gg7. 洗涤:在上一步得到的 抗体-磁珠复合物 中加入500 µL 结合缓冲液 或1×PBS,用移液器轻柔吹打重悬磁珠,接着在磁力架上静置1 min,待磁珠吸附到离心管侧壁上后,吸弃上清。再重复此步骤两次;
good◆ 抗原与抗体-磁珠复合物结合
good◆gg8. 结合:向洗涤后的 抗体-磁珠复合物 中加入500 µL步骤1制备好的样品,置于翻转混合仪上孵育(常温2 h,4℃ 4~6 h或过夜),接着在磁力架上静置1 min,待磁珠吸附到离心管侧壁上后,吸弃上清,离心管中剩余的即为 抗原-抗体-磁珠复合物 ;
good◆gg9. 洗涤:在上一步得到的 抗原-抗体-磁珠复合物 中加入1 mL 洗涤缓冲液 或1×PBS,用移液器轻柔吹打重悬磁珠,接着在磁力架上静置1 min,待磁珠吸附到离心管侧壁上后,吸弃上清。再重复此步骤三次;
good◆g10. 洗脱:本操作说明书提供以下两种抗原洗脱方案,操作者可根据后期检测的需要选择不同的抗原洗脱方法。
goodgoodgoodgo• 变性洗脱:此方法洗脱的样品适用于SDS-PAGE检测。向步骤9洗涤后的 抗原-抗体-磁珠复合物 中加入60 µL 1×SDS-PAGE上样缓冲液(货号:LT101)混合均匀,100℃加热10 min。待冷却后,将离心管在磁力架上静置1 min,待磁珠吸附到离心管侧壁上后,收集上清,进行SDS-PAGE检测。
goodgoodgoodgo• 非变性洗脱:此方法洗脱的样品保持原有的生物活性,可用于后期功能分析。向步骤9洗涤后的 抗原-抗体-磁珠复合物 中加入25~50 µL 洗脱缓冲液 ,室温孵育10 min;将离心管在磁力架上静置1 min,待磁珠吸附到离心管侧壁上后,收集上清液至新的离心管,并立即加入1 µL 中和缓冲液 将洗脱产物pH调节至中性,用于后期功能分析。
常见问题及对策
go◆ 如何避免磁珠在储存或使用过程中可能出现的聚集情况?
go◆ 答:磁珠应保存在2~8℃,使用时应避免由于污染或干燥而导致的聚集。磁珠在低pH值的洗脱缓冲液中发生聚集属于正常现象,不影响磁珠的正常使用。在 结合/洗涤缓冲液 和 洗脱缓冲液 中添加终浓度为0.1%(V/V)的非离子型去垢剂(如Triton X-100、Tween-20或NP-40)可有效防止磁珠聚集。经过低pH值洗脱操作的磁珠可以用结合缓冲液洗涤至中性,然后用含有0.1%(V/V)Tween-20的Tris buffer(pH 7.5)振荡重悬磁珠,并用超声波水浴处理2 min,即可使磁珠恢复均匀状态,以上处理均不影响磁珠的抗体结合效率。
go◆ 磁珠在使用过程中出现结块现象?
go◆ 答:磁珠在极少数情况下会出现结块现象,一般较难振荡打散,从而导致分布不均匀,这主要是因为磁珠在磁场中放置太久而牢固地结合在一起。用超声波水浴处理2 min即可打散磁珠,但要注意超声处理也会使磁珠在样品溶液中捕获的抗体脱落,因此磁珠在加样后洗脱前不宜使用该方法。
go◆ 如何提高抗体与磁珠结合效率?
go◆ 答:磁珠抗体间的结合效率与抗体的种属来源及所属亚型有关,请确认抗体的类型与Protein L配基的亲和效率。如抗体所属亚型与Protein L的亲和度较低,可以通过增加抗体与磁珠的孵育时间(30~120 min)、提高结合缓冲液的pH值(8~9)及降低离子强度(25~10 mM NaCl)等方法提高亲和效率。
go◆ 如何提高磁珠在免疫沉淀反应中的特异性?
go◆ 答:可以先将抗体与样品进行孵育,形成抗体-抗原复合物,再用Protein L磁珠捕获复合物。这种方法可以提高抗体与抗原的结合效率,并降低磁珠与样品接触的时间,从而提高沉淀产物的特异性。对于蛋白质/核酸共沉淀或染色质免疫共沉淀也推荐使用此法。
go◆ 如何解决磁珠易粘附管壁的现象?
go◆ 答:建议使用低吸附率的耗材进行磁珠操作。另外,在缓冲液中添加0.01%~0.1%(V/V)的非离子型去垢剂(如Triton X-100、Tween-20或NP-40)可以有效降低耗材对磁珠的粘附。
注意事项
good1. 为了您的安全和健康,请穿实验服并戴一次性手套操作;
good2. 本产品仅限科研使用。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验基于针对细胞表面标记蛋白的偶联磁珠,利用磁场对目的细胞群体分离是 MACS 磁珠最广泛的应用领域。但 MACS Technology的神通广大不仅仅于此,在蛋白质、核酸分子水平的分离应用中也具有卓越的性能和优势,今天让我们了解一下。 一个细胞也能做的 mRNA 分离和 cDNA 合成 精确的基因表达分析离不开高质量的 mRNA 分离,必须克服潜在的 DNA 污染和 RNA 降解等严重影响数据的风险。传统提取核酸的方法有赖于多步骤的离心和沉降过程,这在样品细胞数量极少时,则带来极大的弊端
磁珠,并可接受订制服务。三、Dynabeads的使用方法Dynabeads可加入到不同种类的悬浮液中以结合靶物质(如细胞、核酸、细菌或其他生物分子),形成一种Dynabeads·靶物质混合物,在通过磁分离器(如Dynal MPC)后可以将该混合物从悬液中移去。四、Dynal MPC 磁分离器的优点1、操作简便2、磁性强久3、适合多种体积(50μl~50ml)4、分离迅速目录号产品说明规格价格(RMB)120.01Dynal MPC-1 for 5ml - 50ml tubes1 unit
Analysis and Purification of Antibody Fragments Using Protein A, Protein G, and Protein L
Today, monoclonal antibodies (mAbs) form the largest category of biopharmaceuticals in clinical trials and their number is expanding rapidly (DataMonitor 2007). The antibodies or functional antibody fragments are being produced in artificial












