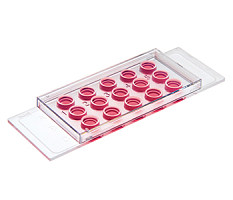
18孔血管生成载玻片
- ¥99
- coolrun
- CR215-G-1
- 深圳
- 2026年04月10日
相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
1000
- 现货状态:
现货
- 供应商:
铨源生命(深圳)科技有限公司
- 规格:
EO灭菌,独立包装
| 品牌 | 货号 | 商品名称 | 包装 | 描述 |
| COOLRUN | CR215-G-1 | 血管生成载玻片 | 独立包装,EO灭菌 一张板有18个孔 |
可以用于血管生成实验 也可以用于类器官培养 |
血管生成实验说明文档
一、血管生成概述
1.1 血管网络的功能
血管网络在哺乳动物体内发挥着至关重要的运输功能,负责将液体、气体、分子以及细胞等物质输送到全身各个部位。同时,免疫细胞借助血管网络进行巡逻,抵御细菌、病毒和寄生虫的入侵。
1.2 血管生成的重要性
- 在正常的生理过程中,血管生成对于胚胎发育、伤口愈合、骨骼生长、妊娠以及月经周期等起着关键作用。
- 疾病关联:当血管生成失调时,可能引发多种疾病,如中风、心肌梗死、动脉粥样硬化和关节炎等。此外,肿瘤血管化是癌症的重要特征之一。
1.3 血管生成机制
- 血管形成(Vasculogenesis):中胚层前体细胞(成血管细胞)分化为内皮细胞,组装形成新血管。
- 血管新生(Angiogenesis):通过现有血管的“出芽”扩展血管网络,涉及基底膜穿透、细胞迁移、增殖和通讯。
- 调控因素:缺氧是主要驱动因素,诱导促血管生成基因(如VEGF)表达。目前,抑制或激活血管生成已成为一些疾病的治疗靶点,例如贝伐单抗被用于转移性结直肠癌和非小细胞肺癌的治疗。
二、血管生成实验方法
2.1 血管生成实验(Tube Formation Assay)
实验原理
内皮细胞(如HUVECs)在基底膜类似基质(如Matrigel®)上形成毛细血管样结构,模拟体内血管生成过程。
实验步骤
1. 实验准备:
(1)在4°C环境中低温融化基质胶,并预冷相关器材(如枪头、待铺胶细胞培养板等)。铺板操作需在冰盒上进行,以防止基质胶在温暖环境中过早凝固。
(2)使用DMEM或条件培养基将基质胶稀释至8-12 mg/mL,根据实际情况可调整稀释比例。由于不同批次的基质胶浓度存在差异,建议在使用前进行不同梯度的稀释。将稀释后的基质胶分别取10 µl加入孔板内,注意避免产生气泡,然后将孔板置于37℃培养箱中放置30-45 min。
(3)对状态良好的细胞采用标准的传代细胞程序进行处理,并å通过预实验确定合适的细胞铺板数量,使其在24 h内达到约80%的融合度。对HUVEC细胞进行饥饿处理,即将完全培养基更换为含1% FBS的DMEM培养基,培养24 h。
2. 细胞接种:
(1)使用DPBS清洗细胞,随后加入胰蛋白酶对HUVEC进行消化。离心沉淀后,使用含有10% FBS的DMEM或条件培养基重悬细胞,并进行多次细胞计数以取平均值,确保准确性。如果需要获取荧光影像数据,可在DPBS清洗细胞前添加终浓度为2 μg/ml的钙黄绿素AM,将标记后的细胞置于37℃和5%CO₂的黑暗环境中30-45 min,之后进行洗涤以去除多余的钙黄绿素AM。
(2)每孔加入50 μl细胞悬液,推荐HUVECs的接种密度约为10,000±3000细胞/孔。在操作时,需保持枪头垂直于孔的上方,避免枪头接触孔内的凝胶。
3. 成像与分析:
(1)将细胞培养板置于37℃、5% CO₂的环境中静置培养。
(2)可根据需要设置时间梯度进行观察,或在特定时间点进行观察。一般来说,细胞在2-4h内开始形成血管样结构,HUVEC种植至基质胶后约4小时即可初步形成血管样结构,管形成峰值通常出现在2-12h之间,之后结构可能会发生塌缩。
(3)拍摄毛细管网络的图像,并可使用Image J的Angiogenesis Analyzer插件或其他软件对管状网络的节点、管数量、管长度、管面积等表型进行分析。
常见应用
- 评估药物促/抗血管生成潜力
- 研究基因与通路对血管生成的影响
- 分析抑制剂或增强剂的作用
注意事项
- 细胞密度:HUVECs推荐5,000–10,000细胞/孔,需预实验优化。
- 基质选择:优先使用生长因子减除型Matrigel®(测试促血管药物时)。
- 对照设置:阳性对照(无抑制剂)、阴性对照(使用不影响细胞活性的抑制剂)。
2.2 血管出芽实验(Sprouting Assay)
实验原理
将多细胞球体置于凝胶基质中,观察内皮细胞向外“发芽”的过程,以模拟血管生成中的出芽现象。
实验步骤
1. 样本制备:将细胞球体嵌入凝胶(如Matrigel®)。
2. 成像与量化:定期拍摄并测量发芽长度。
三、实验优化与常见问题
4.1 时间框架
- HUVECs:2–4小时开始血管生成,24小时后细胞凋亡导致管结构破坏。
- 实时成像:建议每5–15分钟拍摄一次,持续24小时(需自动聚焦和电动载物台)。
4.2 实验设计要点
- 细胞异质性:不同内皮细胞血管生成时间差异大,需预实验确定。
- 移液精度:使用校准移液器确保凝胶和细胞接种量准确(避免弯液面)。
Q&A
1. 血管生成实验需要多长时间?
血管生成实验时长受细胞状态和培养基中血管生成因子浓度影响,二者呈正相关。当细胞处于良好状态时,通常在 2 - 3 小时内就能观察到血管生成现象;反之,若细胞状态欠佳,可能要 18 - 24 小时才会出现血管生成。基于此,在初次开展实验时,建议每间隔 4 小时进行一次观察。另外,使用原代细胞进行血管生成实验时,由于细胞特性,血管生成时间可能会有所延迟。
2. 管状网络形成监测方式选择
手动监测和自动监测各有利弊:
l 手动监测:灵活性强,成本较低,但主观性相对较高,重复性较差,且操作过程较为耗时。
l 自动监测:能提供更客观、高效、精确的结果,但成本较高,且适应性有限,软件可能无法满足所有非常规实验设计需求。
当实验涉及大量样本,或对结果的客观性和重复性要求极高时,自动监测是更佳选择。特别是对于不熟悉所用细胞类型的血管生成行为时,通常会在 24 小时内每 5 - 15 分钟自动拍摄一次照片,以精准监控管形成进程。而若实验规模较小,对结果的详细观察和分析要求较高,且实验室资源有限,手动监测也能满足需求。
3. 无血管生成如何处理?
l 可能原因包括:细胞老化、细胞损伤导致细胞状态不佳、细胞密度过高或过低,或基质胶浓度不合适、过期或质量不佳。
l 解决方案:对于细胞状态不佳的情况,可更换健康细胞或使用代数较低的细胞;针对细胞密度问题,应确保用于血管生成实验的细胞均匀分布且密度适中,由于最佳接种密度具有细胞类型特异性,需通过多次摸索确定;用于实验的培养基应与接种细胞时所使用培养基成分相同,换液时动作要轻柔,以免影响细胞状态;对于基质胶质量问题,可通过重新稀释、更换品牌或批次等方式,确保使用新鲜、质量良好的基质胶。
4. 怎样操作可使基质胶铺板均匀?
l 体积校准:通过标尺纸验证凝胶体积(合适体积时标尺无缩放效应)。
l 基质胶需保存于-20℃,使用时在4℃融化,铺板操作需在冰上进行,以减缓凝固速度。
l 向孔内加入基质胶时应尽可能垂直加入,防止基质胶流经孔壁留下残留胶,并尽量一次性将基质胶铺垫均匀,避免多次加减试剂。
l 在37℃放置固化时,确保放置在水平平面上,以保证实验的准确性和稳定性。
5. 血管生成实验对照组设置
在初次进行血管生成实验时,最少应设置三组对照,具体如下:
l 空白对照组:可以是不含细胞的基质对照组,用于排除基质自身可能带来的背景信号或结构干扰;也可以是仅含有细胞而未进行基质铺板的组别。
l 阳性对照组:需向其中加入已知的促进血管形成物质,在正确的实验条件下应能观察到明显的管状结构形成。
l 阴性对照组:可使用未经任何处理的细胞,或向其中加入已知的血管形成抑制剂。
若实验目的是测试某种药物或化合物对管形成的影响,还需设置不同浓度的该物质作为对照组,同时包括一个无药物处理的对照组,以此评估药物剂量与效果之间的关系。
6. 内皮细胞培养聚团应对策略
内皮细胞在培养过程聚团可能由以下多种因素引起:
l 细胞密度过高或铺板不均匀:可根据实验需求调整细胞接种密度,充分混匀细胞悬液,铺板时动作轻柔、均匀,确保细胞均匀分布。
l 细胞状态不佳或老化:应定期检查细胞状态,及时进行传代操作,避免细胞过度密集培养,以维持细胞的健康状态。
l 基质胶质量差:质量不佳或处理不当的基质胶可能导致细胞无法均匀铺展,需确保基质胶新鲜且严格按照说明书要求进行正确处理。
l 血清促贴壁因子缺乏:建议使用新鲜培养基,或更换为内皮细胞专用培养基,以提供足够的促贴壁因子。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验:1、实验前一天需要将Matrigel置于冰盒,放入冰箱中,同时需要准备一些预冷的枪头用于吸取Matrigel胶;2、将Matrigel胶加到血管生成载玻片时注意枪头要垂直于内孔的正上方加入Matrigel,防止有Matrigel流经上孔而留下残留胶;3、需要按照细胞的生长速度定时采集图像,并且对其成管长度、覆盖面积、成环数和结点进行测量和记录,并且对其进行统计分析;4、分上下孔的ibidi血管生成载玻片能去除凹液面,使成像效果更好。 血管生成载玻片纵截面示意图 (Matrigel铺在下孔,细胞
细胞生长因子 2 (FGF-2) 、骨形态发生蛋白 4 (BMP4) 和血管内皮生长因子 A (VEGF-A) 的刺激下,内皮细胞在中胚层祖细胞中产生,并组成原始管状网络。 随后,在血管生成的过程中,原有的神经丛进行重塑,新的血管发芽和分支,直到一个成熟的循环网络形成【2】。 本篇文章基于 Nature protocol【3】 发表的文章,整理了人类多能干细胞 (hPSCs) 来源的血管类器官培养方案。 培养过程遵循发育原理,依靠上述生长因子进行诱导分化,最终培养成为血管类器官网络。 图1. hPSCs
三句话读懂一篇 CNS,胎盘其实更像肿瘤组织,可能是遗传缺陷和不良妊娠之源...
春暖花开好时节,周末阳光明媚,坐在樱花树下了解最新学术进展,不失为一种粉色的浪漫! 本周学术君继续为大家带来 CNS 文章,助力科研顺利! 1. Science Translational Medicine:小细胞外囊泡促进血管生成 血管生成在胚胎发育和体内平衡中起着至关重要的作用,干细胞衍生的小细胞外囊泡(sEVs)被证明能促进心肌梗死(MI)后的血管生成。 2021 年 3 月 10 日,浙江大学医学院附属第二医院胡新央、王建安团队与阿拉巴马大学伯明翰分校张建一团队合作在 Science
 技术资料
技术资料暂无技术资料 索取技术资料