相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 服务名称:
和元生物目的基因调取
- 提供商:
OBiO和元生物
- 规格:
按服务周期算
人Oct-4启动子报告基因载体构建
摘要: 和元以人基因组为模板扩增Oct-4启动子序列并构建入pGL3-basic载体萤光素酶报告基因上游。根据萤光素酶的表达水平检测Oct-4启动子转录活性。
关键词:Oct-4,启动子, 转录活性, luciferase, 报告基因
一、实验原理
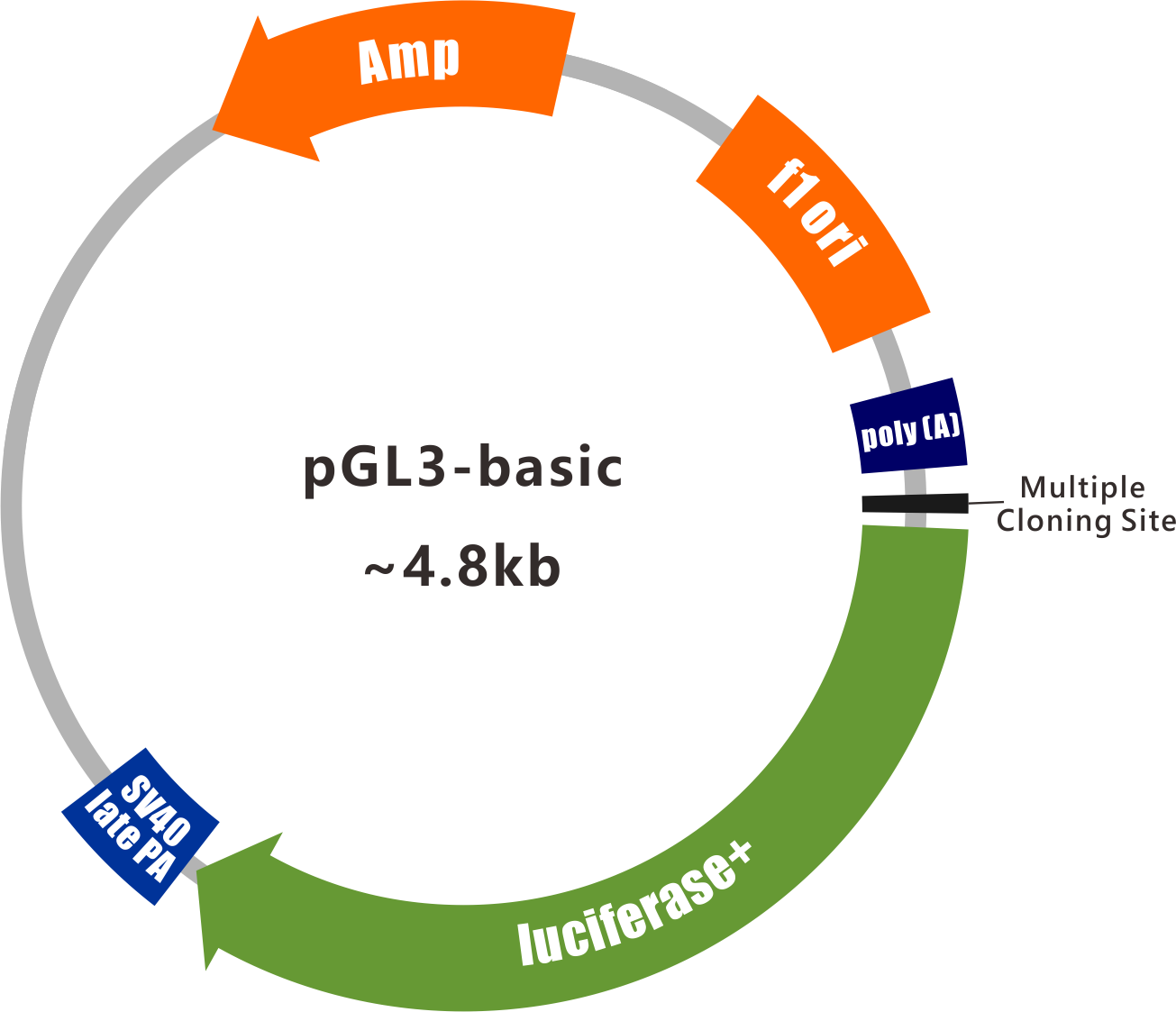
和元PCR扩增Oct-4启动子序列,构建于pGL3-basic载体luciferase上游。根据萤光素酶的表达水平检测Oct-4启动子转录活性。pGL3-basic载体图谱如下:

二、实验目的
和元构建用于检测Oct-4启动子活性的载体质粒。
三、实验方法
和元以人基因组DNA为模板扩增Oct-4启动子序列与经Mlu I和Xho I酶切后的pGL3-basic载体片段同源重组后转化E.coli感受态细胞。用菌落PCR鉴定转化子,筛选到的阳性克隆送测序。测序无误的克隆进行质粒抽提。实验步骤如下:
1. 引物设计:
和元从GenBank中查询目的基因上下游的序列,用VectorNTI软件进行引物设计。
PCR扩增目的片段:
使用高保真的PrimeSTAR酶扩增目的片段,反应体系和条件如下:

2. 琼脂糖凝电泳检测PCR扩增结果:
和元在目的片段PCR扩增成功后,进行琼脂糖凝电泳检测①,通过和DNA Maker的对比,判断目的片段是否扩增成功。
3. 胶回收目的片段:
和元把目的片段条带从琼脂糖凝电泳后的胶中割下来,用TaKaRa MiniBEST Agarose Gel DNA Extraction Kit Ver.3.0做胶回收,具体步骤参考试剂盒说明书。
4. 线性化表达载体的制备:
和元用限制性内切酶对检测载体的进行酶切,酶切反应体系为:质粒2μg, 10 x反应Buffer 5μL,限制性内切酶各1μL,用水补足50μL,于37℃水浴锅中孵育2h以上。酶切产物进行琼脂糖凝电泳检测酶切效果,并把目的载体条带从琼脂糖凝电泳后的胶中割下来,用TaKaRa MiniBEST Agarose Gel DNA Extraction Kit Ver.3.0做胶回收。
5. 目的片段同源重组到线性化检测载体中:

6. 感受态细胞的制备和转化:
DH5α感受态细胞的制备和转化,详见《精编分子生物学实验指南》②
7. 菌落PCR鉴定阳性转化子:
和元挑取平板上长出的转化子重悬于10µl LB培养液中,取1µl做模板进行菌落PCR鉴定。反应体系和PCR循环条件如下:

8. 阳性克隆送测序:
和元将菌落鉴定得到的阳性克隆,送公司进行测序验证。软件比对测序结果并分析。
9. 质粒小提:
和元的测序通过阳性克隆,安排质粒小提。具体步骤见试剂盒说明书。
四、和元实验结果
1. 和元PCR扩增目的片段:
用正向引物GTTTATCGATACGCGTTTCCCATGTCAAGTAAGGG(引物说明:含同源重组序列、Mlu I酶切位点,并含有目的基因5’端配对序列用于PCR扩增目的基因),反向引物GAAGCTTGAGCTCGAGGGGAAGGAAGGCGCCC(引物说明:含同源重组序列、Xho I酶切位点下划线标记的,并含有目的基因3’端配对序列用于PCR扩增目的基因)对人基因组DNA进行扩增,预期PCR产物大小为3948 bp,电泳结果如下:

1kb DNA ladder Marker:10 kb、8kb、6kb、5kb、4 kb、3.5kb、3kb、2.5kb、2kb、•1.5kb、1kb、750 bp、500 bp、250 bp
2. 和元检测载体的线性化
用Mlu I和Xho I对检测载体进行双酶切,胶回收4801bp的载体片段,酶切图谱如下:

第一泳道:空质粒;第二泳道:1kb DNA ladder Marker:10 kb、8kb、6kb、5kb、4 kb、3.5kb、3kb、2.5kb、2kb、1.5kb、1kb、750 bp、500 bp、250 bp;第三泳道:经Mlu I和Xho I酶切后的pGL3-basic载体
3. 和元菌落PCR鉴定阳性克隆
用菌落PCR鉴定转化子,正向引物Oct-4-F GCCTACCGTGGTATTAGATGTC位于目的基因序列中,反向引物Luc-N-R CCTTATGCAGTTGCTCTCC位于萤光素酶基因的N端序列,阳性克隆得到1324bp的片段。电泳结果如下:

1. 阴性对照(H2O) 2. 阳性对照(GAPDH) 3. DL2,000 DNA Marker: 2 kb, 1 kb,750 bp,500 bp,250 bp,100 bp 4-11. 挑取的8个转化子 接种阳性克隆,保种并分装100μL送测序。测序没有问题的,再接种抽提质粒。
4. 和元测序结果分析
阳性克隆测序结果表明,和预期序列完全一致。

五、和元参考文献
1. F.M.奥斯伯等著,马学军等译,精编分子生物学实验指南(第四版),科学出版社,P57~58
2. F.M.奥斯伯等著,马学军等译,精编分子生物学实验指南(第四版),科学出版社,P25~26
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验能对实验性学科作出贡献的。 二、生理学实验课的目的 1.通过实验使学生逐步掌握生理学实验的基本操作技术,了解生理学实验设计的基本原则,进一步了解获得生理学知识的方法,验证和巩固生理学的某些基本理论。 2.通过实验使学生逐步提高对实验中各种生理现象的观察能力、分析能力、独立思考和独立解决问题的能力。 3.在实验过程中,逐步培养学生在科学工作中的严肃的态度、严格的要求、严格的方法和严谨的作风。 三、生理学实验课的要求 提高实验课的教学质量,需
MgCl2,dNTP,引物,模板质粒pBS-CHI,无菌ddH2O。 5.实验准备 dNTP混合液(每种25mM),TAE电泳缓冲液,荧光染料,10´加样缓冲液,1.5ml离心管装入铝制饭盒(灭菌)、移液器吸头装入相应的吸头盒(灭菌)。合成的引物:Sense primer 5'-GGATCCACAATGATGAGAGCC-3' Antisense primer 5'-GATATCATGGTGAGGTAGCTAGCTT-3' 目的基因模板质粒:已经克隆在pBS载体上的1128bp几丁质
一种或者两种适当的限制酶切割,分别产生对称性粘性末端(用一种限制性内切酶进行消化而产生带有互补突出端)、不对称粘性末端(用两种不同的限制性内切酶进行消化而产生带有非互补突出端)、平端。在亚克隆时,首选不对称相容末端连接,次选对称性粘性相容性末端连接,由于平末端连接效率较低,通常很少采用。但有时目的片段的末端与载体不匹配 ,一般先将不匹配末端补平,然后再以平末端连接。(实验操作同前述)三、利用T4 DNA连接酶进行目的DNA片段和载体的体外连接(一)连接要求和结果外源DNA片段末端性质连接要求
 技术资料
技术资料暂无技术资料 索取技术资料