相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 规格:
20次/50次/100次(CX105×2)
| 规格: | 20次 | 产品价格: | ¥988.0 |
|---|---|---|---|
| 规格: | 50次 | 产品价格: | ¥1980.0 |
| 规格: | 100次(CX105×2) | 产品价格: | ¥2980.0 |
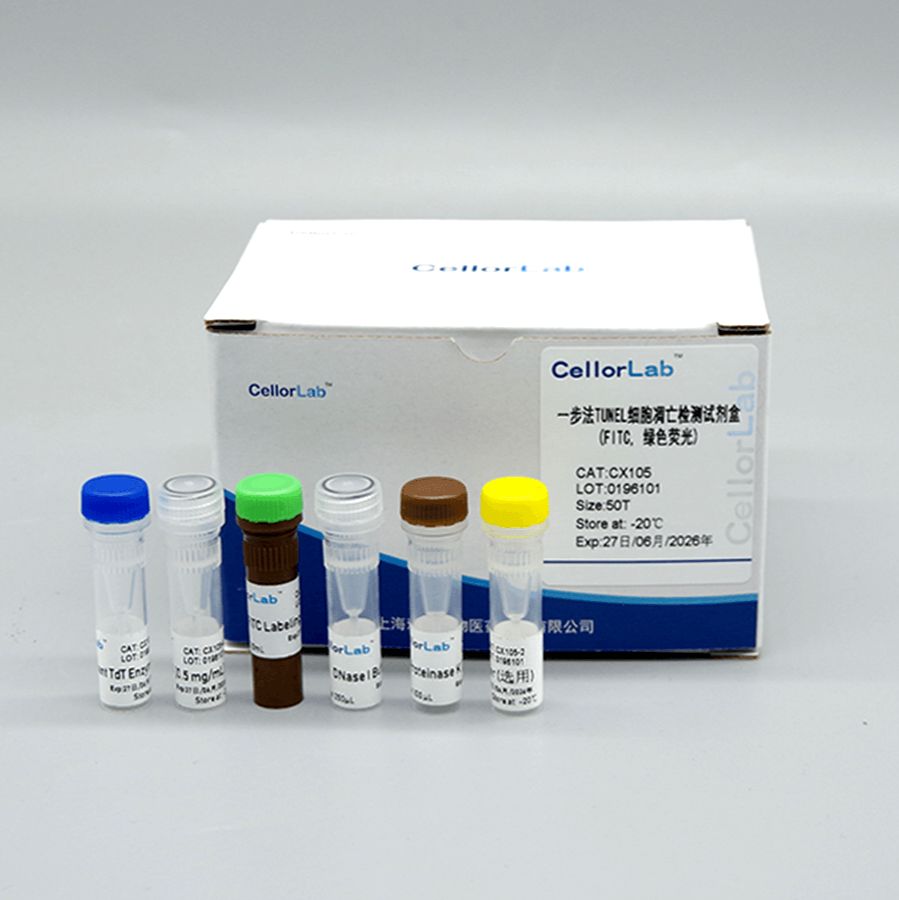
一步法TUNEL细胞凋亡检测试剂盒(FITC, 绿色荧光)
One-step TUNEL Cell Apoptosis Detection Kit (Green, FITC)
本产品需冰袋运输,-20°C避光保存,保质期12个月。
货号规格
产品简介
雅酶本产品采用 TUNEL(TdT mediated dUTP Nick End Labeling) 法,可高灵敏度且简单快速地检测细胞凋亡,对于细胞样本 ( 细胞涂片、细胞爬片、悬浮细胞 ) 或组织样本 ( 石蜡切片、冰冻切片 ),只需经过一步染色反应,洗涤后便可通过荧光显微镜或流式细胞仪检测被标记上绿色荧光的凋亡细胞。
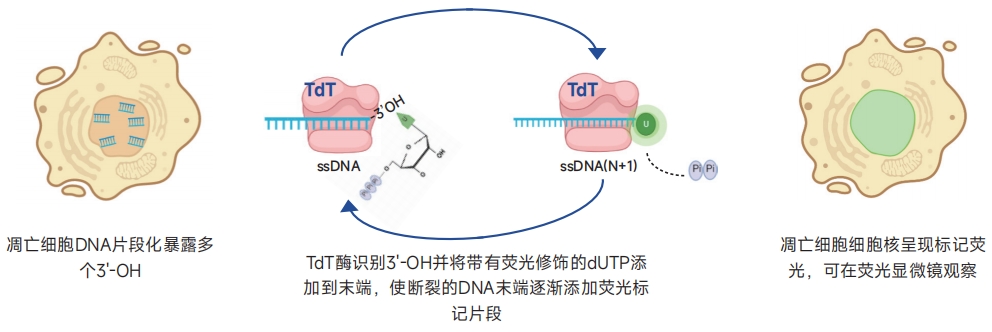
雅酶细胞凋亡时,细胞内的特异性核酸内切酶会被活化,并使染色质 DNA 在核小体间被特异性切割,DNA降解成180~200bp或其它整数倍片段。DNA 分子断裂产生的3'-OH末端可以在末端脱氧核糖核苷酸转移酶 (Terminal Deoxynucleotidyl Transferase,TdT) 的作用下结合 FITC-dUTP,被标记的DNA 可以直接使用荧光显微镜观察或通过流式细胞仪进行定量分析,从而反映细胞凋亡的水平。
示意图如下:
适用样本
雅酶组织样本(石蜡切片、冰冻切片)及细胞样本(细胞爬片、细胞涂片、悬浮细胞)。
产品内容
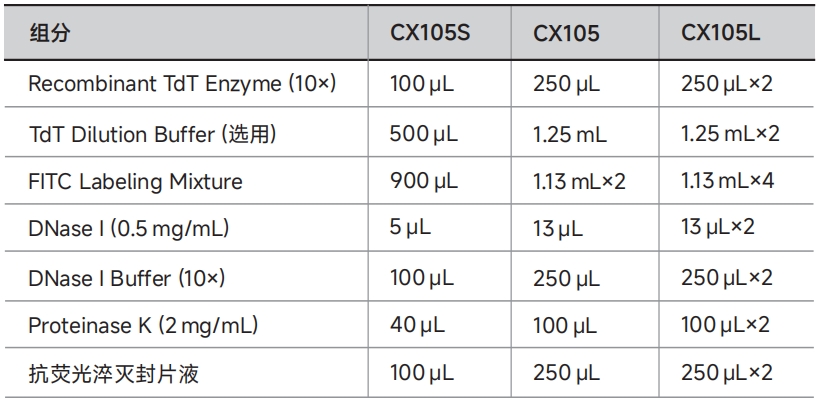
自备试剂
雅酶DAPI/PI、Triton X-100、1×PBS、4%多聚jia醛、无水乙醇。
操作步骤
◆配置工作液
Proteinase K工作液:取1μL Proteinase K(2mg/mL)加入99μL 1×PBS中,混匀。现用现配。
◆样本预处理
A. 贴壁细胞(细胞爬片/涂片)
1. 准备细胞爬片:在TC处理的细胞爬片上培养贴壁细胞。在对细胞进行凋亡诱导处理之后,用1×PBS漂洗爬片两次,转步骤2;
1. 准备细胞涂片:以2×106cells/mL的浓度将细胞重悬于1×PBS中。吸取50~100μL细胞悬液滴于多聚赖氨酸包被的载玻片上,用一片干净的载玻片轻柔地涂开细胞悬液,转步骤2。
2. 固定:将爬片/涂片浸入1×PBS配制的4%多聚jia醛溶液,常温进行细胞固定15min;
3. 将爬片/涂片浸入1×PBS中漂洗两次,每次常温放置5min;
4. 轻柔地去掉多余液体,并用吸水纸吸干爬片/涂片上样本周围的液体;
5. 通透:在每个样本上滴加100μL Proteinase K工作液,使溶液覆盖全部样本区域,常温孵育10min;也可将爬片/涂片浸于1×PBS配制的0.2% Triton X-100溶液中,常温孵育10min;
5. 注意:①Proteinase K通透时长很关键,时间过长会增加细胞在后续洗涤步骤中从载玻片上脱落的风险,时间过短则可能造成通透处理不充分,影响后续标记效率。建议进行预实验,确定最佳Proteinase K孵育时长;
5. 注意:②细胞爬片/涂片在处理时较易脱片,因此建议使用0.2% Triton X-100溶液进行通透,以避免脱片的发生。
6. 用1×PBS润洗样本2~3次。轻柔地去掉多余的液体,并用吸水纸小心吸干载玻片上样本周围的液体。在实验过程中,切勿让样本干燥。处理好的样本需放入湿盒中保持湿润。
B.悬浮细胞
1. 取3×106~5×106个细胞,用1×PBS漂洗两次,每次离心5min(300×g,4℃),然后用0.5mL 1×PBS重悬;
2. 固定:向细胞悬液中加入5mL 1×PBS配制的1%多聚jia醛溶液,4℃进行细胞固定20min;
3. 离心5min(300×g,4℃),弃上清,用5mL 1×PBS重悬细胞;
4. 再次离心5min(300×g,4℃),弃上清,用0.5mL 1×PBS重悬细胞;
5. 通透:向细胞悬液中加入5mL 70%乙醇(冰上预冷),冰上破膜30min;
5. 注意:①通透后的细胞折射率会下降,导致其边缘模糊不易观察,操作过程中应格外小心,避免丢失细胞;
5. 注意:②-20℃的条件下,细胞能在70%乙醇中保存一周。
6. 将通透后的细胞离心5min(300×g,4℃),弃上清,用5mL 1×PBS重悬细胞;
7. 再次离心5min(300×g,4℃),弃上清,用1mL 1×PBS重悬细胞;
8. 转移2×106个细胞至新的1.5mL离心管中,进行后续标记实验或阳性对照制备。
C.石蜡切片
1. 脱蜡:将石蜡切片置于二甲苯中浸泡10min;换用新鲜二甲苯再浸泡10min;更换50%的二甲苯再浸泡5min;无水乙醇中浸泡5min;更换新的无水乙醇再浸泡5min;更换95%乙醇浸泡5min;更换85%乙醇浸泡5min;更换75%乙醇浸泡5min;更换50%乙醇浸泡5min;更换30%乙醇浸泡5min;更换1×PBS浸泡5min;
2. 通透:用吸水纸吸干载玻片上切片组织周围的多余液体,每个样本上滴加100μL Proteinase K工作液,使溶液覆盖全部样本区域,37℃反应10min;
2. 注意:不同组织或物种的样本所需反应时长可能不同,Proteinase K通透时间过长会增加组织切片在后续洗涤步骤中从载玻片上脱落的风险,时间过短则可能造成通透处理不充分,影响后续标记效率。建议进行预实验,确定最佳Proteinase K孵育时长。
3. 将通透后的样本浸入1×PBS漂洗3次,每次5min。轻柔地去掉多余液体,并用吸水纸小心吸干载玻片上样本周围的液体。在实验过程中,切勿让样本干燥。处理好的样本需放入湿盒中保持湿润。
D.冰冻切片
1. 固定:将冰冻切片平衡至常温,浸入1×PBS配制的4%多聚jia醛溶液,常温固定15min;
2. 将固定后的冰冻切片浸入1×PBS漂洗两次,每次5min;
3. 通透:用吸水纸吸干载玻片上切片组织周围及背面的多余液体,每个样本上滴加100μL Proteinase K工作液,使溶液覆盖全部样本区域,37℃反应10min;
3. 注意:不同组织或物种的样本所需反应时长可能不同,Proteinase K通透时间过长会增加组织切片在后续洗涤步骤中从载玻片上脱落的风险,时间过短则可能造成通透处理不充分,影响后续标记效率。建议进行预实验,确定最佳Proteinase K孵育时长。
4. 将通透后的样本浸入1×PBS漂洗3次,每次5min。轻柔地去掉多余液体,并用吸水纸小心吸干载玻片上样本周围的液体。在实验过程中,切勿让样本干燥。处理好的样本需放入湿盒中保持湿润。
◆标记及检测
1. 分组设置
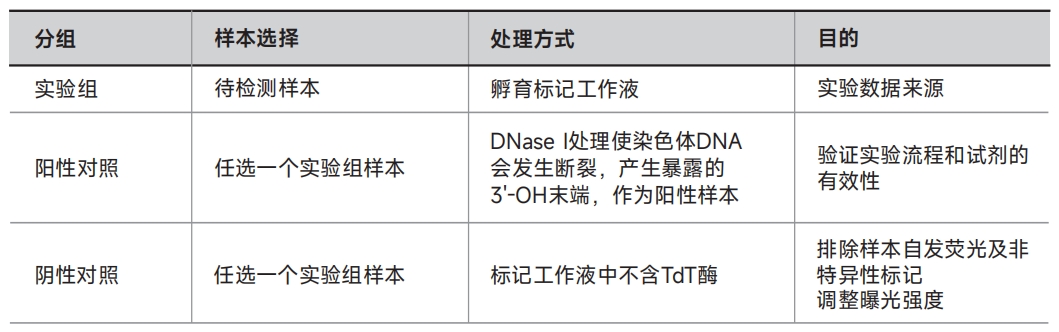
制备阳性对照
(1)用去离子水按 1:10 的比例稀释 DNase I Buffer (10×) < 例如:每个样本需使用 200 µL 1×DNase I Buffer,即用 20 µL DNase I Buffer (10×) 和 180 µL 去离子水混合稀释 >,取其中100 µL 滴加到已通透的样本上 ( 如果样本是悬浮细胞,需提前离心去除上清 ),室温孵育 5 min;
(2)配制 DNase I 工作液:向剩余的 100 μL 1×DNase I Buffer 中加 1 μL DNase I (0.5 mg/mL),使其浓度为 5 µg/mL,现配现用;
⑵注意:DNase I 会在剧烈混合下变性,建议不要涡旋 DNase I 溶液。
(3)用移液器轻轻吸除样本上的液体,加入 100 μL DNase I 工作液 (5 µg/mL),一定要覆盖住整个样本,常温孵育 10 min;
(4)将样本浸入1×PBS漂洗3次,每次5min。
⑵注意:阳性对照必须使用单独的染色缸,否则其上残留的DNase I可能会使实验组出现假阳性信号。
雅酶一步法TUNEL细胞凋亡检测试剂盒(FITC, 绿色荧光)
2. 按照下表配制标记工作液;
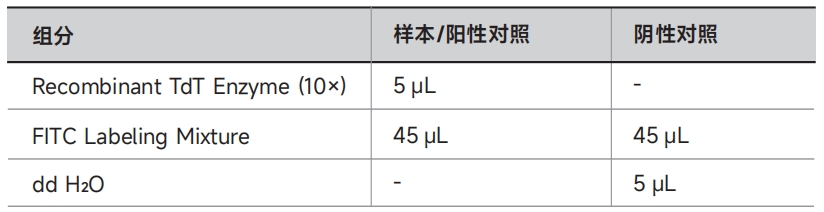
注意:(1)以上为单个样本所需标记工作液的用量,50μL×样本/对照数量即为所需标记工作液的总体积。
注意:(2)如果 TUNEL 反应过强造成荧光背景过高,可以用本试剂盒提供的 TdT Dilution Buffer 稀释 Recombinant TdT Enzyme (10×),即配制 TUNEL 检测液时,减少 Recombinant TdT Enzyme (10×) 的用量,用相应量的 TdT Dilution Buffer 补足。
雅酶一步法TUNEL细胞凋亡检测试剂盒(FITC, 绿色荧光)
3. 标记与检测
A.对于细胞爬片/涂片、石蜡切片或冰冻切片
⑴用吸水纸吸去预处理后的样本上多余的液体,若样本为 9 mm 细胞爬片或相似面积的其它样本,在其上滴加 50 μL 上步配制的标记工作液即可完全覆盖样本,若样本面积较大,可按比例增加标记工作液用量,保证工作液完全覆盖样本即可;
⑴注意:①请严格避免干片;
⑴注意:②请勿将吸水纸接触到细胞或者组织;
⑴注意:③滴加标记工作液后,样本需要避光处理。
⑵将封口膜剪成与组织或爬片同等大小,轻盖在样本上以保证试剂分布均匀,将样本置于湿盒内(湿盒的底部需铺上用水浸湿的纸巾),37℃避光孵育60min;
⑶轻柔地去掉样本上多余的液体,用1×PBS漂洗3次,每次5min;
⑴注意:为将游离的未反应标记物去除干净,样本在用1×PBS漂洗后,可用含0.1% Triton X-100和5mg/mL BSA的1×PBS再漂洗3次。
⑷用吸水纸轻柔地吸干样本周围多余的液体,并向样本区域滴加适量 抗荧光淬灭封片液 ( 例如 9 mm 细胞爬片需滴加 5 μL 抗荧光淬灭封片液 ),对样本进行封片,即可在荧光显微镜直接观察分析样本;
⑴注意:如需DAPI或PI复染,可在封片前加入用1×PBS配制的2μg/mL DAPI溶液或1μg/mL PI溶液,常温避光孵育5min。用1×PBS漂洗3次后再进行封片。
⑸立即在荧光显微镜下观察分析样本。
◇FITC 的激发波长范围覆盖 460~550 nm, 最大激发峰位于 494 nm 附近 ; 发射波长范围 集中在 520~530 nm, 最大发射峰约 525 nm;
◇DAPI与双链DNA结合时最大激发波长是358nm,最大发射波长是461nm;
◇PI与核酸结合时最大激发波长是535nm,最大发射波长是617nm。
雅酶一步法TUNEL细胞凋亡检测试剂盒(FITC, 绿色荧光)
B.对于悬浮细胞
⑴对于2×106个细胞的一个标准反应,所需标记工作液的用量是50μL。将预处理步骤准备好的2×106个通透后的细胞离心5min(300×g,4℃),弃上清,加入50μL标记工作液重悬细胞,37℃避光孵育60min,每隔15min轻弹管壁或用微量移液器轻轻重悬细胞;
⑵将标记后的细胞离心5min(300×g,4℃),弃上清,用 1×PBS 漂洗 3 次,每次 5 min;
⑶用 250~500 μL 1×PBS 重悬细胞;
⑷用流式细胞仪分析细胞或者涂片后在荧光显微镜下观察,参考前述激发 / 发射波长。
雅酶一步法TUNEL细胞凋亡检测试剂盒(FITC, 绿色荧光)
注意事项
1. 本说明书中推荐的实验条件是通用的,用户可根据不同的样本类型和预实验结果,对样本处理时间、试剂浓度等条件进行优化,以确定最适实验条件;
2. 产品组分避免反复冻融;
3. 为了您的安全和健康,请穿实验服并戴一次性手套操作;
4. 本产品仅限科研使用。
雅酶一步法TUNEL细胞凋亡检测试剂盒(FITC, 绿色荧光)
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验的细胞几乎没有DNA的断裂,因而没有3'-OH形成,很少能够被染色。由此,TUNEL成为了检测DNA片段化(细胞凋亡)的最常用方法。(以TUNEL法细胞凋亡检测试剂盒(增强型,绿色荧光)为例) TUNEL检测:使用20 U/ml Dnase处理Hela细胞10分钟。 二、TUNEL实验中关键步骤 1. 充分脱蜡和水化。脱蜡前可先将切片在 60ºC烤片 20 min,再使用二甲苯脱蜡2次,每次 5-10 min;而水化一般建议用梯度乙醇从高浓度到低浓度浸洗,便于后期试剂能充分、均匀的结合反应
Annexin V是一种钙离子依赖性磷脂结合蛋白,与磷脂酰丝氨酸PS有高度亲和力,可通过细胞外侧暴露的PS与凋亡早期细胞胞膜结合,将Annexin V标记上荧光染料利用流式细胞仪或荧光显微镜可检测细胞凋亡。 由于凋亡晚期或坏死细胞膜完整性丧失,细胞核染色液可进入细胞内染色细胞核,搭配Annexin V使用可将处于不同凋亡时期的细胞区分开。 A.悬浮细胞: 按照实验方案进行凋亡诱导,300 g离心5 min,弃上清,收集细胞,用PBS洗涤细胞一次,轻轻重悬浮细胞并计数。 取1~5 ×
产品名称:Annexin V-FITC & PI凋亡检测试剂盒英文名称:Annexin V-FITC & PI Apoptosis Detection Kit产品分类:细胞凋亡检测试剂盒[Apoptosis Assay Kit]产品编号:A0001c检验方法:Apoptosis包 装:20T产品说明:Annexin V-FITC & PI凋亡检测试剂盒 概述产品说明在正常细胞中,磷脂酰丝氨酸只分布在细胞膜脂质双层的内侧,细胞发生凋亡早期,膜磷脂酰丝氨酸(PS)由脂膜内侧翻向外侧。Annexin V