万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
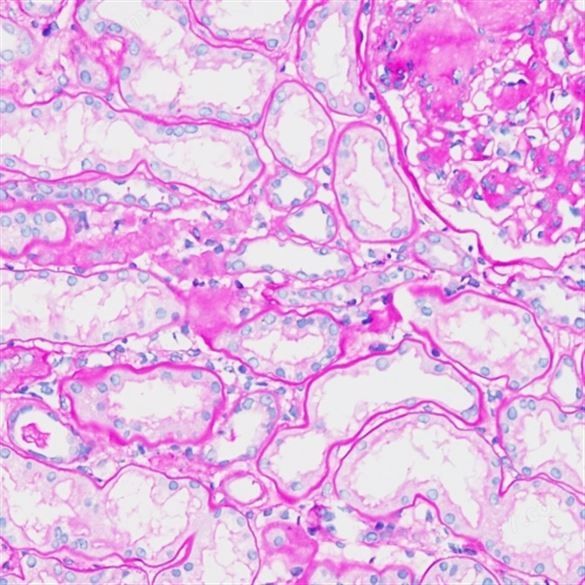
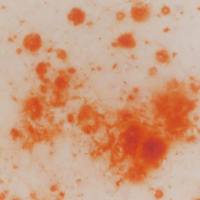
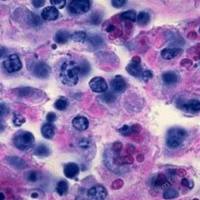
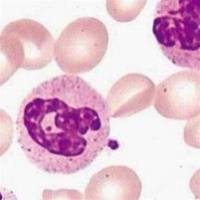
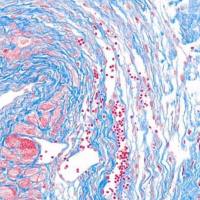
PAS糖原染色简介:
PAS染色又称过dian酸雪夫染色,糖原染色;一般用来显示糖原和其他多糖物质。还可以观察肾小球基底膜、结肠杯状细胞中性黏液物质、阿米巴滋养体和霉菌的着色。
PAS染色实验意义
随着医学实验技术的发展,糖原染色应用的范围更加广泛,如用以证明与鉴别细胞内空泡状的性质,心肌病变及其他心血管疾病的诊断,糖原累积病诊断和研究,糖尿病的诊断和研究,用于某些肿瘤的诊断等,为临床诊断、分类和治疗提供了重要的依据。
实验步骤:
(1)石蜡切片脱蜡至水(细胞涂片,冰冻切片直接水洗)。
(2)蒸馏水洗。
(3)过dian酸酒清夜10min。
(4)自来水冲洗10min。
(5)Schiff氏液10min。
(6)流水冲洗5min。
(7)用苏mu精染核3min(细胞核染色过深可用盐酸酒精分化)。
(8)流水冲洗5min。
(9)常规脱水透明、封固。
实验结果:
PAS阳性为红色;细胞核蓝色。
实验技巧:
( 1)试剂均应低温保存,临用前半小时取出恢复室温。
(2)过dian酸处理温度以不高于20C为宜,室温高时,处理时间可适当缩短。Schiff染液染色时间可随温度调整,室温高可减少染色时间,冬季室温低可延长至20分钟左右。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验用高碘酸氧化多糖时,醛基被游离出来,而显Schiff 阳性反应,这种 Schiff 反应称为 PAS ( Peri- odic Acid Schiff )反应。自 J.E.A.McManus ( 1946.1948 )、 R.D.Hotchkiss ( 1948 )以来,一直被用作为多糖的组织化学检测方法。将固定好的切片用水及酒精洗涤后以 0.5 % HIO 4处理,待充分洗去 HIO 4后,浸于 Schiff 试剂中,含多糖部位就被染成红色。此反应基于 1 , 2- 乙二醇
用 途 反应用来显示糖元和其它多糖物质操作步骤1、固定液用Carnoy液或75%酒精 Carnoy固定液: 纯酒精 60 ml 冰醋酸 10ml 氯仿 30ml2、染色液(1) 过碘酸酒清夜配法:过碘酸(HIO .2H O) 0.4g 95% 酒精 35ml M/5醋酸钠(2.72g+蒸馏水100ml) 5ml蒸馏水10ml保存于冰箱内,用棕色瓶,可用两周。(2) Schiff氏液:0.5克碱性品红加入100毫升蒸馏水中,时时摇动三角瓶5分钟,使之充分溶解.冷却至50℃后过滤,加入10
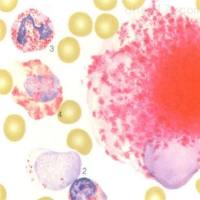
4. 标本运输:室温运输 5. 标本拒收的标准:溶血、稀释标本不能作测定 6. 试剂 6.1 试剂名称:血细胞PAS染色测定 6.2 试剂生产厂家:上海太阳生物技术公司 6.3 试剂组成 试剂1:PAS固定液,10%甲醛甲醇溶液。2℃-8℃避光保存,有效期六个月。 试剂2:PASⅠ液,10g/L(1%)过碘酸溶液。2℃
 技术资料
技术资料暂无技术资料 索取技术资料