万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 提供商:
舒桐科技
【舒桐科技已经成功进行以下菌株的基因编辑】
大肠杆菌、肺炎克雷伯菌、枯草芽孢杆菌、粪肠球菌、恶臭假单胞菌、金葡球菌、沙门氏菌、根瘤菌、咽峡炎链球菌、丝状真菌、酿酒酵母、毕赤酵母、乳酸乳球菌、M13噬菌体、T7噬菌体、金葡球菌噬菌体、肺炎克雷伯菌噬菌体、蓝藻、谷氨酸棒状杆菌等多种菌株。
【CRISPR微生物基因组改造】
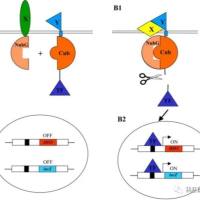
CRISPR序列由高度保守的重复序列(repeat)和间隔序列(spacer)组成。其中,间隔序列来源于外源基因。CRISPR序列附近还有一些相关基因,编码一系列Cas蛋白(核酸酶)。该系统最初是从细菌和古细菌中发现的一种适应性免疫系统,可以抵御病毒和质粒DNA的入侵。目前研究最广泛的是II型的CRISPR/Cas9系统,该系统包含两种重要组分:行使核酸内切酶功能的Cas9蛋白;具有导向功能的sgRNA(由tracrRNA和crRNA连接而成)。Cas9由1409个氨基酸组成,包含两个关键的核酸酶结构域(RuvC和HNH)。HNH结构域负责切割与其互补的DNA单链,切割位点位于PAM(protospacer adjacent motifs)序列上游3个核苷酸处。RuvC结构域则负责切割另一条DNA链,切割位点位于PAM序列上游3-8个核苷酸处。在此背景下,舒桐生物推出CRISPR/Cas9方法进行微生物的基因组改造,可在不同类型的细菌中定制化实现目标基因的敲除、大片段缺失、基因整合(过表达)等服务,保证交付阳性突变株。
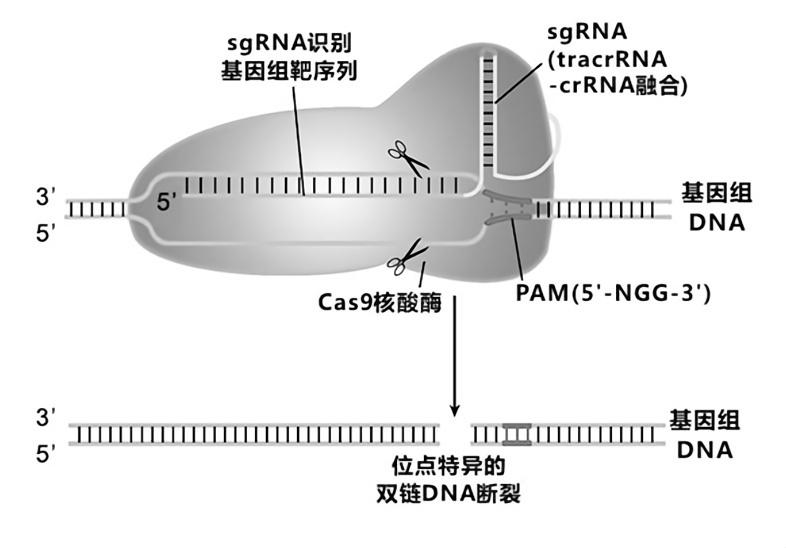
【微生物基因编辑定制服务】
舒桐科技提供多种微生物的编辑服务,针对特定的菌可以制定一对一方案,完美解决您的实验需求。
技术优势
a、高效定点切割:利用CRISPR/Cas9系统高效切割后的同源修补机制,对单位点的基因编辑效率可达90%以上;
b、复杂位点编辑:对于复杂且编辑困难的位点,引入λRed重组系统进一步提高CRISPR/Cas9切割后的同源修补效率;
c、碱基自由编辑:基于CRISPR/Cas9系统的碱基编辑和引导编辑可实现任意碱基的转换;
d、无痕编辑:靶位点编辑后不留任何抗性或重组位点,同时消除外源质粒;
e、操作简单:构建好CRISPR编辑质粒后通过电转的方法导入至目标菌体内进行基因编辑;
f、靶向性强:CRISPR技术具有靶向性强、脱靶率低等优势,可实现对目标位点的精准编辑;
g、适用范围广:可实现对多种细菌微生物的精准基因编辑服务。
【改造方案】
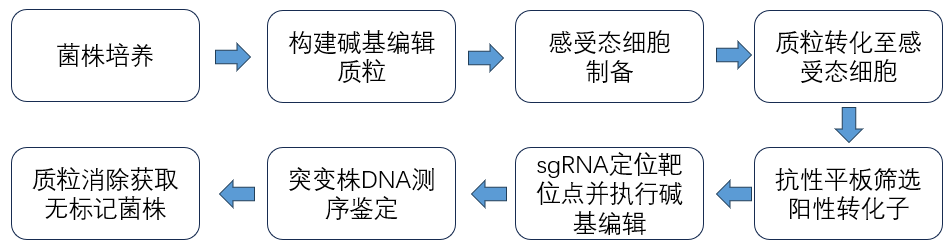
方案一:利用CRISPR/Cas9系统对微生物基因组的改造服务
与传统的λRed同源重组技术相比,CRISPR-Cas9系统可以实现无痕敲除且效率达到90%以上。此外,它可以同时进行多位点编辑,优势显著。
技术流程
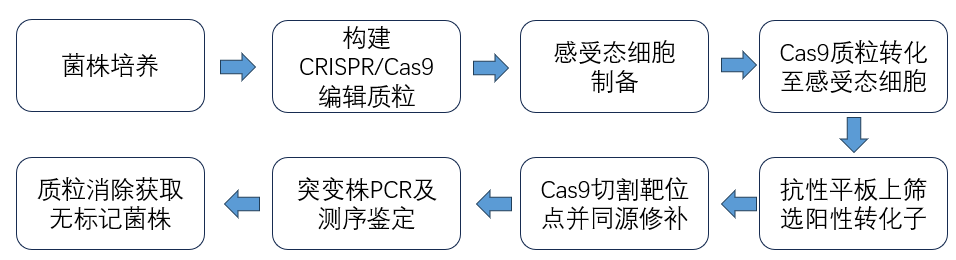
方案二:λRed介导的CRISPR/Cas9基因编辑服务
Red同源重组系统由λ噬菌体的3个基因exo、bet和gam组成,分别编码Exo、Beta和Gam蛋白,主要用于双链DNA同源重组。Exo蛋白单亚基分子量为 24 kD,具有双链核酸外切酶活性,可结合在双链DNA (dsDNA)末端,沿双链DNA的5′端向3′端降解DNA,产生3′突出端。Beta蛋白单亚基分子量为29 kD,是一种单链退火蛋白,在Red同源重组过程中起着决定性作用。Gam蛋白是Exo和Beta蛋白的功能辅助蛋白,可与RecBCD核酸外切酶和SbcCD核酸内切酶结合,分别形成RecBCD-Gam和SbcCD-Gam复合物,进而抑制RecBCD和SbcCD的活性,从而防止线性DNA被降解。针对复杂的编辑位点或自身同源重组能力弱的微生物,舒桐生物了推出λRed介导的CRISPR/Cas9基因编辑服务,通过将λ噬菌体的3个基因exo、bet和gam导入至目标菌株当中,提高菌株对Cas9造成的缺口的同源修补效率。
技术流程
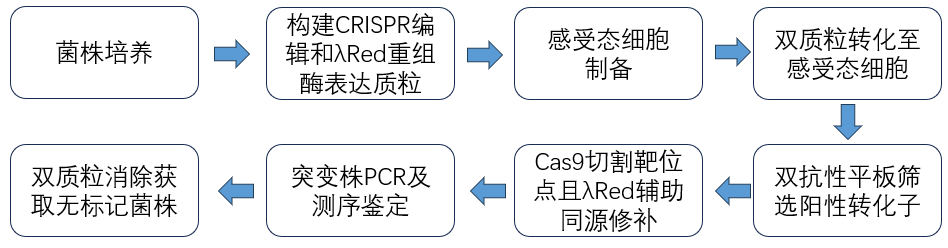
方案三:基于CRISPR/Cas9 的精准碱基编辑技术服务
当dCas9或Cas9n与DNA修饰酶融合表达时,可以在不产生DNA双链断裂的情况下实现单碱基水平碱基替换的工具,其在基础研究和基因治疗领域显示出了极大的潜力。碱基编辑器主要有3种类型:胞嘧啶碱基编辑器 cytosine base editor(CBE)、腺嘌呤碱基编辑器adenine base editor(ABE)和糖基化酶碱基编辑器glycosylase base editor(GBE),它们在不需要DNA双链断裂和编辑模板的情况下可分别实现C-to-T,A-to-G和C-to-G的碱基编辑。在此背景下,舒桐生物推出了基于CRISPR/Cas9 的精准碱基编辑技术服务,可以实现基因组靶位点的精准碱基编辑。
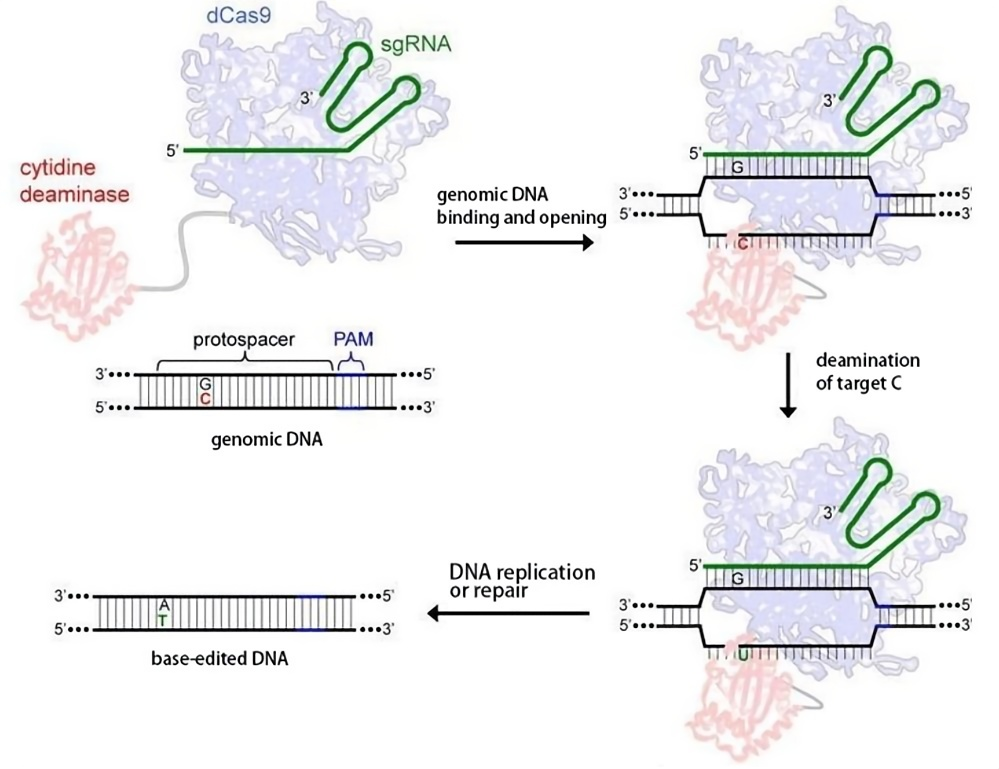
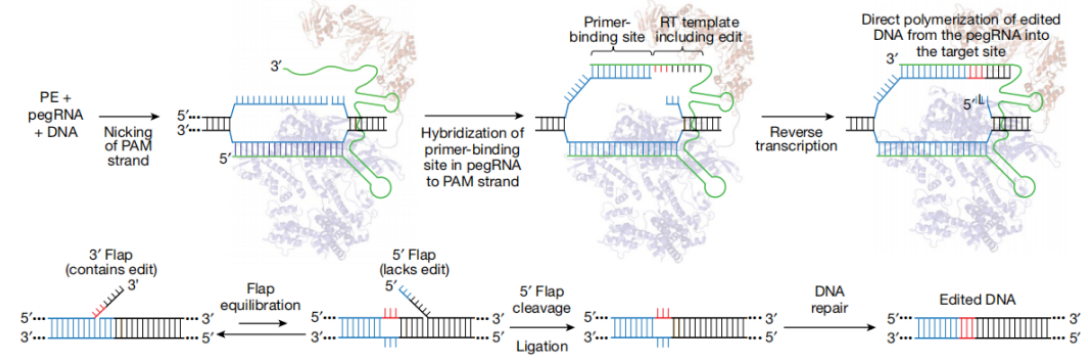
方案四:基于CRISPR/Cas9 的精准引导编辑技术服务
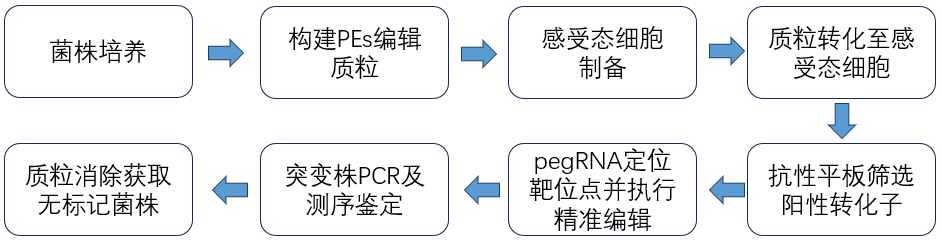
单碱基编辑只能实现特定碱基的转换,无法实现所有碱基的转换。而基于CRISPR系统开发的PEs编辑可有效实现所有12种单碱基的自由转换,而且还能有效实现片段的精准插入与删除。研究表明,该系统在人类细胞中可以引进12个点突变,实现范围是PAM上游3 bp到下游29 bp,插入达44 bp,缺失达80 bp,是目前生物医药领域强有力的研究工具。该技术使用与Cas9n 融合的逆转录酶和prime 编辑扩展的gRNA, 即引导编辑向导RNA (prime editing gRNA, pegRNA),这可使分子剪刀更加稳定和精确。该技术通过在sgRNA 的3′端引入引物结合位点序列(primer binding site, PBS)并将其与Cas9n 断裂的非靶标链结合,逆转录酶根据其携带的RT 模板逆转录出相应的含有目的突变的单链DNA,该细胞通过DNA 修复进一步将目的基因突变引入基因组。在此背景下,舒桐生物推出了基于CRISPR/Cas9 的精准引导编辑技术服务,该技术可以有效地产生精确的碱基置换、插入和缺失等变异,极大地扩大了基因组精准编辑的范围和能力。
技术流程
项目周期:2-3个月
交付标准
① 靶位点PCR及DNA测序鉴定数据
②工程菌株甘油管2支
③ mRNA转录水平数据——过表达
④项目结题报告
【Red/ET法微生物基因组改造】
大肠杆菌Rac原噬菌体上的操纵子recE/recT编码的蛋白能够高效地介导体内同源重组的发生,而且来源于大肠杆菌λ噬菌体的Redα/Redβ蛋白与RecE/RecT蛋白有类似的介导同源重组的功能,因此,Redα/Redβ和RecE/RecT重组酶体系合并命名为“Red/ET重组工程”。与体内自然发生的同源重组相比,Red/ET重组系统只需要40–50 bp的同源臂就能实现高效的同源重组,这一点突破了酶切位点和长片段PCR扩增的局限性对传统基因操作技术的限制,通过合成引物的方式将短同源臂加在PCR产物的两端,可以与任意位置的目标序列进行同源重组,同时Red/ET同源重组技术的操作过程在大肠杆菌中完成,极大缩短了构建载体和基因修饰的步骤与时间,基于此,舒桐科技推出Red/ET法进行微生物的基因组改造,可在不同类型的细菌中定制化实现目标基因的敲除、定点突变、基因敲入、过表达等服务。
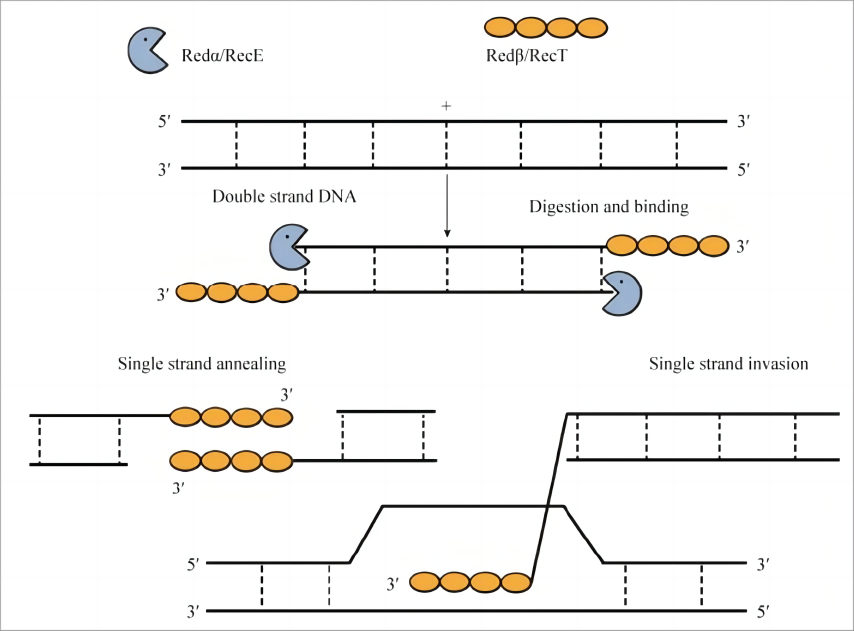
Red/ET法微生物基因编辑定制服务
舒桐生物提供多种微生物的编辑服务,微生物类型包括多种常见细菌,如大肠杆菌、沙门氏菌、农杆菌、分歧杆菌、芽孢杆菌、乳酸杆菌、假单胞杆菌、发光杆菌、伯克氏菌等等。
服务详情
a、无标记基因敲除:利用λRed重组系统实现高效基因敲除,并消除抗性基因;
b、定点突变:利用λRed重组系统实现高效基因点突变;
c、基因过表达:利用λRed重组系统实现基因组特点位点的基因过表达。
技术优势
a、操作简单,只需要40–50 bp的同源臂就能实现高效的同源重组;
b、适用范围广,可以在多种微生物中实现基因编辑;
c、无标记敲除,基因编辑后消除抗性基因。
技术流程
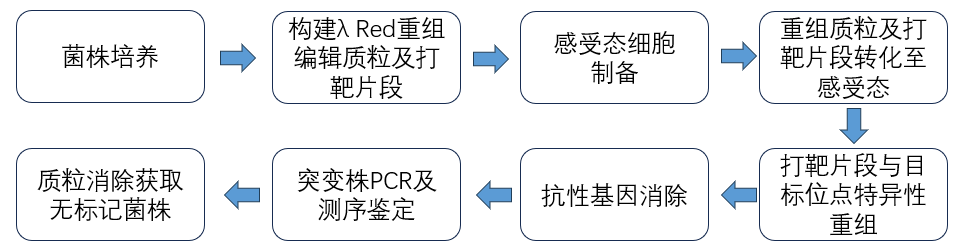
项目周期:2-3个月
交付标准
① 靶位点PCR及DNA测序鉴定数据
②工程菌株甘油管2支
③ mRNA转录水平数据——过表达
④项目结题报告
【案例展示】
(一):粪肠球菌-外源大片段插入
舒桐科技研发团队针对粪肠球菌特性,开发了其SpCas9编辑体系。我们实现了粪肠球菌基因组的外源大片段的插入,1500-3000bp,编辑效率为50%;且该外源大片段包含mCherry序列,使得被编辑菌株能发红色荧光。
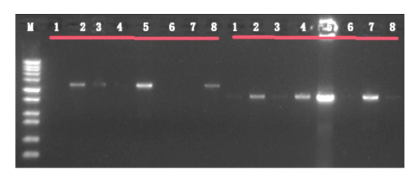
图注. 粪肠球菌基因插入的基因组PCR验证电泳图

图注. 基因编辑后粪肠球菌的荧光显微图像
同样,我们也实现了粪肠球菌的基因的大片段删除,效率为80%。
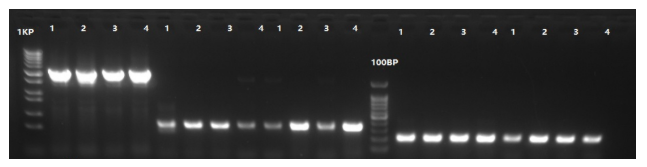
图注. 粪肠球菌基因大片段删除PCR验证电泳图
(二):金葡菌USA300-敲除基因
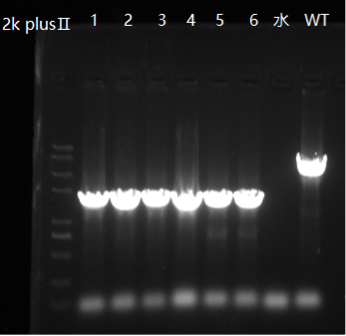
图注. 金葡菌基因敲除PCR验证电泳图
测序最终确认对PCR阳性克隆进行DNA测序,结果准确显示靶基因序列已被成功删除,无移码突变,证明基因敲除圆满成功。
图注. 金葡菌基因敲除DNA测序结果
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验Cell:诺奖得主新作!在大量病毒中发现微型 CRISPR 系统,可高效编辑人类和植物基因组
背景介绍 2020 年,科学家 Emmanuelle Charpentier 和 Jennifer A. Doudna 因开发了用于基因组编辑的 CRISPR 技术而摘得诺贝尔化学奖的桂冠。目前,基于 CRISPR-Cas9 基因编辑的多项临床实验也已启动并获得突破性结果,为许多遗传疾病的治疗开辟了新的途径。 CRISPR/Cas 系统,是一种存在于原核生物中的获得性免疫系统,以消灭外来的质体或者噬菌体的入侵。CRISPR/Cas 系统为大多数的细菌和古生菌提供了适应性免疫
诺奖得主 Jennifer 最新研究:CRISPR/Cas12c 无需切割 DNA 就可实现基因沉默,抵御病毒入侵
导读 CRISPR/Cas 系统为细菌提供了适应性免疫,同时其准确识别和切割特定 DNA 和 RNA 序列的能力也为植物、动物和微生物基因组编辑提供了强大的工具。目前,基于 CRISPR-Cas9 基因编辑的多项临床实验也已启动并获得突破性结果,为许多遗传疾病的治疗开辟了新的途径。 德国马克斯·普朗克病原学研究所的 Emmanuelle Charpentier 以及美国加州大学伯克利分校的 Jennifer A. Doudna 也因为开发了这一最重要的基因组编辑方法而摘得 2020 年
诺奖得主 Science 发文:基因编辑诞生 10 年,未来将如何改变世界?
Doudna(因 CRISPR 获诺贝尔化学奖)和她的同事们在 Science 发表了一项对细菌基因的研究结果。当时,它并没有引起学术圈的热点关注。十年以来,基因编辑领域的研究飞速发展,从基因编辑方法的创新、编辑精度及效率的改进,再到人类疾病的治疗以及农业研究的应用,基因编辑毫无疑问正在改变我们的生活。 2023 年 1 月 19 日,Joy Wang 和 Jennifer Doudna(因 CRISPR 获诺贝尔化学奖)在 Science 上发表了相关综述,重点介绍了过去十年里 CRISPR 基因
 技术资料
技术资料暂无技术资料 索取技术资料