相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 提供商:
北京恩泽 康泰生物科技有限公司
产品介绍
1、服务介绍
蛋白负载:通过内源改造的技术方式将目的蛋白装载至外泌体的膜内或膜外表面。
2、技术原理
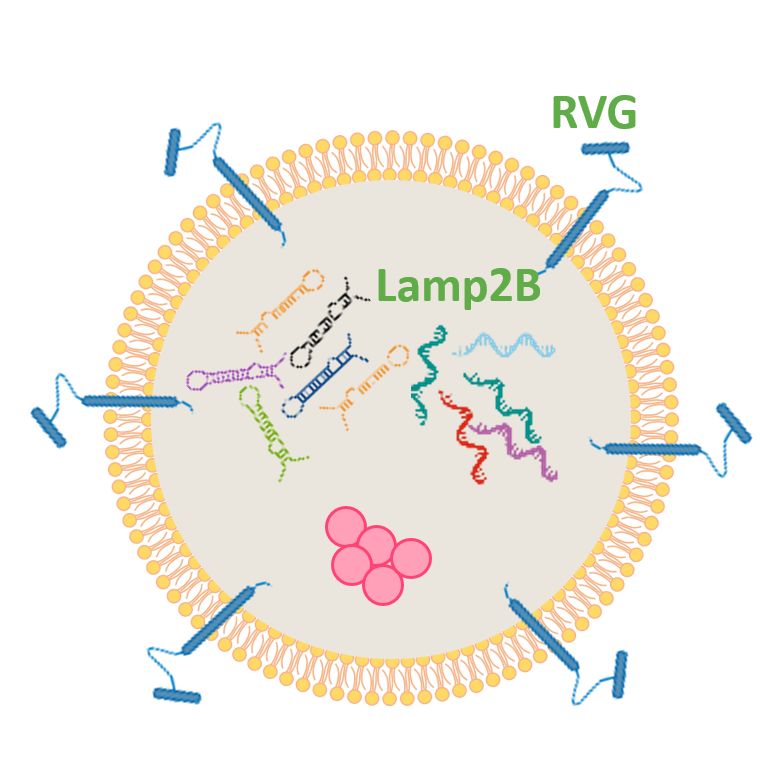
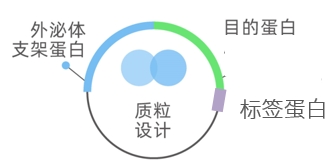
EVs支架是指能够将与之融合表达的目的蛋白携带至细胞外囊泡内或膜上的多肽/蛋白。
标签蛋白:与EVs支架和目的蛋白串联在一起构建融合表达质粒,方便表征目的蛋白是否表达在外泌体上。
利用外泌体支架蛋白的特异分选作用,通过内源改造技术将目的蛋白与支架蛋白融合表达质粒转入293F细胞,培养的上清分离纯化外泌体,最终实现目的蛋白在外泌体中的富集。
3、应用方向
-
类型装载-装载各种胞质蛋白,如各种酶类、功能性蛋白、RNA结合蛋白等
-
应用方向-酶&蛋白替代疗法、蛋白的功能研究

4、产品优势
-
技术成熟-采用成熟的技术,相关流程经过内部、外部验证,技术流程成熟,有项目经验
-
质控严格-从分子到细胞再到外泌体全流程质控,有明确的阳性、阴性对照,降低客户风险
-
效率更高-外泌体膜内蛋白工程化改造体系使得目的蛋白在外泌体中有更高的富集
-
周期更短-依据目的基因序列不同,最快30工作日便可获得快速验证数据
-
产量更高-基于我们的成熟体系,外泌体产量约5E+11到1E+12 Particle/L
5、项目流程

6、交付标准
1)质粒一代测序序列正确;
2)WB检测目的蛋白串联的标签蛋白,表达阳性。
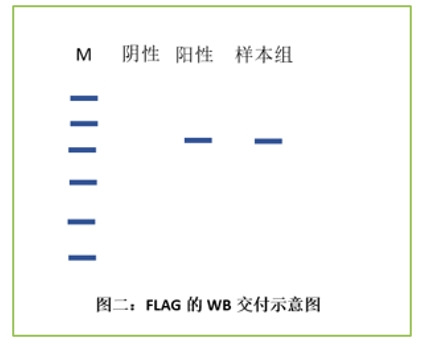
7、项目周期

8、demo展示
- 内载eGFP蛋白
常规eGFP过表达质粒转染母细胞后可以少量进入到外泌体中,但仍然主要存在于细胞中,外泌体中的表达量是细胞的1/2。用我们的内载体系,eGFP蛋白主要富集到外泌体中,细胞中存留的量较少,外泌体中的表达量是细胞的3.5倍。因此利用我们的内载体系可以在原有基础上提高7倍的外泌体富集。
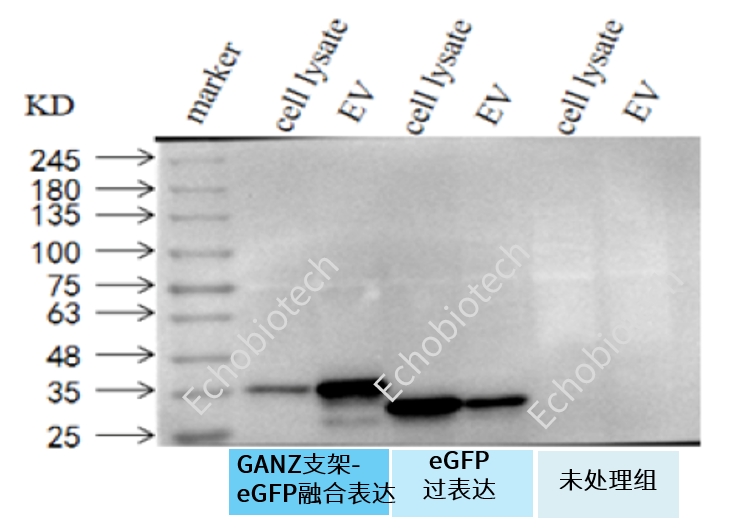
内载eGFP蛋白
- 内载荧光素酶蛋白
内载的荧光素酶蛋白Nanoluc可以实现目的蛋白在外泌体中的分选,并且保持其正常的生物学功能;此外,当EV膜完整时,蛋白酶K无法消化荧光素酶;EV裂解后,腔内释放出来的荧光素酶被蛋白酶K消化,无法与底物反应。证实了Nanoluc蛋白确实表达在外泌体胞内,而非以游离的形式或展示在外泌体膜外。
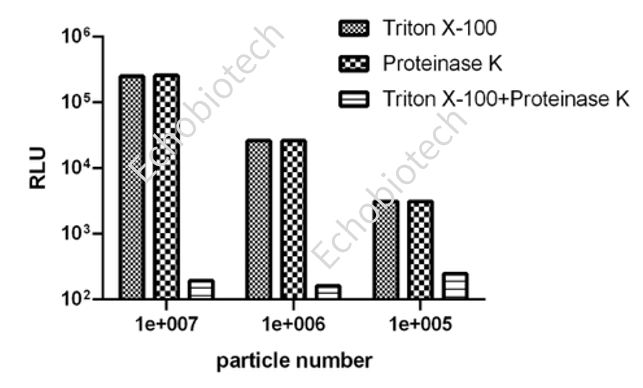
内载荧光素酶Nanoluc蛋白
- 内载RNA结合蛋白
内载的RNA结合蛋白L7Ae更多富集至外泌体中。利用L7Ae的分拣作用实现拣目的mRNA在外泌体中的有效装载,证明内载的L7Ae蛋白是有功能活性的。
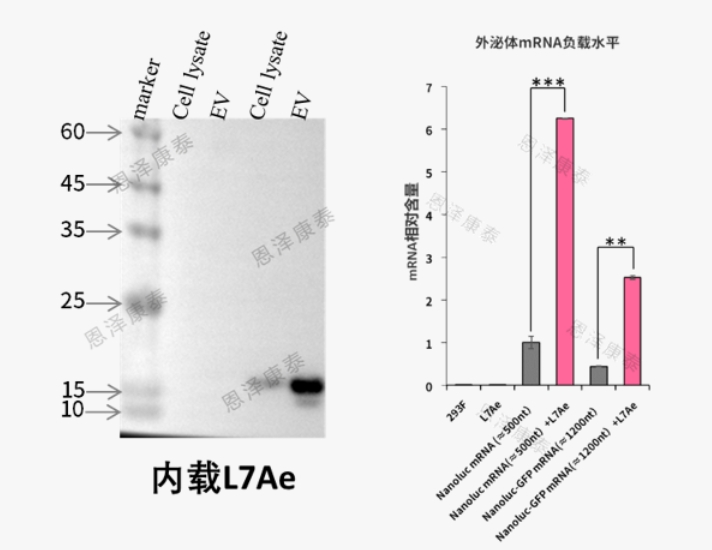
内载RNA结合蛋白L7Ae
经典案例
内载蛋白治疗肾缺血再灌注损伤
发表期刊:Kidney Int.
发表年份:2021年
影响因子:19.00
-
英文标题
Exosome-based delivery of super-repressor IκBα ameliorates kidney ischemia-reperfusion injury
-
中文标题
外泌体递送超抑制因子IκBα可改善肾缺血再灌注损伤
-
研究摘要
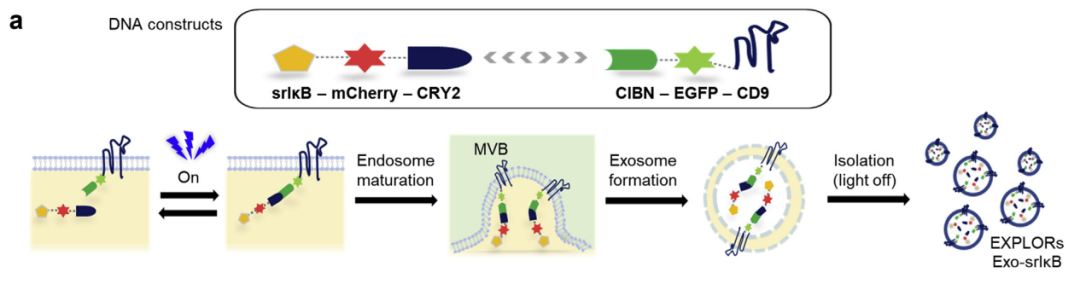
缺血再灌注损伤是急性肾损伤的主要原因。近年来对缺血再灌注急性肾损伤病理生理学的研究表明,免疫反应显著影响肾缺血再灌注损伤和修复。核因子(NF)-ĸB信号通路可以控制细胞因子的产生和细胞存活,在缺血再灌注诱导的急性肾损伤中起重要作用,(NF)-ĸB的抑制可改善缺血性急性肾损伤。利用一种新型的光基因工程外泌体技术EXPLOR,成功地在外泌体中装载了NF-ĸB超级抑制剂srIĸB(Exo-srIĸB)。在肾缺血再灌注手术前、手术后将Exo-srIĸB注入B6野生型小鼠体内,其结果与外泌体注射组(Exo-Naïve)进行了比较。缺血后小鼠在Exo-srIĸB治疗中的血清尿素氮、肌酐和中性粒细胞明胶酶相关脂钙蛋白水平低于Exo-Naïve治疗组。全身递送Exo-srIĸB可降低缺血后肾脏NF-ĸB活性并减少细胞凋亡。与对照组相比,缺血后肾脏的促炎细胞因子和粘附分子的基因表达在Exo-srIĸB治疗组中有所下降。活体成像证实了嗜中性粒细胞和巨噬细胞摄取了外泌体。Exo-srIĸB治疗也显著影响缺血后肾免疫细胞群,与对照组相比,中性粒细胞、单核/巨噬细胞和T细胞频率降低。因此,通过外泌体递送调节NF-ĸB信号可以作为一种新的治疗缺血再灌注引起的急性肾损伤的方法。
内载功能性蛋白治疗溶酶体贮积病LSD
发表期刊:J Extracell Vesicles
发表年份:2021年
影响因子:17.34
-
英文标题
Extracellular vesicles from recombinant cell factories improve the activity and efficacy of enzymes defective in lysosomal storage disorders
-
中文标题
重组细胞工厂来源的细胞外囊泡提高了溶酶体储存障碍中缺陷酶的活性和功效
-
研究摘要
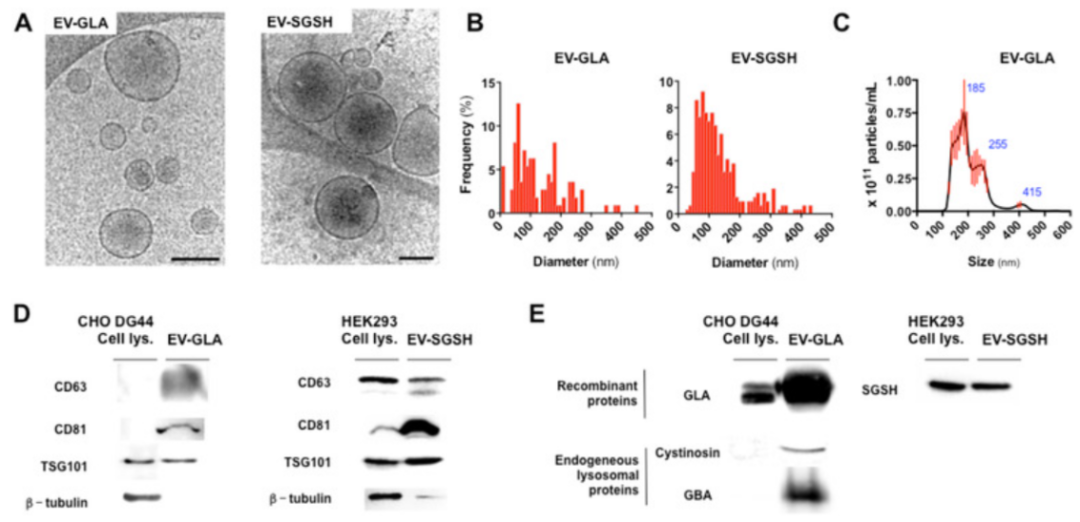
本研究探讨了细胞外囊泡(EVs)作为溶酶体贮积症中递送治疗性酶的载体。α -半乳糖苷酶A (GLA)和n -SGSH,两种酶分别在Fabry病和Sanfilippo A病中存在缺陷,从过表达这两种酶的哺乳动物细胞中分离出EVs。从细胞上清液中直接纯化EV是获得高活性GLA和SGSH蛋白的一种简单有效的方法,即使在EV冻干后也是如此。同样,在Fabry病的细胞模型中,携带GLA的EV (EV-GLA)被迅速吸收并到达溶酶体,这种递送方式比临床中使用的重组酶能够更有效地恢复溶酶体功能。在体内,EV具有良好的耐受性,分布在包括脑在内的所有主要器官中。在动脉内(颈内动脉)或静脉内(尾静脉)给药1小时后,DIR标记的EV定位于脑实质中。此外,单次静脉给药EV-GLA能够降低临床相关组织(如肾脏和脑)中globotriaosylceramide (Gb3)底物水平。总的来说,这项研究结果表明,来自过表达溶酶体酶的细胞的EV作为天然蛋白质递送系统,提高了重组蛋白的活性和功效,并促进了它们进入被传统酶替代疗法忽视的器官。
内载RNA结合蛋白靶向降解溶酶体中特定RNA
发表期刊:J Extracell Vesicles
发表年份:2021年
影响因子:17.34
-
英文标题
Fusion protein engineered exosomes for targeted degradation of specific RNAs in lysosomes: a proof-of-concept study
-
中文标题
融合蛋白工程化的外泌体靶向降解溶酶体中的特定RNA:一项概念验证研究
-
研究摘要
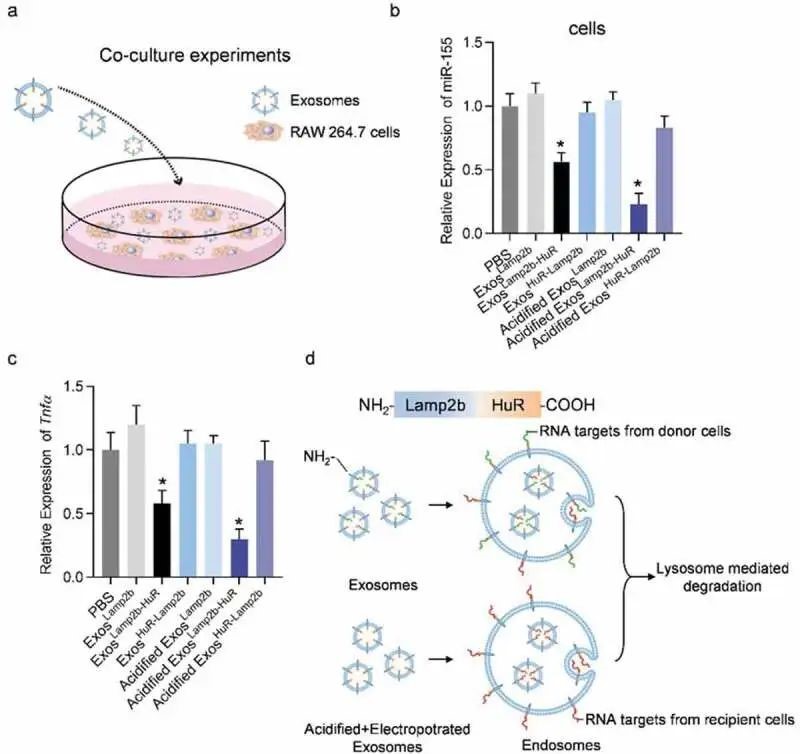
在治疗上想干预RNA在体内的功能仍然是一个巨大的挑战。本研究开发了一种基于外泌体的策略来递送工程化的RNA结合蛋白,目的是将特定的RNA招募到溶酶体中进行降解。作为一项原理验证性研究,RNA结合蛋白HuR被融合到Lam2b的c端,Lam2b是一种定位于外泌体和溶酶体的膜蛋白。通过这种方式可以将融合蛋白分选到外泌体中。此外,用Lamp2b-HuR修饰的外泌体可能通过溶酶体介导的降解成功地降低了目标RNA的丰度,特别是当外泌体被酸化时。该系统在巨噬细胞中特别有效,巨噬细胞富含溶酶体,对常规转染介导的RNAi策略具有抗性。在CCl4诱导的肝损伤小鼠模型中,研究者发现用Lamp2b-HuR工程化的酸化外泌体的递送可以显著减少肝纤维化,同时降低miR-155和其他炎症基因。利用这种基于外泌体的RNA结合蛋白递送策略,即“外泌体介导的溶酶体清除”,利用了外泌体靶向递送的优势,在体内调控系列基因方面具有很大的前景。
内载蛋白治疗败血症相关器官损伤
发表期刊:Sci Adv.
发表年份:2020年
影响因子:14.97
-
英文标题
Exosome-based delivery of super-repressor IκBα relieves sepsis-associated organ damage and mortality
-
中文标题
基于外泌体的超抑制因子IκBα递送减轻败血症相关器官损伤和死亡率
-
研究摘要
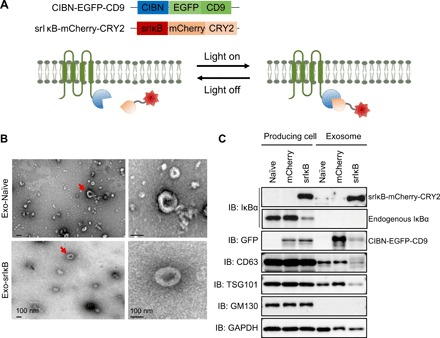
细胞外囊泡通过将细胞物质转移到受体细胞,在细胞间通讯中发挥积极作用,外泌体作为一种天然的治疗药物递送载体,具有很大的潜力。多种疾病模型中的炎症反应可通过引入超抑制因子IκB (srIκB)来降低炎症反应,srIκB是IκBα的主要活性形式,可抑制核因子κB向细胞核的易位。该研究团队之前开发的光基因工程外泌体系统(EXPLOR)可将大量的srIκB装载到外泌体中。作者发现,在脓毒症小鼠模型中,腹腔注射装载了srIκB的外泌体(Exo-srIκBs)可以降低死亡率和全身炎症。在生物分布研究中,发现Exo-srIκBs主要存在于小鼠的中性粒细胞中,少量存在于小鼠的脾脏和肝脏的单核细胞中。此外,研究还发现Exo-srIκB减轻单核THP-1细胞和人脐静脉内皮细胞的炎症反应。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
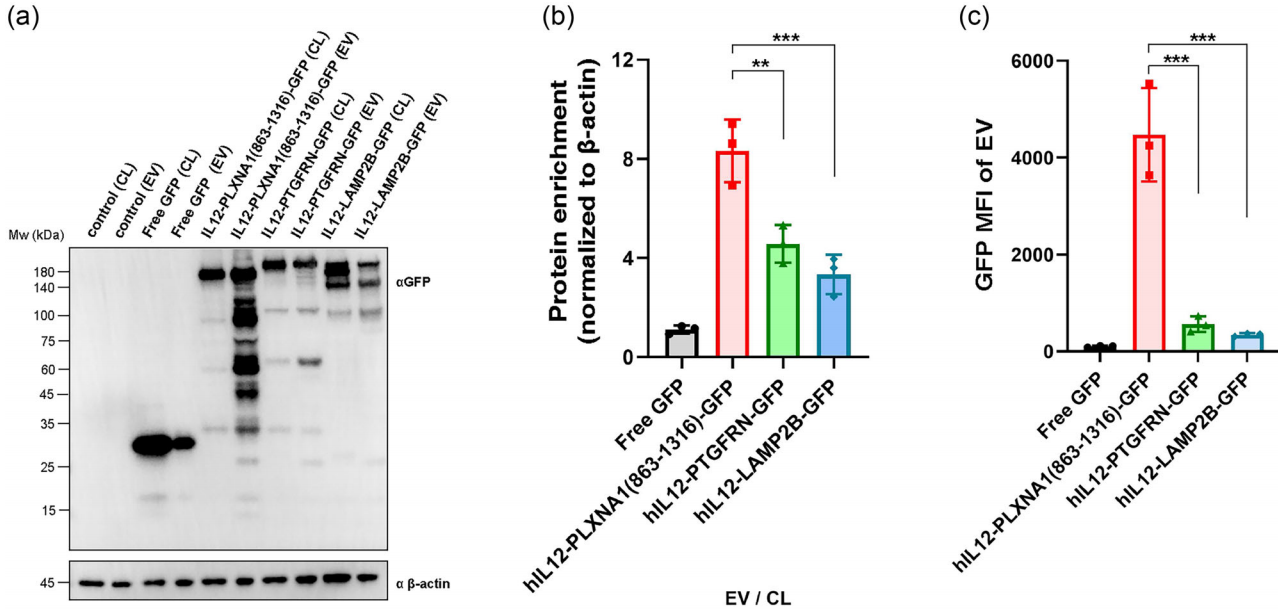
文献和实验1、Zhao H, Li Z, Liu D, et al. PlexinA1 (PLXNA1) as a novel scaffold protein for the engineering of extracellular vesicles. J Extracell Vesicles. 2024;13(11):e70012. IF 14.5 1区
恩泽康泰EVs外载专利支架蛋白PLXNA1发表文献
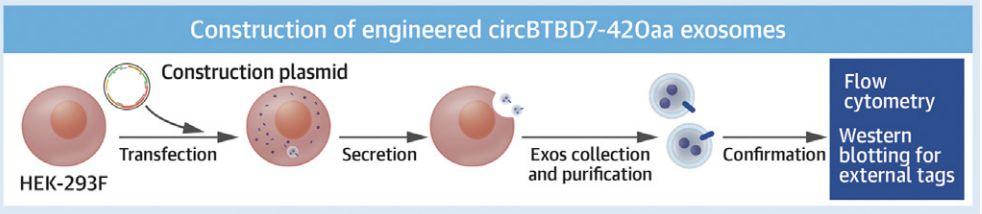
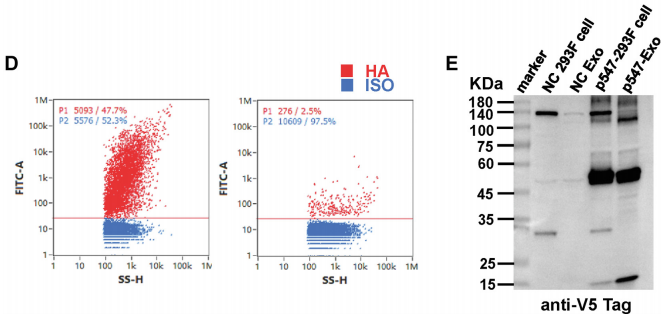
2、Gan X, Chi B, Zhang X, et al. CircBTBD7-420aa Encoded by hsa_circ_0000563 Regulates the Progression of Atherosclerosis and Construction of circBTBD7-420aa Engineered Exosomes. JACC Basic Transl Sci. 2025;10(2):131-147. IF=7.2 1区 293F EVs外载动脉粥样硬化靶向肽+内载CircBTBD7-420aa多肽
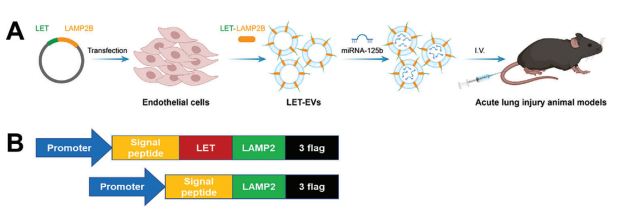
3、Gu Z, Sun M, Liu J, et al. Endothelium-Derived Engineered Extracellular Vesicles Protect the Pulmonary Endothelial Barrier in Acute Lung Injury. Adv Sci (Weinh). 2024;11(6):e2306156. IF=14.1 1区 lamp2b-肺微血管内皮细胞靶向肽融合质粒构建、包装慢病毒

 技术资料
技术资料暂无技术资料 索取技术资料