相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
产品编号:C001396
品系背景:C57BL/6J
繁殖:纯合×纯合
品系描述
视网膜色素变性(Retinitis Pigmentosa, RP)是一种遗传性视网膜疾病,全球患病率约为1:5000-1:3000。RP具有很大的临床和遗传异质性,视紫红质基因(Rhodopsin, RHO)突变导致约25%的显性RP[1]。RHO编码的视紫红蛋白对于光信号传导至关重要,大多数RHO突变导致紫红蛋白在感光细胞中高水平表达,使得大量的突变蛋白在细胞中定位异常并聚集,造成感光细胞凋亡,不能行使正常的光信号传导功能。此外,RHO基因的突变也与先天性静止性夜盲(CSNB)有关。目前靶向RHO基因以治疗视网膜色素变性的基因疗法有ASO、CRISPR等,全人源化动物模型的应用有助于推动RHO相关潜在疗法向临床试验进一步转化。
本模型为小鼠Rho基因人源化模型,利用基因编辑技术将小鼠内源性Rho基因替换为对应的人源RHO基因片段,以在小鼠体内表达人源的视紫红蛋白。在该模型中,小鼠Rho基因被人源RHO基因取代,人源基因编码的蛋白在小鼠体内正常表达,因此该模型的视网膜外形和功能和野生型小鼠相同,不存在视觉缺陷。该模型可用于视觉信号传导和视网膜色素变性的研究。此外,基于自主研发的TurboKnockout融合BAC重组的技术创新,赛业生物还可提供基于该模型构建的热门点突变疾病模型,也可针对不同点突变提供定制服务,以满足广大研发人员关于视网膜色素变性的药效学等实验需求。
构建方式
利用胚胎干细胞(ES)基因编辑打靶技术,将C57BL/6J小鼠的Rho基因ATG启动子至下游500bp片段替换为人源RHO基因ATG启动子至下游500bp片段。
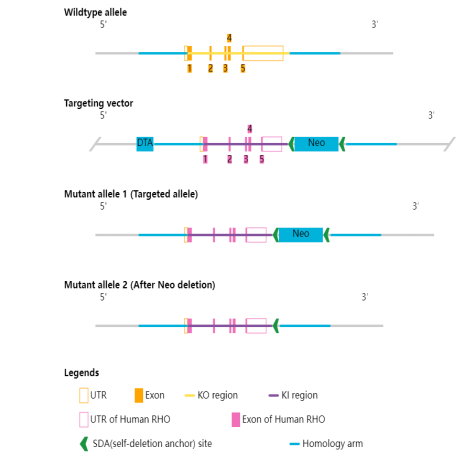
研究应用
视网膜色素变性(RP)研究;先天性静止性夜盲症(CSNB)研究;其它视网膜疾病研究。
模型验证
- B6-hRho小鼠成功表达人源RHO基因

图1. B6-hRho小鼠和野生型小鼠中人源RHO基因表达的检测。利用人源基因的qPCR引物检测小鼠体内人RHO基因的表达,检测结果显示与野生型对照组(B6J)相比,B6-hRho小鼠成功在体内表达人源RHO基因。
- B6-hRho小鼠视网膜形态和视网膜血管正常
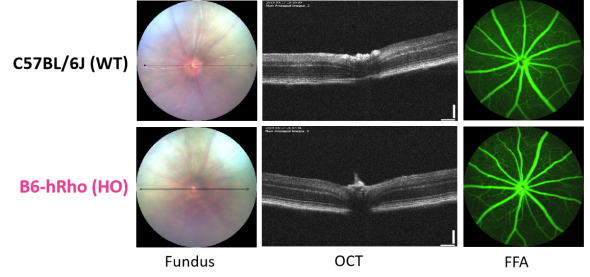
图2. 10周龄纯合B6-hRho小鼠和C57BL/6J野生型小鼠的眼底和视网膜形态检测。纯合B6-hRho在眼底形态(Fundus)、视网膜的光学相干断层扫描(OCT)和眼底荧光素血管造影(FFA)中的结果与野生型小鼠一致,表明B6-hRho小鼠的眼部和视网膜形态无明显变化,能够维持正常的视网膜血管和血液循环。(WT: wild-type, HO: homozygote)
- B6-hRho小鼠视网膜结构和视紫红蛋白蛋白表达正常
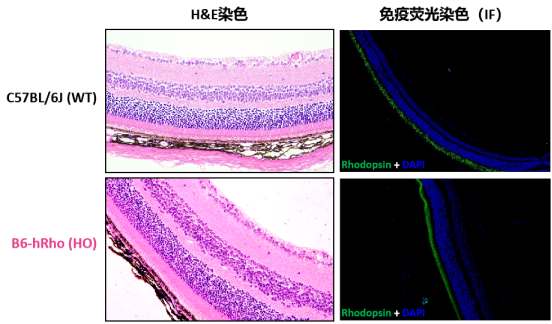
图3. 10周龄纯合B6-hRho小鼠和C57BL/6J野生型小鼠的视网膜结构和视紫红蛋白(Rhodopsin)表达检测。通过H&E染色和免疫荧光染色分别对B6-hRho小鼠和C57BL/6J野生型小鼠的视网膜结构和Rhodopsin蛋白进行检测,检测结果表明B6-hRho小鼠呈现正常的视网膜结构和蛋白表达。
- B6-hRho小鼠视网膜电图(ERG)正常

图4. 纯合B6-hRho小鼠和C57BL/6J野生型小鼠的视网膜电图(ERG)检测结果。纯合B6-hRho小鼠暗适应(Scotopic)和明适应(Photopic)ERG中a波和b波的振幅均与野生型几乎保持一致,表明该模型小鼠视网膜光感受功能正常。
- 结果讨论
通过qPCR、OCT、FFA、ERG、H&E染色和免疫荧光等多种实验技术对B6-hRho小鼠中RHO基因和蛋白表达、视网膜形态和视网膜功能进行检测,检测结果表明人源RHO基因在B6-hRho小鼠中成功表达且可以传导到蛋白水平,同时该小鼠维持正常的视网膜形态和功能。
综上,B6-hRho小鼠在RHO基因替换后,表型与野生型相比无异常,可用于后续视网膜色素变性(RP)和其它视网膜疾病的研究,为人类疾病的研究提供有效的工具。
- 基因基本信息
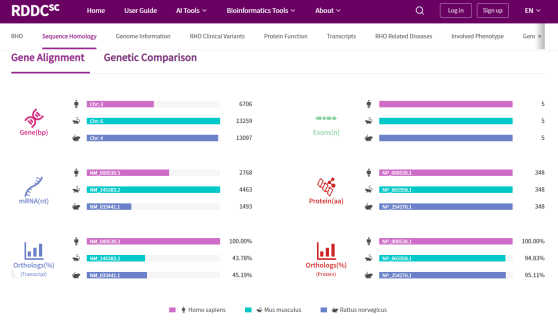
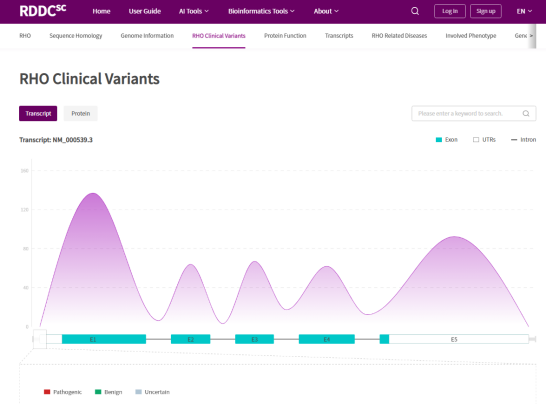
- 临床突变信息
知识拓展
人RHO基因位于5号染色体,编码的视紫红蛋白是第一个被鉴定的视网膜色素变性突变蛋白,它是一个位于视杆细胞外段中的G蛋白偶联受体,对于光信号传导至关重要,大多数RHO突变导致紫红蛋白在感光细胞中高水平表达,使得大量的突变蛋白在细胞中定位异常并聚集,造成感光细胞凋亡,不能行使正常的光信号传导功能。
目前有超过150个RHO基因突变被鉴定与显性RP相关,其中以错义突变为主。RHO基因突变在欧美人群尤其是美国人群中突变率最高,而在亚洲人群中突变率较低。P23H是第一个被发现的RHO基因突变,在美国患者中约占12%,而在其他国家人群患者中却很少发现[2]。RHO基因发生P23H突变导致蛋白不能正确折叠,造成内质网压力及细胞毒性,最终导致视杆细胞退化。视紫红质蛋白末端的347编码区则是另一个基因突变的热点,有6个不同的突变类型:P347T、P347A、P347S、P347Q、P347L、P347R,其中P347L最常见,在显性RP中突变率为3.6%,仅次于P23H,国内研究报道P347L是一个较常见突变位点[3]。关于非编码区功能,有文献报道在RHO的内含子中存在致病突变(g.3811A>G和g.5167G>T),且会导致Pre-mRNA剪切异常[4]。
目前靶向RHO基因治疗视网膜色素变性的基因疗法有ASO、CRISPR等,全人源化动物模型的应用有助于推动RHO相关的潜在治疗方法向临床试验进一步转化。ProQR公司的ASO药物QR-1123用于治疗与RHO(P23H)突变相关的显性RP的临床试验正在进行中(ClinicalTrials.gov标识符:NCT04123626),QR-1123通过抑制突变蛋白的产生治疗疾病,ProQR公司在研发中使用RHO(P23H)随机插入的转基因大鼠作为疾病模型[5]。张锋创立的Editas公布了其体内基因编辑疗法EDIT-103用于治疗由于RHO突变导致的RP[6]。EDIT-103是一种不依赖于突变的基于CRISPR/Cas9的基因编辑疗法,递送敲除和替换视紫红质基因中的突变双AAV5载体,以保持感光器功能,可通过视网膜下注射给药,该疗法有望解决150多种RHO突变导致的RP。CRISPR疗法的相关文献中使用到的动物模型包括P23H转基因小鼠、P347S转基因小鼠、hRHO(C110R/WT)人源化小鼠及同时具有多个突变的人源化小鼠模型等[7-10]。不难发现,CRISPR疗法中,疾病模型携带人突变基因是重要的共同因素,人源化疾病模型小鼠是CRISPR治疗走向临床前很好的验证模型。
综上所述,RHO基因是视网膜色素变性的重要致病基因,致病机理复杂,具有很大的临床和遗传异质性。突变中以错义突变为主,且部分致病突变位于内含子中,会导致剪切异常。目前已出现ASO、CRISPR、AAV多种基因疗法,研究者们会使用人源化小鼠开展药物临床前实验。赛业生物的RHO全人源化小鼠及在该人源化模型基础上构建的热门点突变疾病模型可以应用于RP基因治疗的临床前研究,针对不同点突变还可提供模型定制服务。
参考文献
[1]Hartong DT, Berson EL, Dryja TP. Retinitis pigmentosa. Lancet. 2006 Nov 18;368(9549):1795-809.
[2]Dryja T P, Mcgee T L, Reichel E, et al. A point mutation of the rhodopsin gene in one form of retinitispigmentosa[J]. Nature, 1990, 343(6256):364-366.
[3]Zhang X, Fu W, Pang C P, et al. Screening for point mutations in rhodopsin gene among one hundred Chinese patients with retinitis pigmentosa[J]. Chinese Journal of Medical Genetics, 2002, 19(6):463-466.
[4]Gamundi M J, Hernan I, Muntanyola M, et al. Transcriptional expression of cis-acting and trans-acting splicing mutations cause autosomal dominant retinitis pigmentosa[J]. Human Mutation, 2008.
[5]Biasutto P, Adamson P S, Dulla K, et al. Allele specific knock-down of human P23H rhodopsin mRNA and prevention of retinal degeneration in humanized P23H rhodopsin knock-in mouse, following treatment with an intravitreal GAPmer antisense oligonucleotide (QR-1123)[J]. Investigative ophthalmology & visual science, 2019(9):60.
[6]https://ir.editasmedicine.com/news-releases/news-release-details/editas-medicine-presents-preclinical-data-edit-103-rhodopsin-0
[7]Patrizi C, Llado M, Benati D, et al. Allele-specific editing ameliorates dominant retinitis pigmentosa in a transgenic mouse model[J]. The American Journal of Human Genetics, 2021, 108(2).
[8]Li P, Kleinstiver B P, Leon M Y, et al. Allele-Specific CRISPR-Cas9 Genome Editing of the Single-Base P23H Mutation for Rhodopsin-Associated Dominant Retinitis Pigmentosa[J]. Crispr Journal, 2018, 1(1):55-64.
[9]Xla B , Rja B, Xiang M, et al. Retinal degeneration in humanized mice expressing mutant rhodopsin under the control of the endogenous murine promoter. 2021.
[10]Wen-Hsuan Wu, Yi-Ting Tsai, -Wen Huang et al. CRISPR genome surgery in a novel humanized model for autosomal dominant retinitis pigmentosa. 2022.
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验外观:因为高脂饮食,毛发看起来有些「油腻」。 活动:因 DIO 的肥胖表型,多数小鼠看起来比较「慵懒」,不爱动。 脱毛:因 B6 品系的特性,容易出现理毛导致的脱毛,需关注是否有继发皮肤炎症反应。 运输应激:DIO 小鼠在经历运输后容易出现体重降低的情况。根据友商资料和我们的历史数据,运输后 DIO 平均体重减轻在 10%-15%。一般需要经过 2 周左右的适应性饲养,体重可以恢复到出库水平。 打架现象:因雄鼠的天性问题,可能会出现打架的情况,建议不要将不同笼小鼠进行混装。 B6 小鼠会
[4])。因此,Uox-KO 小鼠出生后需别嘌呤醇等药物维持生存。 Uox-KO 小鼠 品系全称:B6/JGpt-Uoxem3Cd3501/Gpt 品系编号:T011801 应用领域:高尿酸血症、痛风、尿酸肾病研究 Uox-KO 小鼠表型及药效验证 1. 雄鼠和雌鼠都自发出现高尿酸血症,雌鼠的平均尿酸水平较雄鼠低,但个体均一性较雄鼠好,别嘌呤醇可以显著改善因 Uox 敲除引起的小鼠高尿酸血症。 图 2. 图片来源:集萃药康 2. Uox-KO 雄鼠和雌鼠肌酐、尿素氮水平升高,提示出现肾损伤,且雄鼠肾脏损伤较雌鼠
是:某些基因突变导致的表型在不同的近交系中可能有所不同。● 常用的近交系小鼠有:1. C57BL/6JC57BL/6J 也叫 B6、B6J、Black 6 或 C57 Black,是使用最为广泛的近交系小鼠,也是第一个完成基因组测序的品系。来源:jax.orgC57BL/6J 近交系小鼠由 Clarence Cook Little 博士通过将 57 号雌鼠与 52 号雄鼠交配获得,毛色为黑色。自发肿瘤较少,乳腺肿瘤自发率很低;对放射物耐受力中等;补体活性高;抗听源性惊厥;骨密度较低;随年龄增长会发生听力
 技术资料
技术资料暂无技术资料 索取技术资料







