为什么要检测 MSI?——MSI 检测的 4 大临床意义

▊ 辅助诊断林奇综合征
林奇综合征曾被称作遗传性非息肉病性结直肠癌((Hereditary non-polyposis colorectal cancer,HNPCC),这是一种常染色体显性遗传肿瘤综合征,患者罹患结直肠癌或其他多个部位(包括子宫内膜、卵巢、胃、小肠、肝胆、上尿道、脑和皮肤等)的恶性肿瘤风险显著升高。林奇综合征约占所有结直肠癌患者的 2%-4%,是最常见的遗传性结直肠癌综合征。林奇综合征的主要致病因素是 MMR 基因(MLH1、 MSH2、MSH6 或 PMS2 基因)的致病性胚系突变或 EPCAM 基因缺失导致 MSH2 基因沉默。因此,MMR/MSI 的检测可以作为林奇综合征的初筛手段。对于经初筛确定的 dMMR/MSI-H 的患者,再考虑林奇综合征相关基因的胚系突变检测,以明确诊断。


▊ 判断预后
结直肠癌:
2000 年,Gryfe 等使用 2B3D NCI Panel 诊断方法对 607 例结直肠癌患者进行预后分析,发现 I-IV 期的 MSI-H 结直肠癌患者比 MSS 结直肠癌患者均有显著的生存优势 (HR = 0.42, 95%CI:0.27-0.67, P<0.001),且 MSI-H 患者具有较低的区域淋巴结转移率 (HR = 0.33, 95%CI:0.21-0.53,P<0.001) 和远处器官转移率(HR = 0.49,95%CI:0.27-0.89,P<0.02),该研究 首次提示 MSI-H 是结直肠癌的独立预后判断指标。一项纳入 32 个研究共 7642 例患者的 Meta 分析显示,相较于 MSS,MSI-H 是预后良好的独立预测指标,HR = 0.65(95%CI:0.5-0.71)。因此,dMMR/MSI-H 表型的结直肠癌虽然往往分化较差,但通常预后较好,目前公认 dMMR/MSI-H 是 II 期结直肠癌独立良好预后因子。在 II 期结直肠癌患者中,高危因素包括 T4、组织学分化差 (3/4 级,不包括 MSI-H 者)、脉管浸润、神经浸润、 术前肠梗阻或肿瘤部位穿孔、切缘阳性或情况不明、切缘安全距离不足、送检淋巴结不足 12 枚,而 dMMR/MSI-H 被认为是低危因素。
胃癌:
近期,一些研究表示,具有 MSI-H 表型的胃癌患者预后较好,也无法从辅助化疗中获益。Zhu 等在一项 Meta 分析中显示,MSI-H 的胃癌患者预后较好,且淋巴结转移少,肿瘤浸润浅,(HR = 0.63,95%CI:0.52-0.77)。基于此,《胃癌 CSCO 诊疗指南》(2019 版)中推荐 MSI/MMR 检测用于判断预后。

▊ 预测辅助化疗疗效
结直肠癌:
Ribic 等在一项回顾性研究中长期随访了 II/III 期结直肠癌,并首次提出 MSI 可能是辅助化疗的疗效预测指标,且 MSI-H 结直肠癌不能从 5-FU 化疗中获益。Sargent 等在一项研究中也得出了相似的结论,dMMR/MSI-H 结直肠癌患者不能从 5-FU 辅助化疗中获益,尤其在 II 期结直肠癌中,反而生存期缩短(HR = 2.3, 95%CI:0.84-6.24)。这些研究数据表明,II 期的 dMMR/MSI-H 型的结直肠癌患者不仅无法从 5-FU 单药辅助化疗中得到生存获益,反而是不利的。目前,国外的 NCCN 指南和国内的 CSCO 指南均指出,II 期的 dMMR/MSI-H 型的结直肠癌患者预后较好,不建议使用氟尿嘧啶类单药辅助治疗。
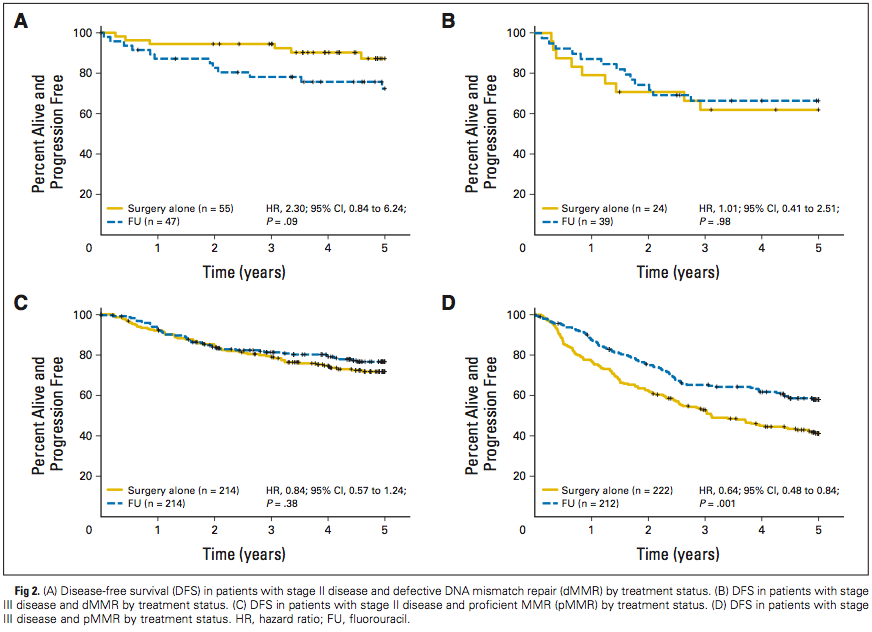
来源:Sargent et al., JCO, 2009
胃癌:
在胃癌中,MSI-H 也能够预测辅助化疗疗效。MAGIC 研究结果显示,仅接受手术治疗的患者中,dMMR/MSI-H 患者的 OS 未达到,而 pMMR/MSI-L/MSS 患者的 OS 为 20.5 个月(P 值 = 0.09),接受手术和化疗的患者中,dMMR/MSI-H 患者的 OS 为 9.6 个月,pMMR/MSI-L/MSS 患者的 OS 为 19.5 个月(P 值 = 0.03)。综上,dMMR/MSI-H 给仅手术治疗的患者带来阳性预测结果,而接受化疗的患者与阴性预测作用相关,因此,可手术的 dMMR/MSI-H 患者不能从围手术期化疗中获益。
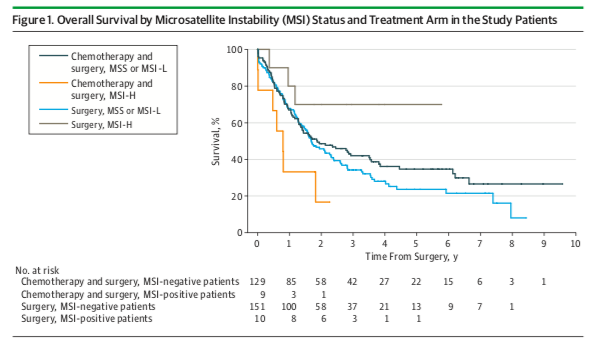
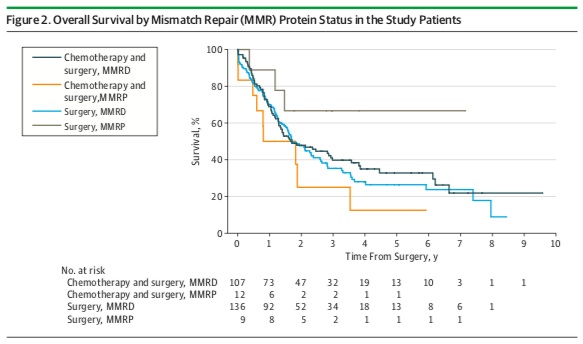
来源:Smyth et al., JAMA Oncol, 2017

▊ 指导免疫治疗疗效
Le 等于 2015 年首次报道了 dMMR/MSI-H 型的结直肠癌患者能够从帕博利珠单抗的治疗中获益,同时,发现 dMMR/MSI-H 型的其他癌种患者也能够从中获益。后续在更大样本量的研究中,帕博利珠单抗在 12 个癌种的 dMMR/MSI-H 患者中的疗效得到再次证实。这些研究表明,dMMR/MSI-H 患者能够从免疫检查点抑制剂中获益,且不限癌种。

来源:Le et al., Science, 2017
基于此,FDA 于 2017 年批准了帕博利珠单抗用于治疗 dMMR/MSI-H 型不可切除或转移性经治的实体瘤患者。紧接着,FDA 批准纳武利尤单抗单药或联合伊匹木单抗用于氟尿嘧啶、奥沙利铂和伊立替康治疗后出现进展的 dMMR 或 MSI-H 的转移性结直肠癌患者。由此,MSI 成为了所有实体瘤中免疫治疗疗效的预测因子,可见 MSI 的检测将在整个肿瘤领域越来越重要。
MSI-H 或 dMMR 型转移性结直肠癌的一线治疗标准方案长期以来仍以化疗为基础,但是患者预后较差。在 2020 年 ASCO 会议上,公布了 KEYNOTE-177 的研究结果,该研究是一项 III 期随机开放标签研究,探索了帕博利珠单抗对比标准治疗 (化疗±贝伐珠单抗或西妥昔单抗) 作为一线治疗在 MSI-H 型转移性结直肠癌患者中的疗效和安全性。主要研究重点为 PFS 和 OS,次要终点包括 ORR 和安全性。
研究结果显示,帕博利珠单抗组的中位 PFS 为 16.5 个月,化疗组的中位 PFS 为 8.2 个月,(HR = 0.60; 95%CI,0.45-0.80; P = 0.0002)。其中,帕博利珠单抗组 12 个月和 24 个月 PFS 率为 55.3% 和 48.3%,而化疗组分别为 37.3% 和 18.6%。帕博利珠单抗组和化疗组的 ORR 分别为 43.8% 和 33.1%。因此,相较于化疗,帕博利珠单抗作为 MSI-H/dMMR 转移性结直肠癌的一线治疗方案具有临床意义和统计学意义的 PFS 显著改善,且观察到的治疗相关不良事件更少。
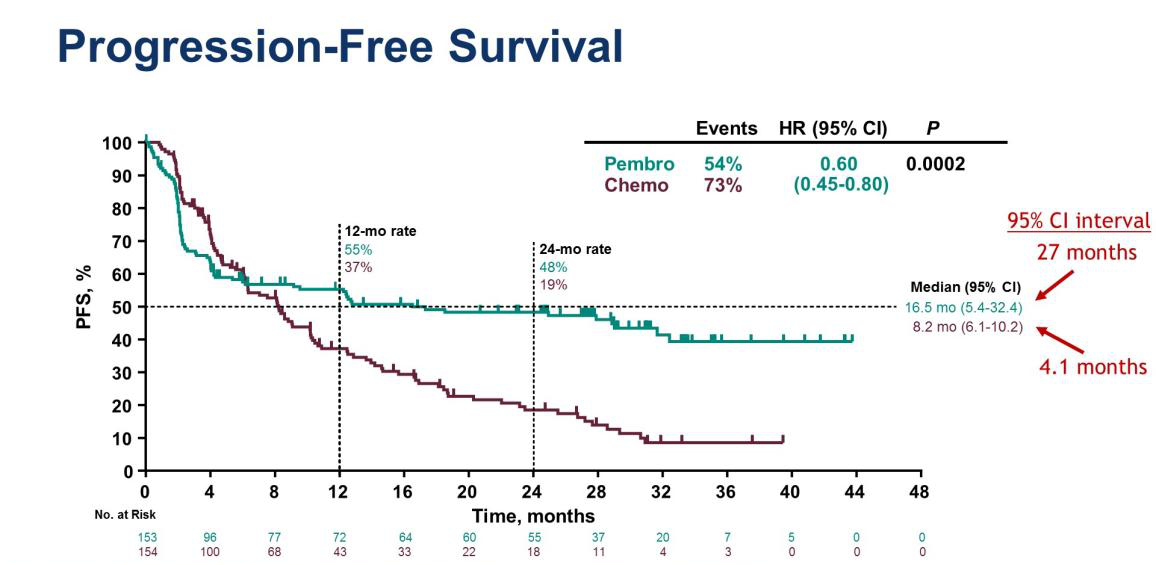
基于此研究结果,2020 年 6 月,FDA 批准帕博利珠单抗用于一线治疗 MSI-H/dMMR 的不可切除或转移性结直肠癌(mCRC)。此次获批,或将改变 MSI-H/dMMR 的不可切除或 mCRC 的一线治疗模式。
参考文献:
1. Christine M. Ribic, M.S., et al., Tumor Microsatellite-Instability Status as a Predictor of Benefit from Fluorouracil-Based Adjuvant Chemotherapy for Colon Cancer. n engl j med 2003. 349(3).
2. Le, D.T., et al., PD-1 Blockade in Tumors with Mismatch-Repair Deficiency. N Engl J Med, 2015. 372(26): p. 2509-20.
3. Gryfe, R., et al., Tumor Microsatellite Instability and Clinical Outcome in Young Patients with Colorectal Cancer. The New England Journal of Medicine, 2000. 342(2).
4. Popat, S., R. Hubner, and R.S. Houlston, Systematic review of microsatellite instability and colorectal cancer prognosis. J Clin Oncol, 2005. 23(3): p. 609-18.
5. Sargent, D.J., et al., Defective mismatch repair as a predictive marker for lack of efficacy of fluorouracil-based adjuvant therapy in colon cancer. J Clin Oncol, 2010. 28(20): p. 3219-26.
6. Le, D.T., et al., Mismatch repair deficiency predicts response of solid tumors to PD-1 blockade. Science, 2017. 357(6349): p. 409-413.


