| mRNA的COVID-19疫苗的成功,离不开几十年来对脂质载体给药系统的研究。该技术已被用于向目标细胞和组织传递各种生物活性分子,如小分子抑制剂和疫苗成分。脂质载体技术与传统的药物传递方式相比有很多优势,包括增加药物的稳定性、生物利用度和分布。
脂质纳米颗粒(Lipid nanoparticles,LNPs)是脂质载体给药系统中的重要技术之一,已成为基于寡核苷酸治疗药物的一个重要进展。封装在脂质纳米颗粒中的寡核苷酸在传递过程中受到保护,不受酶降解,并有效地传递到细胞中,在细胞中载体颗粒中的内容物被释放并被翻译为治疗蛋白。鉴于LNPs对基于寡核苷酸的治疗具有巨大的革命性潜力,新一波研究人员正在追求基于LNPs更有针对性的应用。
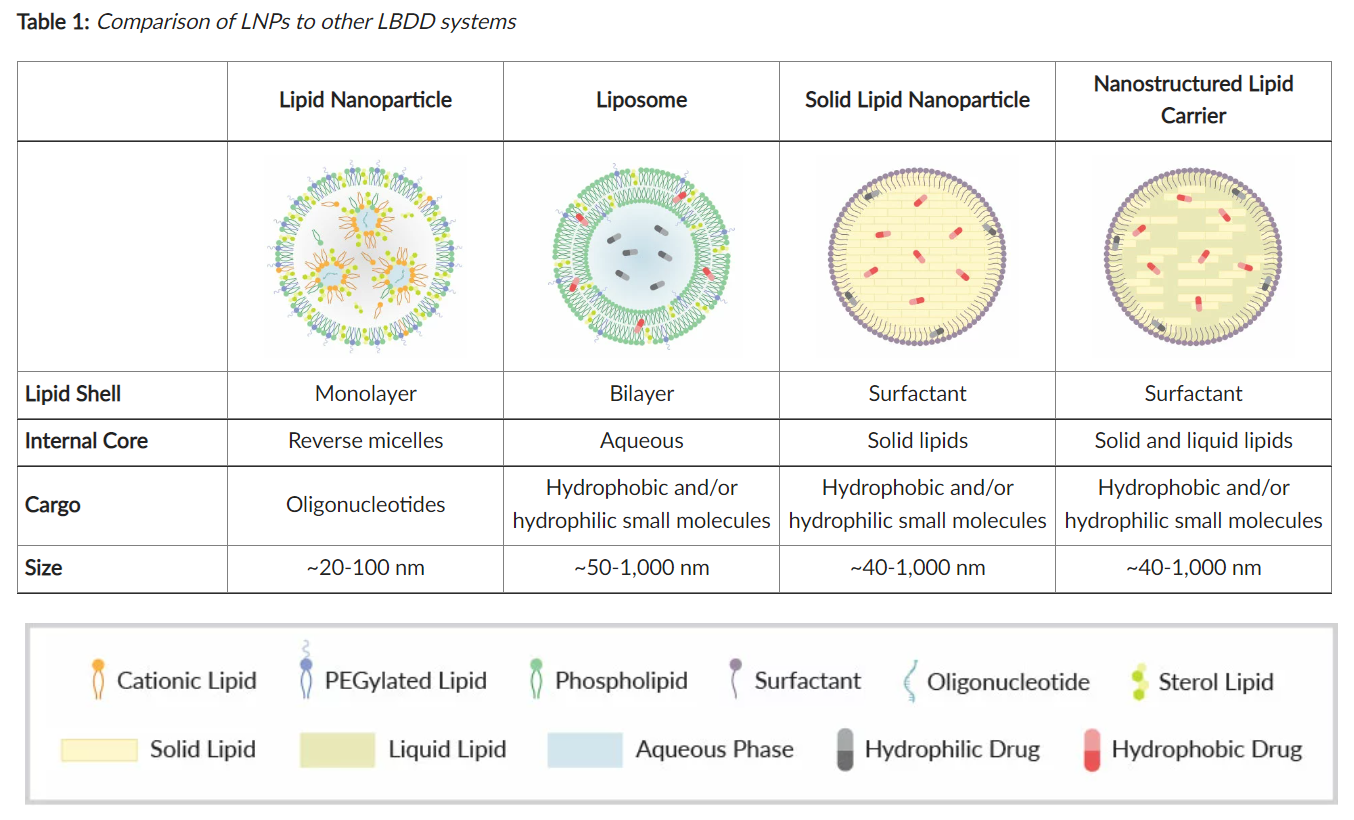
图1. 脂质纳米颗粒、脂质体、固体脂质纳米颗粒、纳米脂质载体结构上的区别。
表1.脂质纳米颗粒组成部分介绍:脂质纳米颗粒,通常由甘油磷脂、阳离子脂质、固醇脂质和包覆寡核苷酸的聚乙二醇化脂质组成(聚乙二醇化脂质属于亲水部分)。 LNPs中使用的许多相同的结构组件也是其他脂质载体给药系统技术(如脂质体、固体脂质纳米颗粒、纳米脂质载体)的组件。脂质和含有它们的分子,比如表面活性剂,可以用来调整脂质纳米颗粒的行为和性质。因此,在脂质纳米颗粒的构建中,结构组分的选择是重要的考虑因素。
纳米载体内容药物
LNPs更适合做为寡核苷酸药物的包封,而其他脂质载体给药的系统更适合于小分子抑制剂或脂类。针对不同应用所需的脂质载体给药技术取决于,脂质系统内部携带的药物。药物在脂质载体粒子中的定位则取决于其物理化学性质,下面就介绍一下几种不同的药物
· 寡核苷酸
mRNA、siRNA和pDNA是常见的寡核苷酸内容药物。寡核苷酸带负电荷,最好使用可电离的阳离子脂质封装在LNPs中。 含有mRNA的LNPs是几种COVID-19疫苗的基础,含有转甲状腺素靶向siRNA的LNPs已被开发用于治疗遗传性淀粉样变转甲状腺素(ATTRv)淀粉样变。
· 小分子化合物
疏水和/或亲水小分子可以分别溶解在脂质体、SLNs和NLCs的水腔或亲脂腔中。
疏水药物分散在LBDD系统的亲脂区。 两性霉素B(一种抗真菌剂)和维替泊芬(一种光敏剂)是fda批准的疏水药物的例子,它们被制成脂质体。
亲水性药物在LBDD体系的水室中溶解。 阿霉素是一种抗肿瘤抗生素,是一种亲水药物。 Doxil®是一种脂质体包裹的阿霉素,是第一个被FDA批准的LBDD配方。
· 脂质
如何设计一个脂质纳米颗粒的药物载体?
在选择脂类及其如何配制成LNPs时,应考虑以下几个因素。
1.脂质摩尔比决定了颗粒的脂质组成,并影响其大小、多分散性和功效。建议参考此前已开发的类似应用,从相关文献入手,以确定脂质摩尔比。下表展示了FDA批准的LNPs药物的脂质摩尔比:
| |
Patisiran |
BNT162b2 |
mRNA-1273 |
| 内容药物类型 |
siRNA |
mRNA |
mRNA |
| Ionizable Cationic Lipid(可电离阳离子脂质体) |
DLin-MC3-DMA |
ALC-0315 |
SM-102 |
| Neutral Phospholipid(中性磷脂) |
1,2-DSPC |
1,2-DSPC |
1,2-DSPC |
| Sterol Lipids(固醇脂) |
Cholesterol |
Cholesterol |
Cholesterol |
| PEGylated Lipids(PEG化磷脂) |
DMG-PEG(2000) |
ALC-0159 |
DMG-PEG(2000) |
| 脂质摩尔比* |
50:10:38.5:1.5 |
46.3:9.4:42.7:1.6 |
50:10:38.5:1.5 |
FDA批准的LNPs药物中的脂质摩尔比(*Ionizable cationic lipid : neutral phospholipid : cholesterol : PEGylated lipid)
(相关产品链接请见文末)
2.脂质与寡核苷酸的重量比影响包封效率。大多数LNPs的配方为脂质:寡核苷酸重量比为10:1。
3.可电离脂质氮:寡核苷酸磷酸(N:P)摩尔比表示可电离阳离子脂质阳离子叔胺与寡核苷酸主链阴离子磷酸基团之间的电荷平衡。这一性质是电离阳离子脂质与寡核苷酸络合的基础。LNP的N:P比率通常在6左右。
4.脂酸解离常数(脂质pKa)是脂质在相同浓度下的电离和非电离形态的pH值。脂质pKa影响LNP的包封效率、疗效、传递和毒性。 对于RNA传递,脂质pKa一般在6-7之间。已经确定了不同给药途径的具体范围。静脉给药和肌肉给药的最佳脂质pKa范围分别为6.2-6.6和6.6-6.9。
5.水缓冲液的三个重要参数是它的组成、离子强度和pH值。缓冲液稳定溶液中的寡核苷酸,可电离的阳离子脂质在酸性水缓冲液中混合后变成质子化和正电荷。LNP制剂中常用的缓冲液为25-50 mM的醋酸钠或柠檬酸钠,pH为4-5。LNPs被透析到中性缓冲液中,如pH 7.4的PBS中储存和使用。
6.颗粒大小改变给药颗粒的药代动力学。 更小的颗粒通常有更长的循环半衰期,因为它们逃避单核吞噬细胞机制的清除。小于100nm的颗粒可轻易通过有孔的内皮细胞穿透靶组织。颗粒大小取决于制备方法。根据LNP制备方法的不同,可以使用挤压来实现更小、更均匀的颗粒尺寸。
7.两种最常用的给药途径是静脉注射和肌肉注射。 静脉给药的LNP主要分布在肝脏和脾脏,但也分布在肺部。带净正电荷、中性电荷和负电荷的LNPs可分别靶向肺、肝和脾。在配方中加入胆固醇或聚乙二醇化脂质,以及增加LNP的大小,增加了脾脏的分布。肌肉注射通常用于疫苗,因为它有助于淋巴结靶向和激活免疫反应。当使用疫苗时,抗原提呈细胞(APCs),如巨噬细胞和树突状细胞,被招募到交付点,在那里它们可以遇到疫苗抗原。 然后它们转移到淋巴结,刺激T细胞反应。值得注意的是,针对某一特定给药途径进行优化的制剂通常不适用于其他给药途径。
8.制备方法决定了LNPs的性质,包括尺寸、均匀性和包封效率。 在选择制备方法时,还应考虑成本、可扩展性、可再现性和时间承诺。
文章部分相关产品:
化合物
| Cat No. |
产品名称 |
CAS No. |
纯度 |
产品类型 |
| 34364 |
DLin-MC3-DMA |
1224606-06-7 |
≥95% |
可电离阳离子脂质体 |
| 34337 |
ALC-0315 |
2036272-55-4 |
≥98% |
可电离阳离子脂质体 |
| 33474 |
SM-102 |
2089251-47-6 |
≥98% |
可电离阳离子脂质体 |
| 34372 |
Lipid 5 |
2089251-33-0 |
≥95% |
可电离阳离子脂质体 |
| 35337 |
Lipid 29 |
2244716-55-8 |
≥98% |
可电离阳离子脂质体 |
| 35051 |
L-319 |
1351586-50-9 |
≥95% |
可电离阳离子脂质体 |
| 25726 |
DODAP |
127512-29-2 |
≥98% |
可电离阳离子脂质体 |
| 34363 |
DLin-KC2-DMA |
1190197-97-7 |
≥98% |
可电离阳离子脂质体 |
| 34336 |
ALC-0159 |
1849616-42-7 |
≥95% |
PEG化磷脂 |
| 33945 |
DMG-PEG(2000) |
160743-62-4 |
≥90% |
PEG化磷脂 |
| 9003100 |
Cholesterol |
57-88-5 |
≥95% |
固醇脂 |
| 15100 |
1,2-DSPC |
816-94-4 |
≥98% |
中性磷脂 |
LNP探索工具盒
| Cat No. |
产品名称 |
产品作用 |
| 36970 |
Lipid Nanoparticle (LNP-MC3) Exploration Kit |
用于准备含有DLin-MC3-DMA的LNPs |
| 35426 |
Lipid Nanoparticle (LNP-0315) Exploration Kit |
用于准备含有ALC-0315的LNPs |
| 35425 |
Lipid Nanoparticle (LNP-102) Exploration Kit |
用于准备含有SM-102的LNPs |
测量LNP诱导的免疫反应的试剂盒
| Cat No. |
产品名称 |
靶点 |
| 501240 |
Mouse IgG ELISA Kit |
小鼠免疫蛋白 |
| 501030 |
Interleukin-6 (human) ELISA Kit |
IL-6 |
| 583311 |
Interleukin-1β (human) ELISA Kit |
IL-1β |
| 502220 |
SARS-CoV-2 Neutralizing Antibody SimpleDetect ELISA Kit |
新冠中和抗体 |
上海优宁维生物科技股份有限公司 试剂 | 耗材 | 仪器 | 软件 | 定制 | 实验服务 | 供应链 免费热线:4008-168-068 咨询邮箱:info@univ-bio.com 订购商城:www.univ-bio.com 微信公众平台:优宁维抗体专家,欢迎关注! 小优博士(小程序):5大课堂, 让你的科研不再难!
  |

