METHOD for Western Blots: 1.While your SDS-PAGE gel is runningmake your transfer buffer and chill to 4℃.Check that you have a frozen buffer dam is ready (stored in freezer next to Shikhatop shelf to t ...
DunnAnal.Biochem.1986: 157 GeorgiaTimes"1.5L GeorgiaTimes"1.0L GeorgiaTimes"10mM NaHCO3 ...
ECL or autoradiography? ECL is an appealing technique because it is quick and very sensitive and does not expose the investigator to radioactivity.The use of radioiodinated protein A to detect bound a ...
薄层色谱,或称薄层层析(thin—layer chromatography),是以涂布于支持板上的支持物作为固定相,以合适的溶剂为流动相,对混合样品进行分离、鉴定和定量的一种层析分离技术。这是一种快速分离诸如脂肪酸、类固醇、氨基酸、核苷酸、生物碱及其他多种物质的特别有效的层析方法,从50年代发展起来至今,仍被广泛采用。 一、基本原理 薄层层析是把支持物均匀涂布于支持板(常用玻璃板,也可 ...
Materials •Suspension culture of fibroblast cells (1 liter) •35 mM Tris-HClpH 7.4140 mM NaCl (TBS buffer) •10 mM Tris-HClpH 7.510 mM KCland 1.5 mM magnesium acetate (TBS-M) •10X T ...
Motor proteins of several kinesin family groups have now been crystallized: monomeric Kinesin-1 motor domains from humanrat and Neurospora (Kull et al.1996; Sack et al.1997; Song et al.2001)and dimeri ...
Materials Milipore filter type HA 0.45 micron Culture plates (Linbro model 76-033-05) Protein in DDW or HEPES buffer (10 mg/ml) Vacuum grease Syringe with 18 G needle Procedure 1.Millipore filter a ...
1.Fix gel in 50% methanol for greater than 1 hour rinse gel in dH2O 3 times 5 minutes each place back in 50% methanol for 1 hour. 2.Stain gel in 100 mls of stain solution for 30 minutes 3.Rinse gel i ...
SDS-PAGE: gel electrophoresis of proteinsTECHNIQUE is to set up gel plates before you mix the gel mixes.Use the THIN spacers and choose a comb--number of wells varies.Make both resolving gel and stack ...
1.Rinse gel on glass plate briefly with distilled water. 2.Wash gel in fresh 50% ETOH-12% HAcwith shaking3 times1 hour each.(Fix IEF gel ON in 10% TCA). 3.Wash gel four times with 10% ETOH-5% HAc for ...
NuPAGE Gels A gel electrophoresis system used for SDS-PAGE protein analysis.The gels are made up of Bis-Tris-HCl (pH 6.4)polyacrylamide and are intended for denaturing conditions only. NuPAGE Electrop ...
现代近红外光谱(NIR)分析技术是近年来分析化学领域迅猛发展的高新分析技术,越来越引起国内外分析专家的注目,在分析化学领域被誉为分析“巨人”,它的出现可以说带来了又一次分析技术的革命。 近红外区域按ASTM定义是指波长在780~2526nm范围内的电磁波,是人们最早发现的非可见光区域。由于物质在该谱区的倍频和合频吸收信号弱,谱带重叠,解析复杂,受当时的技术水平限制,近红外光 ...
近红外光谱分析应用方式的特点: 近红外光谱的工作谱区信息量丰富,对样品有较强的透过能力。近红外光谱分析能在几秒钟内对被测样品完成一次光谱的采集测量,瞬间即可依靠数学模型完成其多项性能指标的测定。分析过程不产生污染、不消耗其它材料、不破坏样品,分析重现性好、成本低;可以实现快速分析、绿色分析、廉价分析,具有“多、快、好、省”的特点。尤其是在复杂物、天然物的无损、微损分析、在线 ...
我国对近红外光谱技术的研究及应用起步较晚,除一些专业分析工作人员以外,近红外光谱分析技术还鲜为人知。但1995年以来已受到了多方面的关注,并在仪器的研制、软件开发、基础研究和应用等方面取得了较为可喜的成果。但是目前国内能够提供整套近红外光谱分析技术(近红外光谱分析仪器、化学计量学软件、应用模型)的公司仍是寥寥无几。随着中国加入WTO及经济全球化的浪潮,国外许多大型分析仪器生产商纷纷登陆中国,想在第 ...
AAS原理: 通过原子化器将待测试样原子化,待测原子吸收待测元素空心阴极灯的光,从而使用检测器检测到的能量变低,从而得到吸光度。吸光度与待测元素的浓度成正比。 AAS主要分火焰法和石墨炉法。 火焰法现在大家常用的是C2H2+O2,也有极少数还在使用乙炔+笑气的(非常危险,易爆)。火焰燃烧使试样中的待测元素原子化。 石墨法炉主要是采用石墨管加热使用待测试样原子化。由于石墨炉的温度高,因此能测试的元素 ...
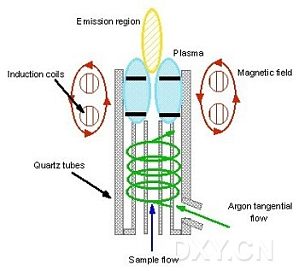
ICP的工作原理: 感耦等离子体原子发射光谱分析是以射频发生器提供的高频能量加到感应耦合线圈上,并将等离子炬管置于该线圈中心,因而在炬管中产生高频电磁场,用微电火花引燃,使通入炬管中的氩气电离,产生电子和离子而导电,导电的气体受高频电磁场作用,形成与耦合线圈同心的涡流区,强大的电流产生的高热,从而形成火炬形状的并可以自持的等离子体,由于高频电流的趋肤效应及内管载气的作用,使等离子体呈环状结构。 ...
ICP光谱仪是由ICP光源、进样装置、分光装置、检测器和数据处理系统组成。其中ICP光源由高频发生器、石英炬管和高频感应线圈组成;进样装置是由蠕动泵(一些仪器直接利用同心雾化器提升)、雾化器和雾室等组成;分光装置由入射狭缝、分光元件、若干光学镜片组成及出射狭缝(全谱直读型没有);检测器现在用的主要是光电倍增管和固体成像器件(目前主要有CCD和CID);数据处理系统主要有计算机、数据通讯 ...
电感耦合等离子体发射光谱仪(Inductively Coupled Plasma Optical Emission Spectrometer,ICP-OES)的研究领域:分析化学。 主要用途: 可用于地质、环保、化工、生物、医药、食品、冶金、农业等方面样品中元素的定性、定量分析。 指标信息: 1.检测范围:可以测定全部的金属原素及部分非金属元素(70多种http://www.parti ...
操作说明由三部手册组成: Z-5000系列偏振塞曼原子吸收光谱仪维修手册。 Z-5000系列偏振塞曼原子吸收光谱仪,火焰法分析部分手册。 Z-5000系列偏振塞曼原子吸收光谱仪,石墨炉分析法操作手册。 安全注意事项: 在维修手册中介绍,所以使用仪器前一定要阅读维修手册。 石墨炉分析法操作手册介绍了使用Z-5000系列偏振塞曼原子吸收光谱仪如何进行石墨炉法分析,在用此仪器前,必须阅读这本手册。火焰分 ...
一、关于血清使用的几点建议: 1、血清必须贮存-20℃,如存放于4℃,请勿超过两周,对于某些单位一次无法用完一瓶,可在无菌条件下将其40-45ml分装于无菌50ml离心管中(或血清瓶中),由于血清解冻时体积会增加10%,必须预留此膨胀体积的空间,否则易发生污染或容器冻裂的情形。 2、一般公司所提供的血清一般为200ml和500ml装量,因此建议在使用中宜采取逐步解冻的方法解冻血清:-20℃&rar ...