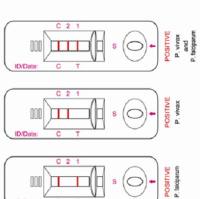
疟蚊疟疾免疫的调控
一个研究蚊子基因功能的令人兴奋的新模型,并支持FREP1在疟疾传播阻断策略中的作用。
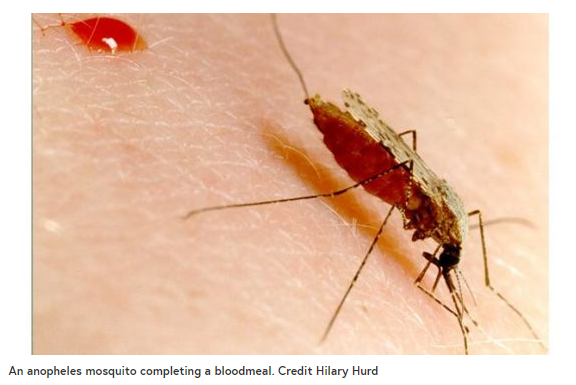
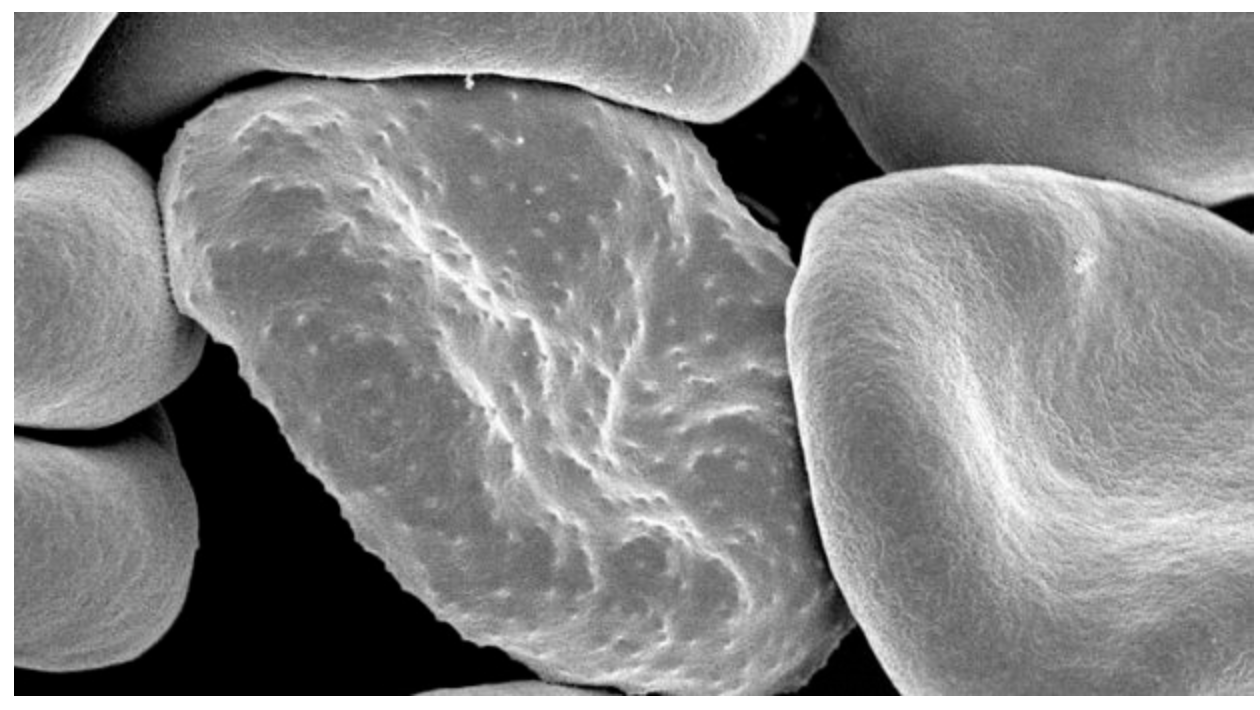
疟疾寄生虫几乎只通过被感染的疟蚊叮咬传播给人类。其他蚊子是抗疟疾的;由于先天免疫反应,它们无法维持感染。这些防御机制包括黑色素化(黑色素在细胞表面的沉积)和寄生虫的直接分解。多年来,人们一直在研究蚊子的折射现象,希望它们的免疫系统能够被改造成抗疟疾的。
CRISPR/Cas9型
随着基因编辑技术的进步,利用蚊子免疫力的潜力最近才得以实现。CRISPR/Cas9系统的发展允许高特异性基因修饰和更广泛的染色体改变。这种(最初是细菌性的)抗病毒机制以其目前在治疗学上的探索而闻名,特别是对于由基因异常引起的疾病,例如癌症。在科学界,CRISPR/Cas9很容易被用于大量的研究,从基因功能研究到人类疾病模型的复制(这里总结得很好)。
这些基因编辑工具最近被用来制造抗疟疾的冈比亚按蚊——疟疾的主要媒介。本月,Yuemie Dong和他的同事发表了他们关于纤维蛋白原相关蛋白1(FREP1)基因失活对疟原虫易感性和蚊子适应度的影响的研究。
FREP1基因的传递阻断活性
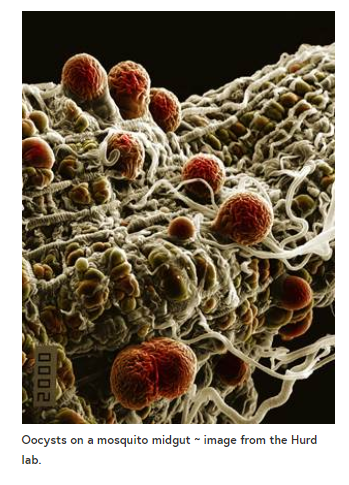
虽然还不完全了解,但FREP1是一种已知的蚊子宿主因子,可促进寄生虫通过蚊子中肠,帮助传播。去年,FREP1高度保守的纤维蛋白原样结构域(FBG)被作为阻断传播疫苗的靶点进行了研究,取得了令人鼓舞的结果。通过与蚊子中肠内配子体和卵母细胞期的相互作用,阐明了FBG的传递阻滞机制。使用抗FREP1抗体,在标准膜喂养试验期间,柏盖氏疟原虫和间日疟原虫的传播显著减少。这一点得到了小鼠研究的支持,其中FBG免疫获得了75%以上的阻断效果,抗FBG血清减少了81%以上的恶性疟原虫感染冈比亚疟原虫。
冈比亚按蚊的FREP1沉默
在此基础上,Dong等人使用CRISPR/Cas9创建FREP1基因敲除冈比亚疟原虫株系。简言之,他们交叉两个转基因蚊子株系来产生生殖系基因敲除物:1)在VASA2启动子下的Cas9表达系和2)在U6聚合酶III启动子下的FREP1靶向rna(gRNA)转基因系。后者的后代通过3XP3-TFP报告基因在幼虫或成虫眼睛中显示稳定的蓝色荧光,用于识别突变体以供进一步研究。与3个对照蚊虫株系(WT、Cas9表达株系和FREP1-gRNA株系)相比,由此产生的FREP1基因敲除表明对恶性疟原虫和伯氏疟原虫感染的易感性显著降低。此外,在卵囊期和子孢子期都观察到这种显著的减少。
利用驱动核酸内切酶基因(DEGs)的“基因驱动”机制可用于在蚊子种群中传播基因,否则将遵循孟德尔种群遗传学。这样,FREP1基因敲除基因型就可以在蚊子种群中分布,并作为疟疾的另一种媒介控制工具。然而,这些机制在很大程度上依赖于感兴趣基因的适应度代价。
健身成本效益
不幸的是,在这项研究中,FREP1基因敲除者遭受了巨大的健康代价。这些因素包括显著降低血液喂养倾向、血液餐后寿命、繁殖力和卵子孵化率。由于FREP1被认为在血液喂养和消化中起作用,它的破坏可能会影响蚊子对营养的吸收或损害蚊子中肠的防御能力,从而导致观察到的健康成本。作者还注意到,CRISPR/Cas9介导的基因编辑以在非靶点产生不想要的变化而闻名,尽管在他们的gRNA设计中考虑到了这一点,但这仍有可能导致适应度降低。由于没有观察到对成年蚊子大小和寿命的影响,他们建议通过在成年蚊子中肠或唾液腺中诱导阶段性和组织特异性基因缺失来克服适应成本。
总之,他们描述了一个研究蚊子基因功能的令人兴奋的新模型,并为FREP1在疟疾控制的传播阻断策略中的作用提供了支持性证据。