相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
999
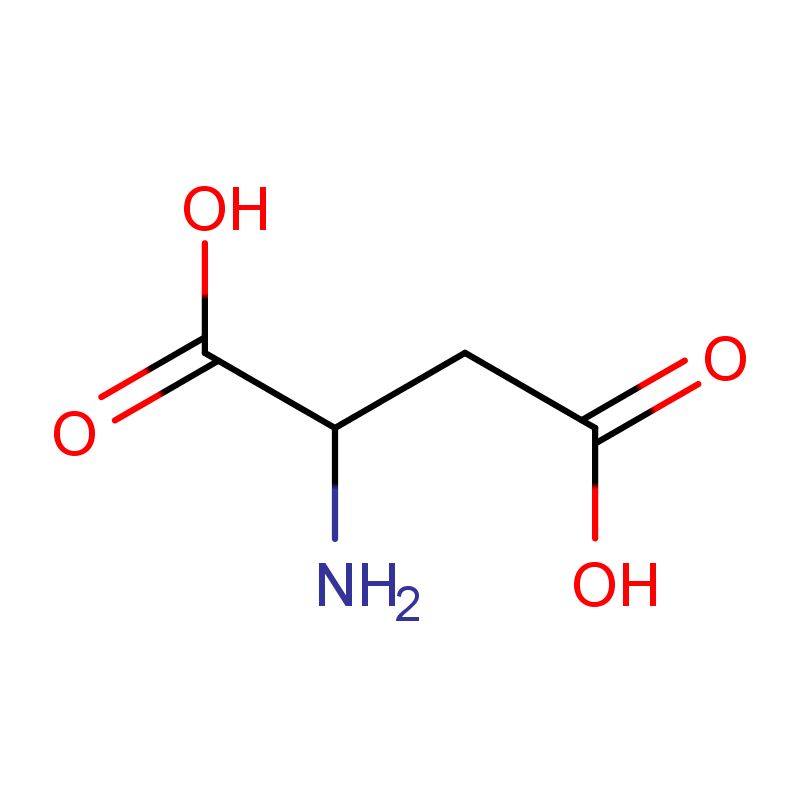
- 英文名:
D-Aspartic acid
- CAS号:
1783-96-6
- 保质期:
详见产品说明
- 供应商:
仕诺达生物
- 保存条件:
RT
- 规格:
100mg,分析标准品级别,98%(多种规格可选)/5g,BR,99% /10g,BR,99% /100g;高纯,99%
| 规格: | 100mg,分析标准品级别,98%(多种规格可选) | 产品价格: | ¥100.0 |
|---|---|---|---|
| 规格: | 5g,BR,99% | 产品价格: | ¥30.0 |
| 规格: | 10g,BR,99% | 产品价格: | ¥50.0 |
| 规格: | 100g;高纯,99% | 产品价格: | ¥100.0 |
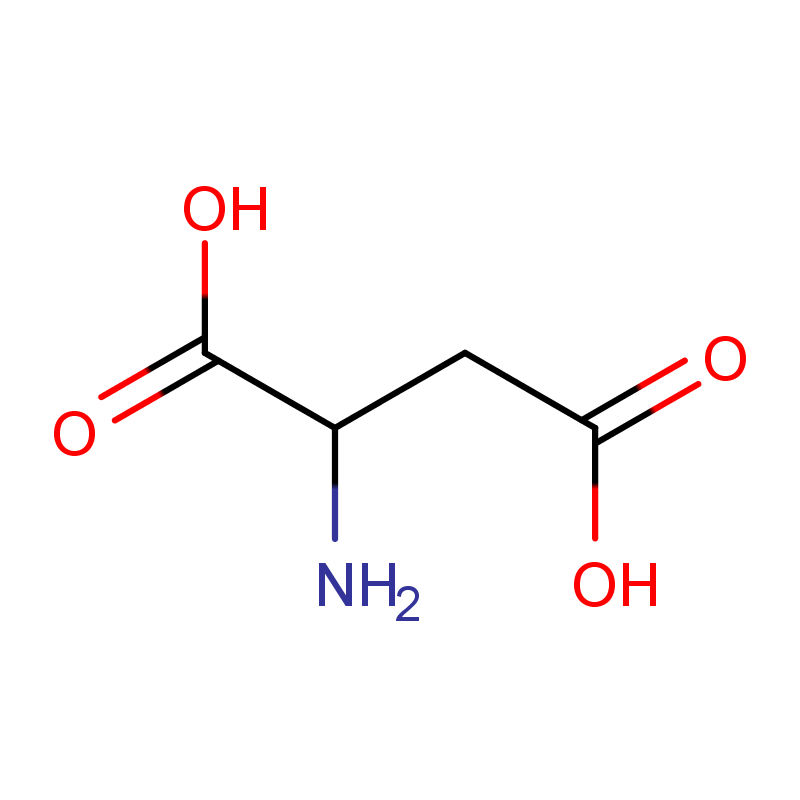
| 中文名 | D-天门冬氨酸 |
| 英文名 | D(-)-Aspartic acid |
| 别名 | D-天冬氨酸 二胺基丁二酸 D-天门冬氨酸 D(-)-天冬氨酸 D-天门冬氨酸,H-D-ASP-OH D-ASPARTIC ACID D-天冬氨酸 |
| 英文别名 | H-D-Asp d-aspartic H-D-Asp-OH d-asparticaci D-Aspartic acid l-Asparagic acid D(-)-Aspartic acid D-Aminosuccinic acid (R)-(-)-ASPARTIC ACID (R)-AMINOSUCCINIC ACID D-2-Aminobutanedioic acid 1-Amino-1,2-carboxyethane (R)-(-)-AMINOSUCCINIC ACID |
| CAS | 1783-96-6 |
| EINECS | 217-234-6 |
| 化学式 | C4H7NO4 |
| 分子量 | 133.1 |
| InChI | InChI=1/C8H12N2O8/c9-8(7(17)18,2-5(13)14)10-3(6(15)16)1-4(11)12/h3,10H,1-2,9H2,(H,11,12)(H,13,14)(H,15,16)(H,17,18)/t3?,8-/m1/s1 |
| InChIKey | CKLJMWTZIZZHCS-UWTATZPHSA-N |
| 密度 | 1.66 |
| 熔点 | >300°C(lit.) |
| 沸点 | 245.59°C (rough estimate) |
| 比旋光度 | -25.8 º (c=5, 5N HCl) |
| 水溶性 | SOLUBLE |
| 溶解度 | 酸水溶液 (微溶) |
| 折射率 | -25 ° (C=8, 50% HCl) |
| 酸度系数 | pK1: 1.89(0);pK2: 3.65;pK3: 9.60 (25°C) |
| 存储条件 | Keep in dark place,Inert atmosphere,Room temperature |
| 外观 | 结晶性粉末 |
| 颜色 | White to off-white |
| Merck | 14,840 |
| BRN | 1723529 |
| 物化性质 | 外 观 白色或类白色结晶性粉末 比旋度[a]20D -24°~ -26° |
| MDL号 | MFCD00063081 |
计算化学数据:
- 分子量:133.10268g/mol
- 化合物是否规范:True
- 准确质量:133.03750770
- 同位素质量:133.03750770
- 复杂度:133
- 可旋转化学键数量:3
- 氢键供体数量:3
- 氢键受体计数:5
- 拓扑极表面积:101
- 重原子数量:9
- 确定原子立构中心数量:1
- 不确定原子立构中心数量:0
- 确定化学键立构中心数量:0
- 不确定化学键立构中心数量:0
- 同位素原子计数:0
- 共价键单元数量:1
- CACTVS Substructure Key Fingerprint:AAADcYBiOAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAHgAQCAAACCjBgAQACABAAgAIAACQCAAAAAAAAAAAAIGAAAACABgAAAAAQAAGEAAAAABDAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAA==
■针对客户购买情况公司有不同的优惠折扣,欢迎咨询订购~
■郑重申明:本公司销售所有产品均为实物拍摄,如产品出现质量问题,本公司包一切售后!!!
■500元以上包邮,本公司提供正规发票,货到付款,可按科研实验要求定制产品!!!
■本公司已与很多高校中科院及研发单位合作并也获得了老师的认可和推荐!!! 
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验1. [IF=7.79] Ye Lu et al."Enhancing hydrogel-based long-lasting chemiluminescence by a platinum-metal organic framework and its application in array detection of pesticides and D-amino acids."Nanoscale. 2020 Feb;12(8):4959-4967
2. [IF=5.537] Yurong Ma et al."Pre-cut NaCl solution treatment effectively inhibited the browning of fresh-cut potato by influencing polyphenol oxidase activity and several free amino acids contents."Postharvest Biol Tec. 2021 Aug;178:111543
3. [IF=4.556] Dandan Zhao et al."Physico-chemical properties and free amino acids profiles of six wolfberry cultivars in Zhongning."J Food Compos Anal. 2020 May;88:103460
4. [IF=4.379] Feng Lin et al."Chemical profile changes during pile fermentation of Qingzhuan tea affect inhibition of α-amylase and lipase."Sci Rep-Uk. 2020 Feb;10(1):1-10
5. [IF=4.35] Xiaomei Dai et al."1-Methylcyclopropene Preserves the Quality of Chive (Allium schoenoprasum L.) by Enhancing Its Antioxidant Capacities and Organosulfur Profile during Storage."Foods. 2021 Aug;10(8):1792
6. [IF=2.752] Yuting Zhang et al."Metabolomic Analysis and Identification of Sperm Freezability-Related Metabolites in Boar Seminal Plasma."Animals-Basel. 2021 Jul;11(7):1939
7. [IF=4.242] Hang Yang et al."Dietary leucine requirement of juvenile largemouth bass (Micropterus salmoides) based on growth, nutrient utilization and growth-related gene analyses."Aquaculture. 2022 Jun;555:738207
of technique. In general, living organs are composed of l -form amino acids. Conversion from l -form to d -form amino acids is a first-order chemical reaction. Thus, the quantity of d -form amino acids in an organ is proportional to the passed time (age
L-氨基酸氧化酶,存在于肾脏 肝脏 霉菌、蛇毒、细菌等中,为直接氧化 L-氨基酸的需氧性脱氢酶。 EC1. 4. 3. 2.如果不存在过氧化氢酶,则以 H2 O2 脱羧形成酮酸。 其辅酶是 FMN或 FAD。底物专一性广泛,能很好地氧化亮氨酸、甲硫氨酸等,但不作用于天冬氨酸、谷氨酸、甘氨酸等。但是,鸟类肝脏的酶对碱性氨基酸具有专一性。不过,由于活性低,因此动物的酶对氨基酸代谢是否有意义尚属疑问。但对 L-α -羟酸的氧化活性
β-咪唑丙烯酸。给予狗大量的组氨酸后可从尿中得到,还有细菌作用于组氨酸也能生成尿刊酸。在哺乳类的肝脏或细菌中作为从组氨酸到谷氨酸的代谢途径的中间体,在组氨酸酶的作用下进行分子内的无氧脱氨基而生成。通常尿刊酸在肝脏酶(尿刊酸酶)的作用下进一步分解转变成谷氨酸。
 技术资料
技术资料