相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 供应商:
上海研卉生物科技有限公司
- 库存:
大量
- 英文名:
FCP
- 规格:
60ug
胶原杂交肽,5-FAM结合物(F-CHP),Collagen Hybridizing Peptide, 5-FAM Conjugate (F-CHP)-
货号:FLU60
胶原杂交肽(CHP)是一种新颖独特的多肽,在体外和体内都能特异性地结合未折叠的胶原链。[1,2,3]通过共享天然胶原的Gly-X-Y重复序列,CHP具有通过改造三螺旋结构与变性胶原链杂交的强大能力以类似于DNA片段退火成互补DNA链的方式。chp是非常特异的:由于缺乏结合位点,它对完整的胶原分子的亲和力可以忽略不计,并且由于其中性和亲水性,它对非特异性结合是惰性的。
CHP是一种强大的组织病理学工具,可以直接检测多种疾病引起的炎症和组织损伤,以及在发育和衰老过程中的组织重塑。[3]CHP在三维胶原培养中有力地显示了癌细胞蛋白水解酶迁移引起的细胞周围基质转换,不使用合成的含氟基质或转基因细胞。[4]CHP可以在分子水平上测量和定位胶原组织的机械损伤。[5]它还可以评估去细胞外基质中的胶原变性。[6]此外,CHP可用于SDS-PAGE凝胶中胶原条带的特异性显示,无需蛋白印迹。
f-chp用荧光素标记直接荧光检测。特征
胶原蛋白是人体含量最丰富的蛋白质,是各器官细胞外基质的主要结构组分。生物体组织内的胶原蛋白会因癌症、心肌梗死以及纤维化等多种疾病而引发大规模的降解。这些损伤的胶原蛋白往往是组织病变的重要标记,然而实际上却难以采用常规的方法进行检测。近期,一种新颖的靶向受损胶原蛋白的多肽探针问世----CHP,其很好地实现了利用组织切片进行多种疾病的检测,使其成为检测、探究多种相关疾病的有力工具,并且可用于靶向病变组织的药物输送等药物研发领域。胶原杂交肽(CHP)是一种新颖且独特的肽,其可以在体内外特异性结合未折叠的胶原链。胶原蛋白分子具有独特的三螺旋结构,经酶解的胶原分子其三螺旋犹如拉链一般被解旋开来。CHP可通过改变胶原蛋白分子的三螺旋结构,与变性的胶原链杂交,其方式类似于与互补DNA链退火的DNA片段。1. 特异性地结合组织中受损的胶原蛋白
CHP非常特异,主要表现在其能够特异性地结合组织中降解的胶原蛋白。这是由于CHP缺乏与正常完整胶原分子的结合位点,导致其对于完整胶原分子的亲和力可忽略不计。加上CHP呈中性,且具有亲水性,使其对完整胶原分子的非特异性结合反应是惰性的。因而,CHP与正常完整的胶原分子结合率极低,即实现了特异性结合组织中受损的胶原蛋白。
此外,CHP还能够检测出骨关节炎、心肌梗死、肾小球性肾炎、肺纤维化以及胚胎骨骼发育和皮肤老化等多种病理生理变化,但不结合对照组中的正常组织。2. 无需抗体即可检测受损的胶原蛋白
目前,市面上有不少关于胶原蛋白的检测抗体,然而往往针对于正常完整的胶原蛋白。如若将这些抗体用于检测受损的胶原蛋白时,往往效果不佳。CHP无需抗体,即可实现受损胶原蛋白的检测,很好地弥补了原先采用抗体检测受损胶原蛋白的局限性。
3. 强大的组织病理学工具,可用于药物研发
CHP是一种强大的组织病理学工具,在多个科研领域呈现出多重作用。
(1)检测癌细胞的细胞周期:CHP可以有效检测出3D胶原培养物中癌细胞蛋白水解迁移引发的细胞周期变化,无需荧光基质或转基因细胞。
(2)检测胶原组织的机械损伤:CHP可以在分子水平上测量并定位包括骨、软骨、肌腱、韧带、椎间盘、心脏瓣膜、血管、皮肤、角膜等部位的胶原组织机械损伤。(3)评估胶原变性:CHP可以直接定量分析脱细胞化的细胞外基质中的胶原变性。(4)实现胶原带的可视化:CHP可用于在SDS-PAGE凝胶中特异性可视化胶原带,无需进行蛋白质印迹。
(5)检测药物筛选疗效:CHP可用于临床前和临床实验中检测候选药物的疗效。
(6)分子造影、药物靶向输送的新工具:CHP也是一种靶向多种疾病组织微环境的新方式,为分子造影、靶向药物输送带来了新机遇。
CHP检测方法与其他胶原蛋白检测法的比较
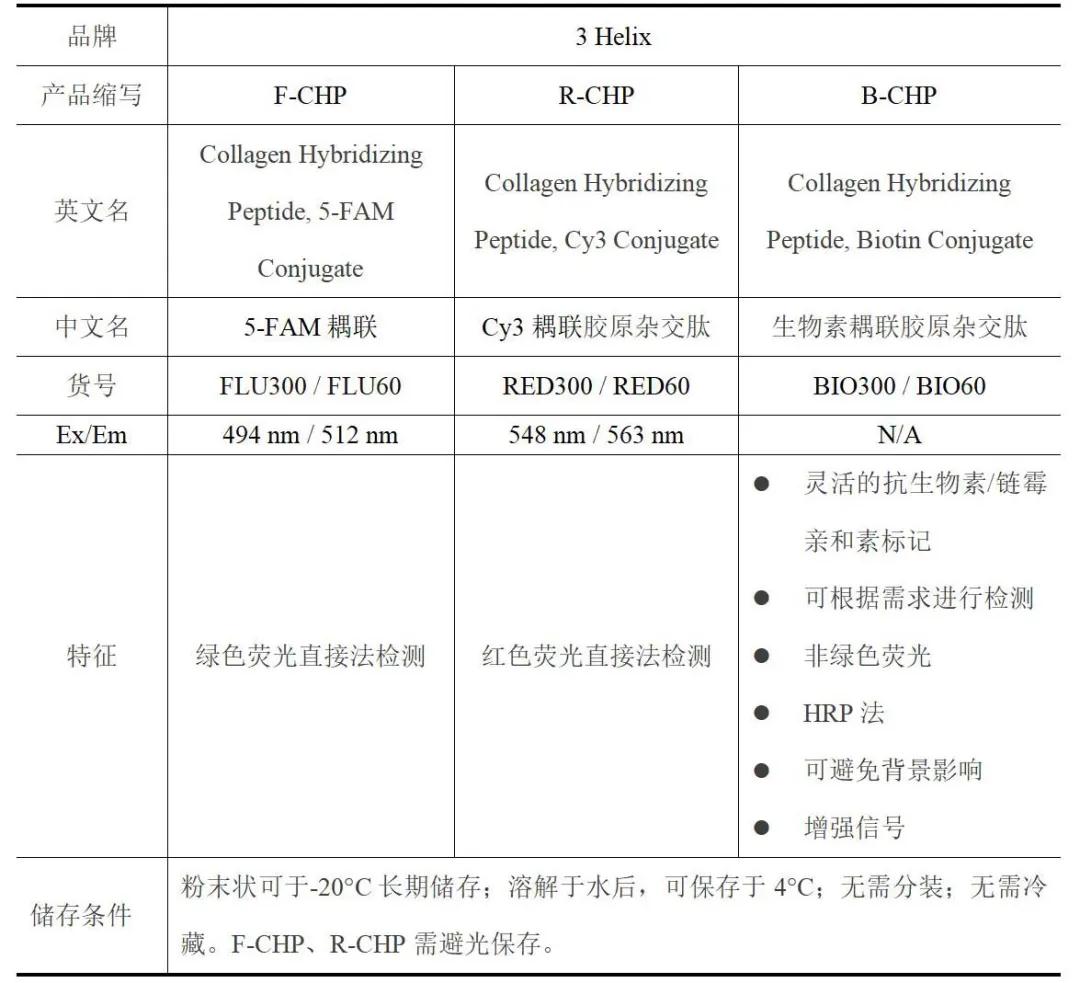
CHP三种标记产品
CHP可用于免疫荧光,免疫组化,SDS-PAGE等多种实验,并且有三种标记产品可供选择。
比酶谱、dq胶原、shg和tem更具信息性、可靠性和方便性。
对胶原的高亲和力和无yu伦比的特异性,基本上没有非特异性结合
适用于所有种类的胶原蛋白,依赖于胶原蛋白的二级结构而不是任何确定的结合顺序
适用于冰冻切片和石蜡切片,无需抗原提取
一种对共染色抗体无物种限制的非抗体方法
小尺寸(2%的IgG×MW),无需切片即可轻松穿透组织和整个样本染色
在4°C的溶液中稳定,无需等份储存
文献参考:
[1] Targeting and mimicking collagens via triple helical peptide assemblies. Current Opinion in Chemical Biology, 2013, 17, 968–975.
[2] In situ imaging of tissue remodeling with collagen hybridizing peptides. ACS Nano, 2017, 11, 9825-9835.
[3] Targeting collagen strands by photo-triggered triple-helix hybridization. Proceedings of the National Academy of Sciences of the United States of America, 2012, 109, 14767-14772.
[4] Visualizing collagen proteolysis by peptide hybridization: From 3D cell culture to in vivo imaging. Biomaterials, 2018, 183, 67-76.
[5] Direct detection of collagenous proteins by fluorescently labeled collagen mimetic peptides. Bioconjugate Chemistry, 2013, 24, 9-16.
[6] Molecular level detection and localization of mechanical damage in collagen enabled by collagen hybridizing peptides. Nature Communications, 2017, 8, 14913, doi: 10.1038/ncomms14913.
[7] Molecular assessment of collagen denaturation in decellularized tissues using a collagen hybridizing peptide. Acta Biomaterialia, 2017, 53, 268–278.
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验against bcl-2, via a derivative of 1,4,7,10-tetraazacyclododecane- N,N′,N′,N′′-tetraacetic acid (DOTA), which facilitates the incorporation of macrocyclic radiometal chelates into a peptide–PNA conjugate and thus the construct can be traced when used
周期性在表观上的简单性,使它得到了大量研究。引人注目的是,两个螺旋间的相互作用仍然是高度特异性的过程。正是结构周期表面的简单性与高特异性和强亲和力相结合,使这个普遍存在的蛋白质结构类型这样地引人注目。 在天然的和设计的含 2 个 或 3 个螺旋的标准盘绕螺旋中,界面边缘的互补电荷可缓解不同螺旋间的排斥这就是以促进杂寡聚的形成。我们把这称为肽拉链(PV ) 假定 [8] 。这是在参考了 Kim 及其合作者设计的、他们称之为 “ Peptide Velcro” 的、专性杂二聚盘绕螺旋
 技术资料
技术资料暂无技术资料 索取技术资料