万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 提供商:
南京博恩生物技术有限公司
- 服务名称:
流式细胞术实验服务
南京博恩生物技术有限公司提供一站式流式细胞术实验服务,覆盖方案评估、panel 设计、样本前处理、染色上机、数据分析及发表级结果图整合等完整环节。服务对象涵盖高校、科研院所、医药企业及生物技术企业,可满足免疫细胞分型、功能亚群分析、肿瘤免疫微环境研究、细胞凋亡与周期检测、胞内细胞因子检测、磷酸化蛋白检测以及干细胞与分化细胞表型分析等多类项目需求。
流式细胞术是一种基于单细胞悬液、多参数荧光标记和高速光学检测的分析技术,可在单细胞水平同步检测多个表面或胞内标志物。其核心特点在于单细胞、多参数、定量化分析,适用于细胞群体比例变化、功能状态变化、特定 marker 表达改变、凋亡与增殖状态评估以及免疫抑制群体识别等研究场景。
导读
一、服务概述
二、服务范围
三、服务优势
四、适用客户类型
五、服务流程
六、质量控制要点
七、样本要求
八、交付内容
九、售后支持
十、周期与报价方式
十一、博恩优势
附录A、流式细胞术原理
附录B、流式细胞术应用场景与常见 marker 选择
附录C、流式细胞术与其他蛋白检测实验的应用对比分析
一、服务概述
南京博恩生物技术有限公司提供一站式流式细胞术实验服务,覆盖方案评估、panel 设计、样本前处理、染色上机、数据分析及发表级结果图整合等完整环节。服务对象涵盖高校、科研院所、医药企业及生物技术企业,可满足免疫细胞分型、功能亚群分析、肿瘤免疫微环境研究、细胞凋亡与周期检测、胞内细胞因子检测、磷酸化蛋白检测以及干细胞与分化细胞表型分析等多类项目需求。
二、服务范围
2.1 基础检测服务
可开展常规免疫细胞表型分析、细胞亚群分型、细胞活率检测、细胞凋亡检测、细胞周期分析、细胞增殖分析、膜蛋白表达分析及基础多色流式检测。
2.2 功能检测服务
可开展细胞因子胞内染色、活化状态分析、耗竭状态分析、磷酸化蛋白流式检测及刺激后功能检测分析,适用于免疫功能研究、药效研究及信号通路评估。
2.3 专题研究服务
可开展肿瘤免疫微环境分析、巨噬细胞极化分析、树突细胞亚群分析、NK 细胞状态分析、MDSC 分型、干细胞与祖细胞分型及分化细胞表型分析等专题项目。
2.4 数据整理服务
可提供原始数据整理、中文报告撰写、中英文图注整理及发表级结果图整合,便于后续论文、汇报及项目材料使用。
三、服务优势
3.1 项目流程清晰
从前期方案评估到最终结果交付均按照标准流程推进,覆盖实验设计、样本接收、检测执行、数据分析和结果整理全过程。
3.2 检测方案适配性强
可根据样本类型、物种背景、目标群体、检测指标及研究重点进行方案调整,适配不同研究方向和应用场景。
3.3 结果输出结构完整
结果交付包含原始文件、中文报告、中英文图注及整理后的发表级整合结果图,便于后续科研整理与成果输出。
四、适用客户类型
4.1 高校与科研院所
适用于免疫表型分析、机制研究、论文补充实验、课题申报数据支持及结题材料整理。
4.2 医药企业
适用于药效免疫评价、细胞治疗相关检测、靶点验证、通路检测及研发阶段数据支撑。
4.3 生物技术企业
适用于抗体验证、细胞产品表型分析、多参数筛查及项目外包检测。
五、服务流程
5.1 方案提交
提交研究目的、样本类型、物种、分组设计、目标细胞群、目标 marker、参考文献及预期分析方式等基础信息。
5.2 方案评估
对样本是否适合流式检测、panel 设计是否合理、荧光通道分配是否可行、是否需要活死染、胞内染色、刺激处理或磷酸化检测进行评估。
5.3 问题反馈与优化
针对 marker 搭配、种属适配、串色风险及分析逻辑进行检查和优化,完善实验方案。
5.4 正式报价
根据样本数量、检测指标数量、颜色数及实验复杂度出具正式报价。
5.5 合同签订与项目启动
确认合作内容、周期安排及交付标准后启动项目。
5.6 实验执行与结果整理
进入样本处理、染色上机、数据分析、中文报告整理、图注撰写及发表级结果图整合流程。
5.7 结果交付
完成项目后交付原始文件、中文报告、中英文图注及整理后的发表级整合结果图。
六、质量控制要点
6.1 样本质量评估
样本接收后需评估细胞状态、活率、团聚情况、碎片比例及是否存在明显污染,以降低样本本身对结果的干扰。
6.2 对照与补偿设置
根据项目复杂度设置空白对照、单染补偿对照、FMO 对照及必要生物学对照,保证多色检测边界设定和补偿准确性。
6.3 上机采集控制
根据目标群体丰度设定合理采集事件数。低频群体通常需要更高采集量,以保证结果具有基本统计可靠性。
6.4 分析逻辑审核
数据分析需遵循清晰的母群体建立、亚群拆分和功能群定义逻辑,降低误判风险。
七、样本要求
流式细胞术要求样本尽可能制备为高质量单细胞悬液,并尽量减少碎片、团聚、死亡细胞及红细胞污染。样本质量会直接影响分析准确性、背景水平和最终结果可信度。
7.1 细胞悬液样本
需保证为单细胞悬液,尽量无团聚,细胞状态良好。适用于常规细胞表型分析,建议冰上短途运输并尽快检测。
7.2 PBMC 样本
需保证分离后细胞活率较高、数量充足,适用于人外周免疫分型,可采用冰上运输或按方案冻存运输。
7.3 全血样本
需明确抗凝类型并尽快处理,适用于人全血免疫分型,通常采用常温或低温短时运输。
7.4 脾脏、淋巴结及肿瘤组织样本
需保持组织新鲜,便于制备单细胞悬液,适用于小鼠组织免疫微环境分析,建议冰上运输并尽快处理。
7.5 骨髓样本
需保持细胞新鲜并避免严重凝集,适用于造血及髓系分析,建议冰上运输。
7.6 贴壁细胞样本
建议采用温和消化方法,避免表面抗原丢失。部分消化条件可能影响表面 marker 表达,需提前说明处理方式。
7.7 固定后样本
需提前说明固定方式及处理条件。部分活率检测和功能检测不适用于固定样本,应在方案评估阶段确认适配性。
7.8 送样地区确认
由于流式细胞术通常要求样本保持新鲜状态并尽快完成检测,如由客户自行提供样本,需在送样前先确认送样地区、运输方式及预计到样时间,确保样本到达时仍满足检测要求。
7.9 客户需同步提供的信息
需提供物种、组织来源、分组方式、目标群体、目标 marker 以及是否涉及胞内或核内染色等关键信息,以便完成 panel 设计和分析逻辑构建。
八、交付内容
8.1 原始实验文件
交付原始 FCS 文件及相关原始数据文件,便于后续数据存档、复核及再分析。
8.2 中文报告
交付中文报告,内容包括试剂信息、仪器信息、实验方法及结果描述。
8.3 中英文图注
交付与结果图对应的中英文图注,便于后续论文、汇报及材料整理使用。
8.4 发表级整合结果图
交付整理好的发表级整合结果图,便于直接用于论文初稿、汇报展示或项目材料整理。
九、售后支持
项目完成后可就交付结果中的基础内容进行必要沟通与说明。
十、周期与报价方式
常规项目周期通常为 20–40 个工作日。报价根据样本数量、检测指标数量、颜色数及实验复杂度综合确定。
十一、博恩优势
南京博恩生物技术有限公司提供覆盖方案设计、实验执行、数据分析和结果整理的流式细胞术实验服务,可支持免疫细胞分型、功能亚群分析、肿瘤免疫微环境评估、凋亡与周期检测、胞内细胞因子检测、磷酸化蛋白检测及干细胞表型分析等多类项目。项目流程清晰,结果输出完整,检测体系可根据研究方向进行调整,便于后续科研、研发及项目材料整理。
附录A、流式细胞术原理
A1、技术原理概述
流式细胞术是一种基于单细胞悬液、多参数荧光标记和高速光学检测的分析技术,可在单细胞水平同步检测多个表面或胞内标志物。其核心特点在于单细胞、多参数、定量化分析,适用于细胞群体比例变化、功能状态变化、特定 marker 表达改变、凋亡与增殖状态评估以及免疫抑制群体识别等研究场景。
A2、信号检测机制
流式细胞术通过让单个细胞依次通过激光检测区域,记录前向散射光、侧向散射光及多个荧光通道信号,从而在单细胞水平分析细胞大小、内部复杂度和标志物表达。前向散射光通常反映细胞大小,侧向散射光通常反映内部复杂度,而荧光信号则反映特定分子的表达状态。通过多参数联合分析,可在同一样本中同时完成细胞组成、功能状态及相关表达变化评估。
附录B、流式细胞术应用场景与常见 marker 选择
B1、总体设计原则
流式细胞术的应用场景与 marker 设计密切相关。实际设计中通常应先明确样本来源、物种、研究问题和目标群体,再依次选择基础 marker、分群 marker、功能 marker 和状态 marker,避免仅凭单一指标直接定义复杂细胞亚群。
B2、免疫总群与基础分群
B2.1 总白细胞起始圈门
免疫细胞分析中常以 CD45 作为总白细胞起始 marker,用于建立免疫细胞母群体。在 PBMC、脾脏、肿瘤组织及炎症组织样本中,CD45 常作为进入免疫群分析的基础入口。
B2.2 淋巴系与髓系基础拆分
在总白细胞基础上,可结合 CD3、CD19、CD11b、CD14、CD11c、HLA-DR 等 marker 进一步区分淋巴细胞与髓系细胞群体。该类设计适用于基础免疫分型、药效评估及组织免疫状态比较。
B3、T 细胞相关应用与 marker
B3.1 T 细胞基础分型
T 细胞常以 CD3 作为基础 marker,再结合 CD4、CD8 进行辅助性 T 细胞和细胞毒性 T 细胞分群。该类分析适用于外周免疫分型、肿瘤浸润淋巴细胞分析及干预前后免疫状态比较。
B3.2 初始、记忆与效应 T 细胞分析
在基础分型之上,可进一步加入 CD45RA、CCR7、CD62L、CD27、CD28 等 marker,用于区分初始型、中心记忆型、效应记忆型及终末效应型等不同分化状态。
B3.3 T 细胞活化分析
活化 T 细胞常在 CD3+ 群体基础上结合 CD69、CD25、HLA-DR、CD38 等 marker 进行评估,适用于刺激实验、药物处理实验及早期免疫应答观察。
B3.4 Treg 分析
Treg 通常采用 CD3+、CD4+、FOXP3+、CD25+ 组合,必要时加入 CD127 low 以提高定义特异性。扩展 marker 可包括 CTLA-4、CD39、CD73、Helios 等,用于增强对调节性表型的刻画。
B3.5 Th1、Th2、Th17 及相关功能亚群分析
(1)Th1 常结合 T-bet、IFN-γ、CXCR3。
(2)Th2 常结合 GATA3、IL-4、IL-13、CCR4。
(3)Th17 常结合 RORγt、IL-17A、CCR6,必要时可扩展 IL-22。
该类设计适用于炎症、感染、免疫调节和功能分化研究。
B3.6 耗竭 T 细胞分析
耗竭 T 细胞常在 CD3+、CD8+ 或 CD4+ 群体基础上联合观察 PD-1、TIM-3、LAG-3、TIGIT 等 marker。部分研究也会扩展 CD39、CTLA-4 等分子,用于更细化的功能衰竭表型分析。
B3.7 细胞毒性功能分析
如需评估细胞毒性能力,可结合 Granzyme B、Perforin、CD107a、IFN-γ 等 marker,对杀伤活性和脱颗粒状态进行分析。
B4、B 细胞相关应用与 marker
B4.1 B 细胞基础分型
人样本中 B 细胞常用 CD19、CD20 作为基础 marker;小鼠样本中常用 B220 或 CD19。该类项目适用于 PBMC 分型、脾脏免疫分析及体液免疫相关研究。
B4.2 B 细胞成熟与记忆分群
可进一步加入 IgD、CD27、CD38、CD24、CD21、CD23 等 marker,用于区分初始 B 细胞、记忆 B 细胞、过渡型 B 细胞、浆母细胞等不同成熟阶段和功能亚群。
B4.3 浆细胞与抗体分泌细胞相关分析
如需关注浆母细胞或浆细胞方向,可结合 CD27、CD38、CD138 等 marker 进行扩展分析。
B5、NK 细胞相关应用与 marker
B5.1 NK 细胞基础识别
NK 细胞通常需先排除 CD3 阳性群体。人样本中常用 CD56、CD16、NKp46、NKG2D 等 marker;小鼠样本中常用 NK1.1、NKp46、NKG2D、CD122 等 marker。不同物种及不同小鼠品系之间 marker 适用性存在差异。
B5.2 NK 细胞亚群分析
在人样本中,可结合 CD56 bright 与 CD56 dim 状态区分不同功能倾向亚群;也可结合 CD16、CD57、NKG2A、KIR 家族分子等进行更精细分层。
B5.3 NK 细胞活化与功能分析
可在 NK 总群基础上增加 CD69、CD25、CD107a、IFN-γ、Granzyme B、Perforin 等 marker,用于观察活化、脱颗粒与细胞毒功能状态。
B6、单核细胞与巨噬细胞相关应用与 marker
B6.1 单核细胞基础分型
人样本中单核细胞常用 CD14、CD16 作为基础分群 marker,并可结合 HLA-DR、CCR2、CD11c、CD64 等提高分群精度。常见分析方向包括 classical、intermediate 和 non-classical 单核细胞分群。
B6.2 总巨噬细胞识别
巨噬细胞分析通常应先定义总巨噬群。人样本中常参考 CD68、CD163、CD14、CD64;小鼠样本中更常用 F4/80、CD68、CD11b 等 marker。
B6.3 M1-like 巨噬细胞分析
M1-like 状态常在总巨噬群基础上结合 CD80、CD86、HLA-DR、TLR4、iNOS、TNF-α 等 marker 进行判断,适用于炎症反应、免疫激活及抗肿瘤效应研究。
B6.4 M2-like 巨噬细胞分析
M2-like 状态常在总巨噬群基础上结合 CD163、CD206、CD209、Arginase-1 等 marker 进行判断,适用于免疫抑制微环境、组织修复及肿瘤促进状态研究。
B7、树突细胞相关应用与 marker
B7.1 树突细胞基础识别
树突细胞常以 CD11c、HLA-DR 或 MHC II 为基础 marker,并结合 lineage 排除策略提高识别准确性。该类分析适用于抗原递呈、疫苗反应及免疫激活研究。
B7.2 cDC 与 pDC 分群
人样本中,cDC 常结合 CD1c、CLEC9A、CD141 等 marker 细分;pDC 常结合 CD123、CD303、CD304。小鼠体系中则常结合 CD11c、MHC II、XCR1、Siglec-H、CD317 等 marker 进行亚群分析。
B7.3 功能状态扩展分析
在树突细胞群体基础上,可进一步加入 CD80、CD86、CCR7 等 marker,用于评估成熟状态和抗原递呈活化状态。
B8、中性粒细胞与髓系抑制性细胞相关应用与 marker
B8.1 中性粒细胞分析
人样本中中性粒细胞常用 CD15、CD16、CD66b、MPO 等 marker;小鼠样本中常用 Ly6G、CD11b、MPO,必要时结合 Ly6C。该类项目适用于炎症研究、感染研究及肿瘤相关髓系分析。
B8.2 MDSC 分析
MDSC 的 marker 体系具有明显物种差异。人样本中常用 CD11b、CD33、HLA-DR low 作为基础识别框架,并可结合 CD14、CD15、CD66b 等区分不同亚型;小鼠样本中常用 CD11b、Gr1、Ly6C、Ly6G 进行分析。该类检测适用于肿瘤免疫抑制研究、药效研究及髓系重塑分析。
B9、干细胞与祖细胞相关应用与 marker
B9.1 基础分型
干细胞与祖细胞分析常以 CD34 为基础,人样本中可结合 CD38、CD90、CD45RA、CD117 等 marker 进行扩展;小鼠体系中常进一步加入 Sca-1、c-Kit 等 marker。
B9.2 分化状态比较
在基础 marker 之上,可根据研究方向补充特定谱系 marker,用于比较不同分化阶段的表型差异和群体比例变化。
B10、凋亡、增殖、周期及功能检测相关应用与 marker
B10.1 细胞凋亡检测
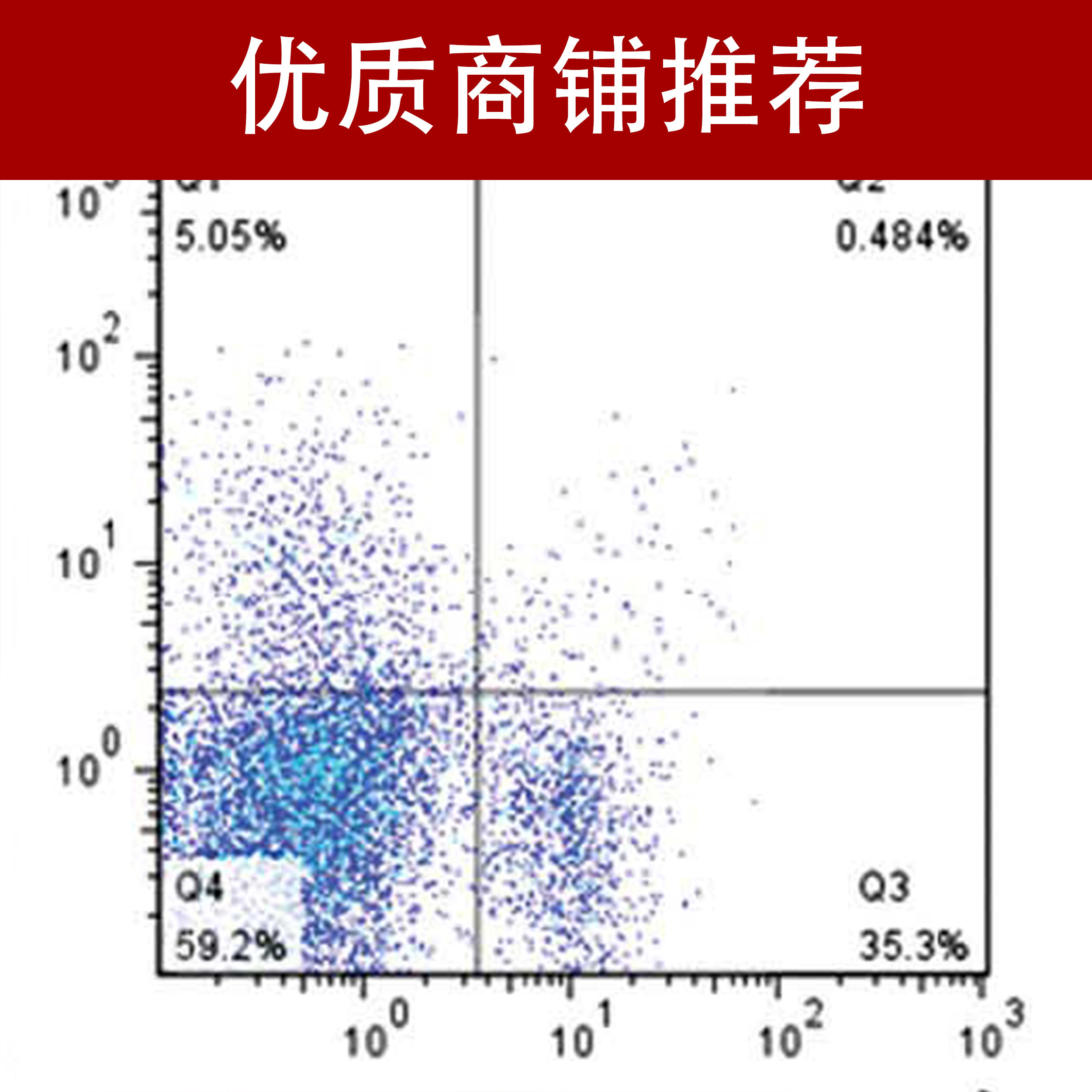
常采用 Annexin V/PI 或同类方案,用于区分早期凋亡与晚期凋亡群体,适用于药效、毒性及细胞损伤研究。
B10.2 细胞周期检测
常采用 DNA 含量染色,用于分析 G0/G1、S、G2/M 期比例,适用于增殖、阻滞及药物作用机制研究。
B10.3 细胞增殖检测
常采用 CFSE、CTV 或 Ki-67 进行评估,用于分析细胞分裂代数及增殖率,适用于免疫活化与药物干预研究。
B10.4 胞内细胞因子检测
常检测 IFN-γ、IL-2、IL-4、IL-10、IL-17A、TNF-α 等指标,适用于 T 细胞功能研究、炎症研究及刺激后应答评估。
B10.5 磷酸化蛋白检测
常检测 p-STAT3、p-STAT5、p-AKT、p-ERK、p-p38、p-S6 等指标,适用于信号通路活化状态评估及快速功能检测分析。
B11、人鼠差异与 marker 选择注意事项
不同物种的 marker 体系不能直接照搬。巨噬细胞在人样本中更常用 CD68、CD163,小鼠中更常用 F4/80;pDC 在人样本中更常用 CD123、CD303、CD304,小鼠中更常用 Siglec-H、CD317;中性粒细胞在人样本中常用 CD15、CD16、CD66b,小鼠中更常用 Ly6G;MDSC 在人样本中常用 CD33、HLA-DR low,小鼠中则更常用 Gr1、Ly6C、Ly6G。进行 panel 设计时,应先明确样本物种、样本来源和研究问题,再匹配相应体系。
附录C、流式细胞术与其他蛋白检测实验的应用对比分析
C1、与 Western blot 的应用对比
流式细胞术与 Western blot 均可用于蛋白检测,但两者关注层级不同。Western blot 更适合判断目标蛋白条带、分子量及整体表达变化,适用于总蛋白水平验证;流式细胞术更适合在单细胞层面观察蛋白表达,分析不同细胞亚群中的表达差异及比例变化。若研究重点在于明确表达细胞类型、比较阳性率变化或评估特定亚群增强与减弱情况,流式细胞术更具优势;若研究重点在于确认蛋白条带存在情况、分子量准确性及总表达量变化,Western blot 更为适合。
C2、与免疫荧光的应用对比
免疫荧光更适合观察空间定位、组织结构关系、细胞形态及共定位情况;流式细胞术更适合进行大量单细胞定量分析和复杂亚群拆分。若研究重点在于组织切片中的定位关系和微环境空间分布,免疫荧光更具优势;若研究重点在于定量比较、群体比例统计和多参数联合分析,流式细胞术更适合。
C3、与 ELISA 的应用对比
ELISA 更适合对上清、血清或裂解液中的可溶性分子进行总体定量,尤其适用于细胞因子、抗体及分泌蛋白的高通量检测。流式细胞术更适合回答具体由哪类细胞表达或分泌目标分子,尤其在胞内细胞因子检测和亚群功能分析中优势更明显。若研究重点在于总体浓度变化,ELISA 更直接;若研究重点在于细胞来源和表达分布,流式细胞术更具优势。
C4、与免疫组化的应用对比
免疫组化更适合在组织水平呈现目标蛋白在病理结构中的分布,适用于临床病理观察和组织定位判断;流式细胞术更适合将组织消化为单细胞后进行高通量定量和多参数分析。两者在组织样本研究中具有互补关系,前者强调空间信息,后者强调单细胞定量与群体拆分。
C5、方法选择的一般思路
当研究重点在于单细胞、多参数、群体比例、亚群功能和动态状态变化时,优先考虑流式细胞术;当研究重点在于总蛋白表达、条带验证、组织定位或上清浓度时,可根据问题分别选择 Western blot、免疫荧光、免疫组化或 ELISA。对于机制研究、药效研究和免疫微环境研究,流式细胞术通常与其他蛋白检测方法联合使用,以获得更完整的证据链。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验1.Sajedi N, Homayoun M, Mohammadi F, Soleimani M. Myricetin Exerts its Apoptotic Effects on MCF-7 Breast Cancer Cells through Evoking the BRCA1-GADD45 Pathway. Asian Pac J Cancer Prev. 2020;21(12):3461-3468. Published 2020 Dec 1. doi:10.31557/APJCP.2020.21.12.3461
2.Fan B, Shi S, Shen X, et al. Effect of HMGN2 on proliferation and apoptosis of MCF-7 breast cancer cells. Oncol Lett. 2019;17(1):1160-1166. doi:10.3892/ol.2018.9668
3.Mirmalek SA, Faraji S, Ranjbaran S, et al. Cyanidin 3-glycoside induced apoptosis in MCF-7 breast cancer cell line. Arch Med Sci. 2020;19(4):1092-1098. Published 2020 Mar 19. doi:10.5114/aoms.2020.93789
4.Fu YZ, Yan YY, He M, et al. Salinomycin induces selective cytotoxicity to MCF-7 mammosphere cells through targeting the Hedgehog signaling pathway. Oncol Rep. 2016;35(2):912-922. doi:10.3892/or.2015.4434
5.Lv MM, Zhu XY, Chen WX, et al. Exosomes mediate drug resistance transfer in MCF-7 breast cancer cells and a probable mechanism is delivery of P-glycoprotein. Tumour Biol. 2014;35(11):10773-10779. doi:10.1007/s13277-014-2377-z