万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 技术资料
DNA甲基化整体解决方案
一、结合重亚硫酸盐的测序法实验流程(BSP)(Bisulfite Genomic Sequence)
原理:结合重亚硫酸盐的测序法是一种灵敏的能直接检测分析基因组DNA甲基化模式的方法。重亚硫酸盐处理后,用针对改变后的DNA序列设计特异性引物并进行聚合酶链式反应(PCR)。 PCR产物中原先非甲基化的胞嘧啶位点被胸腺嘧啶所替代,而甲基化的胞嘧啶位点保持不变。PCR产物克隆后进行测序。通过这个方法能得到特定位点在各个基因组DNA分子中的甲基化状态。
该方法特点是:
1. 特异性高,它能够提供特异性很高的分析结果,这是所有其他研究甲基化的分析方法所不能比拟的;
2. 灵敏度高,可以用于分析少于100个细胞的检测样品。用微量的基因组DNA进行分析就能得到各个DNA分子精确的甲基化位点分布图。

图1 结合亚硫酸盐的测序法流程图
DNA用重亚硫酸盐处理后进行PCR扩增,扩增片段纯化后连接进载体,转化大肠杆菌,过夜培养后挑单个阳性克隆进行测序。得到每个DNA分子特定区域甲基化位点的分布图。
结合重亚硫酸盐测序法技术实验流程
A.DNA制备
用DNA抽提试剂盒(Promega, cat. no. A1125)抽提组织,细胞培养物,石蜡包埋组织切片样品中的基因组DNA。
B.重亚硫酸盐处理
C.DNA纯化
用Wizard DNA clean-up kit (Promega, cat. no. A7280)纯化重亚硫酸盐处理后的DNA样品。
D.DNA脱磺基反应
E.PCR扩增
F.PCR产物琼脂糖电泳后回收纯化,随后连接到pGEM-T EASY 载体中克隆及测序。
二、甲基化特异性的PCR实验流程
(methylation-specific PCR, MSP)
原理:甲基化特异性的PCR是一种灵敏度高且操作相对简单的甲基化研究方法。重亚硫酸盐处理DNA后,基因组DNA发生的由甲基化状态决定的序列改变。随后进行引物特异性的PCR。该方法引物设计是关键。MSP中设计两对引物,即一对结合处理后的甲基化DNA链(引物对M),另一对结合处理后的非甲基化DNA链(引物对U)。检测MSP扩增产物,如果用引物M能扩增出片段,则说明检测位点存在甲基化;若用引物U扩增出片段,则说明被检测的位点不存在甲基化(图3)。
该方法优点是:
1、检测灵敏度高,样品消耗少,仅需1μg的基因组DNA,可用于石蜡包埋样本;
2、快速、简单,省时;
3、如果结合Real-time定量PCR技术(Taqman 探针)则能对样品中检测位点的甲基化水平进行定量检测(Methylight)。

图2 甲基化特异性的PCR(MSP)流程示意图
用亚硫酸盐处理后DNA分子发生了由甲基化状态决定的序列改变。用甲基化特异性的引物(primer M)和非甲基化特异性的引物(primer U)进行扩增。只有结合完全的甲基化或
MSP技术实验流程
A.DNA抽提
用DNA抽提试剂盒(Promega, cat. no. A1125)抽提组织,细胞培养物,石蜡包埋组织切片样品中的基因组DNA。
B. 重亚硫酸盐处理
C.DNA纯化
用Wizard DNA clean-up kit (Promega, cat. no. A7280)纯化重亚硫酸盐处理后的DNA样品。
D.DNA脱磺基反应
E.甲基化特异性的PCR反应
针对改变后的DNA序列设计两对引物(M,U),进行PCR反应。为了避免非特异性扩增用TaKaRa的hotstart酶。随后对PCR产物的凝胶电泳图进行分析。
实例:
检测肝癌细胞株Bel7405,Bel7404中SFRP1基因启动子甲基化。重亚硫酸盐处理后,针对改变的DAN序列设计两对引物
M: (forward: AGTTAGTGTCGCGCGTTC; reversal: CCGATACCCATACCGACTC) 299 bp
U:(forward:GGAGTTGGGGTGTATTTAGTTTG; reversal: CCAATACCCATACCAACTCTACA) 247 bp

图3:PCR扩增结果图
三、高分辨率熔解曲线(HRM)法
高分辨率熔解曲线分析技术(High Resolution Melting ),简称HRM ,是近年来兴起的一种检测基因突变、进行基因分型而及甲基化检测的新方法。基本原理是基于核酸分子由于片段长短、GC含量、GC 分布及单个碱基差异等物理性质不同而造成DNA 分子在加热变性时都会有不同的熔解曲线的形状和位置,并配合运用高浓度的饱和荧光染料,可以迅速的检测出核酸片段中GC含量和单碱基的突变。近年来,公司引进了Roche LightCycler® 480 II 和ABI VIIA7 全自动荧光定量PCR系统,为客户提供专业化、个性化的甲基化HRM检测服务。
操作流程:
﹡待测基因序列片段或位点甲基化引物设计(300bp以内)。
﹡利用甲基化转移酶修饰的DNA和非甲基化修饰的DNA制备标准品(0%,1%,5%,10%,20%,50%,100%梯度HRM标准曲线)
﹡亚硫酸氢盐处理样品DNA
﹡上机检测
﹡数据处理,形成报告(包括实验过程、试剂耗材、荧光PCR仪原始文件、测序文件等)。
实验实例:
对2个病例的某基因20个CG位点进行检测,分析出不同的甲基化程度。

四、焦磷酸测序法
焦磷酸测序(Pyrosequencing)技术是由4种酶(DNA聚合酶(DNA polymerase)、ATP硫酸化酶(ATP sulfurytase)、荧光素酶(luciferase)和三磷酸腺苷双磷酸酶(Apyrase))催化的同一反应体系中的酶级联化学发光反应。每一轮测序反应体系中只加入一种脱氧核苷酸三磷酸(dNTP)。如果该dNTP与模板配对,则会在DNA聚合酶的作用下,添加到测序引物的3'末端,同时释放出一个分子的焦磷酸(PPi)。掺入的dNTP和释放的PPi是等量的。CpG甲基化焦磷酸测序检测法基于引物延伸的Pyrosequencing技术,通过将链合成过程中释放出的焦磷酸(PPi)转化成光信号来监测链的合成过程。通过检测CpG对应位点上C/T渗入的比例对目标位点的甲基化程度进行定量分析方法。
操作流程:
﹡DNA亚硫酸盐处理
﹡用焦磷酸测序专门引物设计软件设计甲基化引物
﹡进行PCR扩增预实验及正式实验
﹡PCR产物上焦磷酸测序仪检测
实验实例:

各种方案比较

服务说明
①样品要求:
﹡血液样品:样品为EDTA抗凝或枸椽酸钠抗凝,样品量大于0.5 ml,样品采集后于-20℃或-80℃保存,低温(≤-4℃)运输。
﹡组织样品:样品可以为新鲜组织(最好-80℃保存)或石蜡包埋的组织,也可以是95%乙醇中固定的组织,组织量大于100 mg。
﹡DNA样品:纯度OD260/280 比值为1.8-1.9,浓度≥50ng/ul,体积≥50ul。
②提供详细的基因信息
BSP方法要求待测序列≤300bp,HRM待测序列≤200bp,HRM待测序列≤200bp,焦磷酸测序待测序列≤60bp,且上下游保留200bp用于引物设计;MS方法要求提供待测序列的CG侯选位点。我们会根据客户的基因序列信息选择不同的检测方法,并在方案实验过程中随时与客户沟通。
③提供结果
实验报告(实验步骤,包括BSP法的5个克隆统计结果等)、PCR电泳照片、测序彩色波形图、HRM标准曲线图、焦磷酸测序原始文件、基因芯片的原始文件等。
m6A RNA甲基化测序
RNA甲基化修饰约占所有RNA修饰的60%以上,而N6-甲基腺嘌呤(N6-methyladenosine, m6A)是高等生物mRNA和lncRNAs上最为普遍的修饰。目前发现microRNA,circRNA, lncRNA, rRNA, tRNA和snoRNA上都有发生m6A修饰。 m6A修饰主要发生在RRACH序列中的腺嘌呤上,其功能由“编码器(Writer)”、“消码器(Eraser)”和“读码器(Reader)”决定。“编码器(Writer)”即甲基转移酶,目前已知这个复合物的成分有METTL3,METTL14, WTAP和KIAA1429;而ALKBH5和FTO作为去甲基酶(消码器)可逆转甲基化;m6A由m6A结合蛋白识别,目前发现m6A结合蛋白(读码器)有YTH结构域蛋白(包括YTHDF1, YTHDF2,YTHDF3, YTHDC1和YTHDC2)和核不均一蛋白HNRNP家族(HNRNPA2B1和 HNRNPC)。在基因表达、蛋白翻译和RNA剪切等正常生物过程中具有重要作用。近来有研究显示m6A RNA甲基化在乳腺癌、恶性血液病、胶质母细胞瘤、宫颈癌等多种癌症的发生发展中具有重要作用。
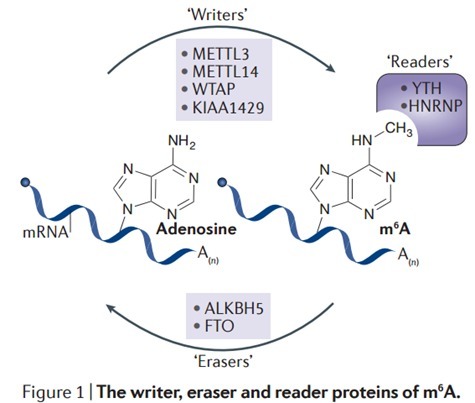
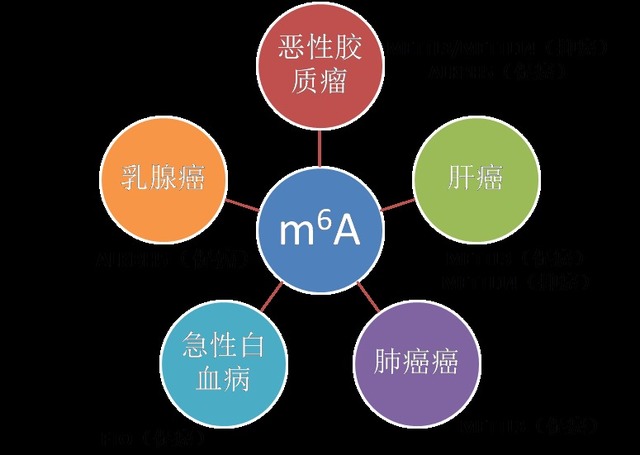
图 1 m6A修饰的酶系统 图 2 m6A生物学功能
一、MeRIP-seq实验流程
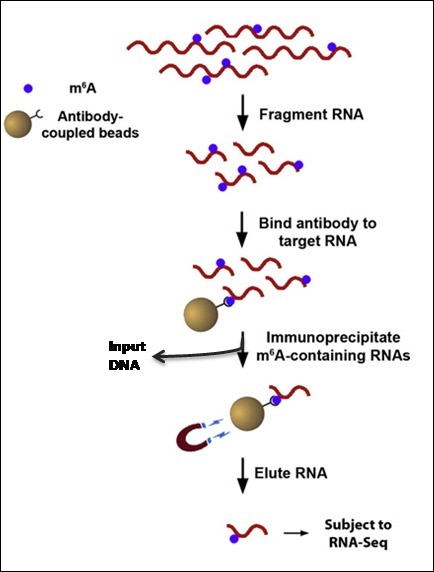
图3 英拜 m6A RNA甲基化测序实验流程
二、m6A甲基化测序分析内容
- 测序数据质量评估及QC
- 测序序列与参考基因组比对
- RNA甲基化peak calling
- peak在基因组中的分布及注释
- Peak在基因组中富集程度统计
- 差异RNA甲基化区域分析
- 差异RNA甲基化区域GO与KEGG富集分析
三、研究案例
1、m6A Demethylase ALKBH5 Maintains Tumorigenicity of Glioblastoma Stem-like Cells by Sustaining FOXM1 Expression and Cell Proliferation Program. Cancer Cell 2017.(IF=27.4)DNA甲基化异常是胶质瘤的表观遗传调控因子,但RNA甲基化在肿瘤包括恶性胶质瘤(GBM)中的调控还尚未清楚。为研究m6A调节可能导致GBM患者临床疗效不佳,作者通过TCGA数据库,发现ALKBH5在恶性胶质瘤样干细胞(GSCs)中高表达且与GBM 病人不良预后相关,干扰ALKBH5 降低GSCs细胞的自我更新能力且抑制GSCs增殖,进一步体内验证敲除ALKBH5可抑制肿瘤生长。
为研究ALKBH5的m6A作用机制,作者利用芯片和m6A-seq筛选到胶质瘤增殖相关的FOXM1,最后通过qPCR、WB、免疫荧光、核质分离WB/qPCR、RIP和MeRIP等实验证明ALKBH5通过去甲基化调节FOXM1在GSCs中的表达。
为研究ALKBH5对FOXM1的作用是否受其他因子的调节,作者研究了FOXM1的邻近基因,发现lncRNA FOXM1-AS与FOXM1序列互补,且共表达、共定位,进一步通过RIP, RNA pull down等实验证明lncRNA FOXM1-AS促进ALKBH5 和FOXM1初级转录本的相互作用。最后通过细胞实验进一步验证ALKBH5在lncRNA FOXM1-AS的作用下维持FOXM1的表达和细胞增殖,从而维持GSCs的干性。
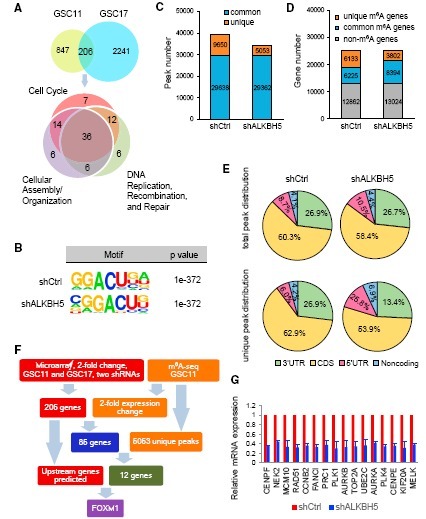 |
图4 ALKBH5敲除细胞中m6A修饰的特征和基因表达的变化
2、RNA N6-methyladenosine methyltransferase METTL3 promotes liver cancer progressionthrough YTHDF2 dependent post-transcriptional silencing of SOCS2. Hepatology,2017.(IF=13.2)
表观遗传改变极大地促进了人类癌症的发生。传统的表观遗传研究主要集中在DNA甲基化,组蛋白修饰和染色质重构。最近,RNA各种可逆的化学修饰被认为是一种新的表观遗传调控方式。m6A是真核生物mRNA最常见的化学修饰,在调控mRNA稳定性,剪切和翻译方面具有重要的作用。
作者使用转录组测序发现了METTL3(甲基转移酶3),一种主要的RNA N6-腺苷-甲基转移酶,在人肝细胞癌(HCC)和多种实体肿瘤中显著高表达。在临床上,METTL3的过度表达与肝细胞癌患者不良预后有关。体外实验证明敲除METTL3会显著抑制HCC细胞增殖,迁移及克隆形成。体内实验证明敲除METTL3会明显抑制HCC体内成瘤和肺转移。另外,使用CRISPR/dCas9-VP 64激活系统,内源性高表达METTL3会显著促进HCC细胞在体外和体内生长。通过转录组测序、m6A-Seq、MeRIP-PCR,作者确定了SOCS2(细胞因子信号2的抑制因子)作为METTL3介导的m6A修饰的下游靶基因。 敲除METTL3表达会消除SOCS2 mRNA m6A修饰并增强SOCS2 mRNA表达。m6A介导的SOCS2 mRNA降解是依赖于m6A“读取器”蛋白YTHDF2。总之,METTL3在HCC大部分高表达中,并通过m6A-YTHDF2依赖机制抑制SOCS2表达从而促进HCC进展。因此,作者发现了在肝肿瘤发生过程中表观遗传改变的一种新机制。
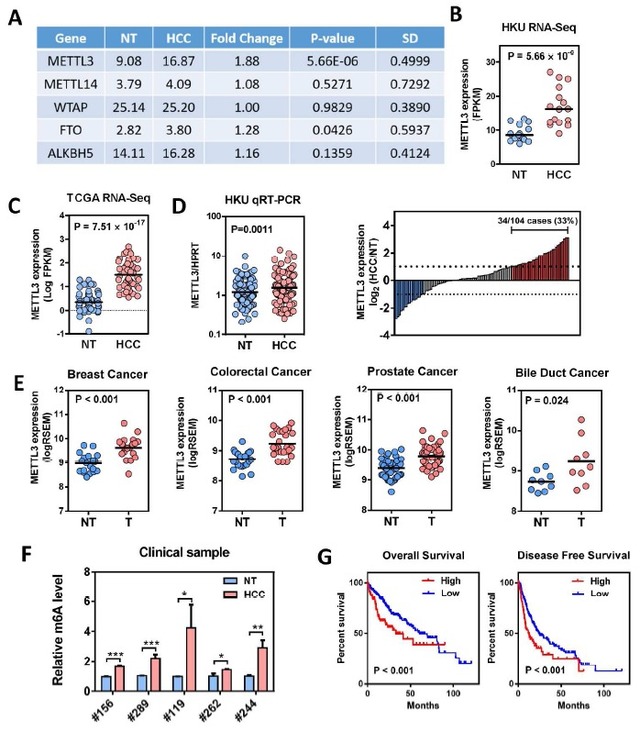
图5 RNA甲基化转移酶METLLT3在肝癌组织中高表达
(转录组测序结果及TCGA数据库分析)
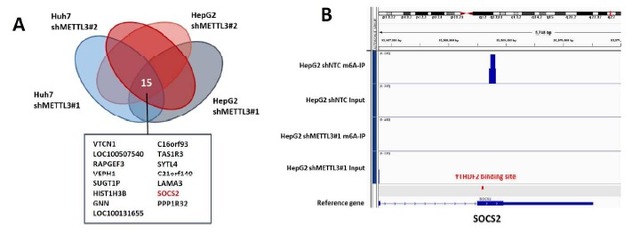
图6 RNA-Seq和m6A-seq联合鉴定SOCS2是METTL3
介导的m6A修饰的下游靶基因
3、N6-adenosine methylation in MiRNAs. PLoS One 2015,
在许多不同种类的RNA中,都已观察到N6 -腺苷(m6A)的甲基化,但其在microRNAs中还没有被研究。研究者在FTO1C1, FTO2D4 和 FTO3C3细胞系中,通过敲除m6A甲基转移酶FTO筛选到表达差异的microRNA,说明miRNA受m6A甲基化的调控。进一步通过MeRIP-Seq发现相当一部分的microRNA具有m6A修饰。通过motif分析,他们发现了区分甲基化和非甲基化microRNA的一致序列。该文章所述的表观遗传修饰在基因表达的转录后调控的复杂性上增加了一个新的层次。
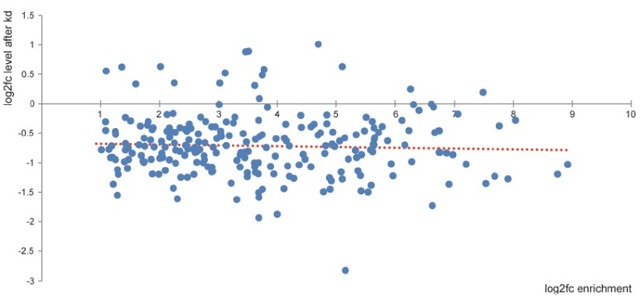
图7 FTO敲除对甲基化的miRNAs的稳定状态的影响。
四、送样要求
A样品要求:- 样品类型:细胞、新鲜组织或RNA样品。
- 样品量:细胞样品请提供至少5×107~108个细胞,组织样品请提供至少5g的组织块,RNA样品请提供500μg以上的总RNA。
- 样品质量:RNA无明显降解,提取的总RNA OD260/280值在1.8~2.2之间,浓度 ≥ 500ng/μl,28S:18S ≥ 1.5,RIN ≥7。
- 样品保存:细胞样品或新鲜组织块(切成~50mg的小块)可用TRIZOL或RNA保护剂处理或液氮冻存后,-80℃保存。RNA样品可溶于乙醇或RNA-free的超纯水中,-80℃保存。样品保存期间避免反复冻融。
- 样品运输:样品置于1.5 ml管中,封口膜封好,干冰运输。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 技术资料
技术资料暂无技术资料 索取技术资料
DNA/RNA 甲基化
询价