相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 保质期:
3年
- 库存:
1
- 供应商:
罗辅医药
- 现货状态:
现货
- 执行标准:
USP/EP/BP/JP
- 产品用途:
蛋白,多肽类药物的溶媒
- 曾用名:
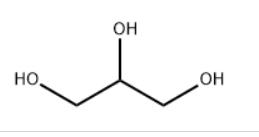
丙三醇
- 批准文号:
CDE登记中
- 英文名:
GLYCERINE (供注射用)
拥有 FDA注册的cGMP生产设施
符合USP / EP/BP/JP药典和注射剂辅料专论。
符合ICHQ7、21 CFR-210-211和IPEC
cGMP工厂2015年4月接收美国FDA检查,无关键缺陷
cGMP工厂2016年4月接收EMEA QP检查,无关键缺陷
工厂经过全球领先的注射剂以及生物制药审计和批准
可根据客户特殊需求定制50gm至5000kg的批量
总计90,000平方英尺的生产车间,包括8个小型cGMP制造模块。
符合ICH Q11的工艺和产品开发。
DOE(实验设计)和QbD(质量设计)过程方法。
高纯度低内毒素,适用于生物制药加工。
产品符合欧洲药典、美国药典、英国药典,日本药典、中国药典
产品类别:适用于注射剂
包装:
4L(5KG)
20L(25KG)
200L(250KG)
中国法规状态:
罗辅医药正在积极准备合成甘油的CDE备案登记,预计2020年公示
产品优势
超纯(99.9%)全合成甘油,质量优良,批间稳定
产品透明无色,无异常气味
超低醛类限度,长期稳定不聚集
TSE/BSE, 无过敏原声明,GMO声明等
热源以及微生物
超低内毒素(<5EU/G,远远低于中国药典以及欧洲药典)
菌落总数 <10CFU/G
总霉菌和酵母菌 < 10CFU/G
大肠杆菌:未检出
残留溶剂
符合ICH Q3C残留溶剂指南以及USP<467>中残留溶剂的限度
WT合成甘油,不含任何一、二,三类残留溶剂(其它合成工艺至少含有三类残留溶剂)
杂质控制
重金属≤2ppm
总杂≤0.5%
任何其它杂质≤0.1%
其它:
DNase(endo)符合要求
DNase(exo)符合要求
RNase符合要求
蛋白酶符合要求

| 关注微信公众号,免费申领样品 |
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验9001双重认证,使用来自日本的健康鲑鱼加工而成,保持极低的重金属含量、汞含量和铁含量。产品无论是细菌内毒素、残留溶剂(乙醇)还是异常毒性都在欧洲、美国药典限度之内,是目前国内所能找到的最高质量的进口硫酸鱼精蛋白原料药,不仅可使用在胰岛素制剂上,还可以用于目前市场上短缺的硫酸鱼精蛋白注射液的生产。据悉,该款产品的进口注册也已在准备之中。雄隽进口辅料的另一款产品Hedinger注射级间甲酚(全球唯一一款符合欧洲、美国药典的注射级间甲酚)已在国内的胰岛素制备中取得了不可替代的地位,此次高质量的硫酸
佚名 人体可利用甘油、糖、脂肪酸和甘油一酯为原料,经过磷脂酸途径和甘油一酯途径合成甘油三酯。 (一)甘油一酯途径 以甘油一酯为起始物,与脂酰CoA共同在脂酰转移酶作用下酯化生成甘油三酯。 (二)磷脂酸途径 磷脂酸即3磷酸1,2甘油二酯,是合成含甘油脂类的共同前体。糖酵解的中间产物类磷酸二羟丙酮在甘油磷酸脱氢酶作用下,还原生成α磷酸甘油(或称3磷酸甘油);游离的甘油也可经甘油激酶催化,生成α
甘油三酯的生成(triglycerides biosynthesis)
动物的肝脏和脂肪组织是合成甘油三酯最活跃的部位;小肠粘膜在脂肪消化吸收后也可由甘油一酯合成大量甘油三酯。油料作物的胚乳及子叶部分的甘油三酯合成也很旺盛。甘油三酯合成的主要前体是脂酰辅酶A和L-α-磷酸甘油。后者可由糖酵解的中间代谢物磷酸二羟丙酮在磷酸甘油脱氢酶的作用下生成,也可由甘油与ATP在甘油激酶作用下生成。甘油三酯合成的第一步是α-磷酸甘油的两个游离羟基在转脂酰基酶的作用下由两分子脂酰辅酶A酰化生成L-α-磷脂酸。磷脂酸在磷脂酸磷酸酶的作用下生成甘油二酯。甘油
 技术资料
技术资料暂无技术资料 索取技术资料










