相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 服务名称:
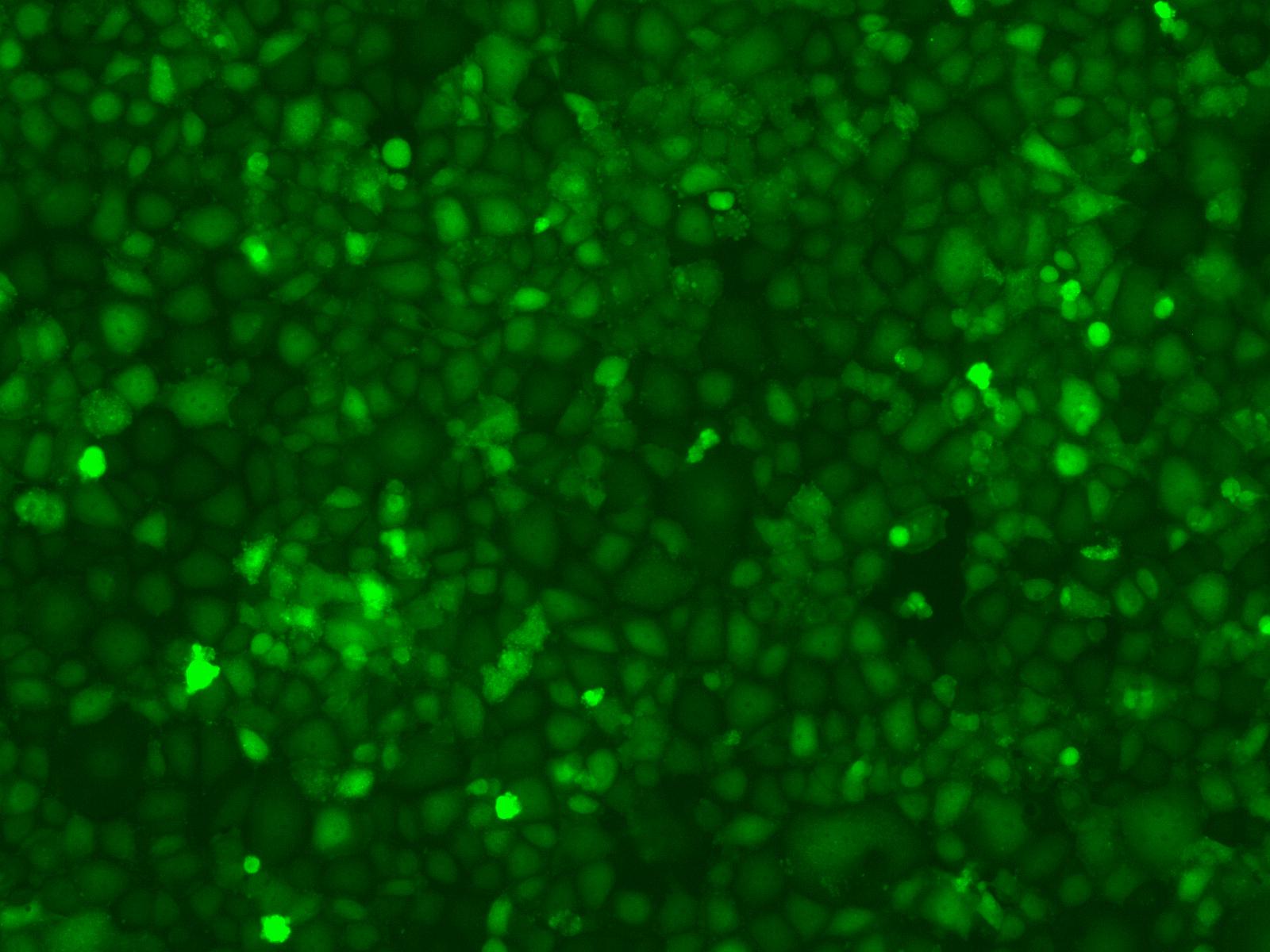
细胞转染
- 提供商:
威斯腾生物
一、基因转染技术简介
转染-即把核酸导入细胞,已经成为当前生命科学研究中基本操作之一,转染方法有多种,包括介质介导和电穿孔,其中介质又有早期的磷酸钙法,脂质体法和病毒介导。目前使用最广泛的是脂质体介导法,有很多商品化转染试剂可供选择,很多公司,包括国内研究人员耳熟能详的Invitrogen、Roche、Qiagen、Novagen等等都开发生产了转染试剂,它们也的确帮助了多数研究者完成了转染实验。转染的关键是高转染效率和低细胞毒性,即把核酸转入尽可能多的细胞,又要使转染了核酸的细胞尽可能多地存活,且没有发生分化。
二、脂质体介导DNA转染法
脂质体(lipofectin regeant,LR)试剂是阳离子脂质体N-[1-2,3-Dioleyoxy, Propyl]-n, n,n-Trimethylammonium Chloride(DOTMA)和Dioleoyl photidye-thanolamine(DOPE)的混合物[1:1(w/w)]。它适用于把DNA转染入悬浮或贴壁培养细胞中,是目前条件下最方便的转染方法之一。转染率高,优于磷酸钙法,比它高5~100倍,能把DNA和RNA转染到各种细胞。
用LR进行转染时,首先需优化转染条件,应找出该批LR对转染某一特定细胞适合的用量、作用时间等,对每批LR都要做:第一,先要固定一个DNA的量和DNA/LR混合物与细胞相互作用的时间,DNA可从1~5μg和孵育时间6小时开始,按这两个参数绘出相应LR需用量的曲线,再选用LR和DNA两者最佳的剂量,确定出转染时间(2~24小时)。因LR对细胞有一定的毒性,转染时间以不超过24小时为宜。
细胞种类:COS-7、BHK、NIH3T3、Hela和Jurkat等任何一种细胞均可作为受体细胞。
1、操作步骤[方法一]:
(1):取6孔培养板(或用35mm培养皿),向每孔中加入2mL含1~2×105个液,37℃CO2培养至40%~60%汇合时(汇合过分,转染后不利筛选细胞)。
(2)转染液制备:在聚苯乙稀管中制备以下两液(为转染每一个孔细胞所用的量)A液:用不含血清培养基稀释1-10μg DNA,终量100μL,B液:用不含血清培养基稀释2-50μgLR,终量100μL,轻轻混合A、B液,室温中置10-15分钟,稍后会出现微浊现象,但并不妨碍转染(如出现沉淀可能因LR或DNA浓度过高所致,应酌情减量)。
(3)转染准备:用2mL不含血清培养液漂洗两次,再加入1mL不含血清培养液。
(4)转染:把A/B复合物缓缓加入培养液中,摇匀,37℃温箱置6~24小时,吸除无血清转染液,换入正常培养液继续培养。
(5)其余处理如观察、筛选、检测等与其它转染法相同。
注意:转染时切勿加血清,血清对转染效率有很大影响。
2、快速脂质体转染法操作步骤如下[方法二]:
(1)以5×105细胞/孔接种6孔板(或35mm培养皿)培养24小时,使其达到50~60%板底面积。
(2)在试管中配制DNA/脂质体复合物方法如下:
①在1mL无血清DMEM中稀释PSV2-neo质粒DNA或供体DNA。
②旋转1秒钟,再加入脂质体悬液,旋转。
③室温下放置5~10分钟,使DNA结合在脂质体上。
(3)弃去细胞中的旧液,用1mL无血清DMEM洗细胞一次后弃去,向每孔中直接加入1mL DNA/脂质体复合物,37℃培养3~5小时。
(4)再于每孔中加入20%FCS的DMEM,继续培养14~24小时,
(5)吸出DMEM/DNA/脂质体混合物加入新鲜10%FCS的DMEM,2mL/孔,再培养24~48小时。
(6)用细胞刮或消化法收集细胞,以备分析鉴定。
稳定的脂质体转染方法如下:
(1)接种细胞同前,细胞长至50%板底面积可用于转染。
(2)DNA/脂质体复合物制备转染细胞同前(2)、(3)步骤。
(3)在每孔中加入1mL、20%FCS的DMEM,37℃培养48小时。
(4)吸出DMEM,用G418选择培养液稀释细胞,使细胞生长一定时间,筛选转染克隆,方法参照细胞筛选法进行。
三、影响转染的因素:转染是否成功的影响因素很多,如需要转染的细胞类型(对于困难的细胞系尤其如此),需要被转染的分子(DNA、RNA、寡核苷酸、蛋白质),转染试剂等。但无论在何种情况下,转染的成功均取决于转染效率、低细胞毒性以及重现性这几个要素。
实验服务流程
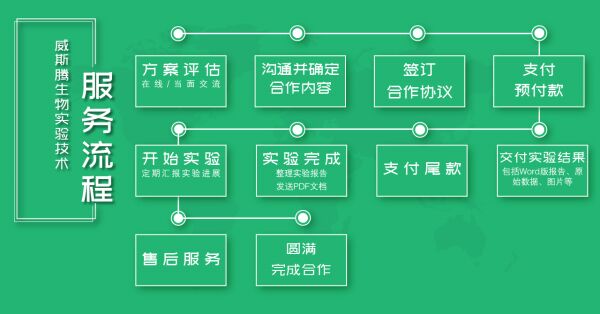
威斯腾生物服务项目
| 分子生物学类 | 蛋白质与免疫学 | 动物实验 |
| 实时荧光定量PCR | 单克隆抗体制备 | 帕金森疾病模型 |
| 免疫共沉淀(Co-IP) | 多克隆抗体制备 | 抑郁症动物模型 |
| ELISA(酶联免疫吸附法)技术 | Western-blot 实验服务 | 脊髓损伤模型 |
| 生化指标检测 | 蛋白双向电泳实验服务 | 脑外损伤模型 |
| 双荧光素酶报告基因检测 | 原核蛋白表达纯化 | 骨神经损伤模型 |
| 染色质免疫共沉淀(ChIP) | 真核蛋白表达纯化 | 心肌缺血模型 |
| GST pull Down | ITRAQ定量蛋白质组学 | 心力衰竭模型 |
| SLAC蛋白组学 | 肺动脉高血压动物模型 | |
| 高血压模型 | ||
| 病毒类 | 实验课题整体外包 | 粥样动脉硬化模型 |
| 过表达/干扰慢病毒包装纯化 | 整体课题外包 | 大脑中动脉阻塞模型 |
| 过表达/干扰腺病毒包装纯化 | 细胞整体实验外包 | 慢性之气管炎模型 |
| 逆转录病毒包装纯化 | 动物整体实验外包 | 过敏性哮喘模型 |
| 腺相关病毒包装纯化 | 肺炎大鼠模型 | |
| 肝炎-肝硬化-肝癌模型 | ||
| 蛋白芯片 | 原代细胞培养 | 肝纤维化模型 |
| 细胞因子芯片 | 骨髓间充质干细胞培养 | 胆结石模型 |
| 生长因子芯片 | 脂肪干细胞培养 | 急性胰腺炎模型 |
| 信号通路磷酸化水平检测芯片 | 心肌成纤维细胞培养 | 急性肾衰竭模型 |
| BioPlex悬浮芯片 | 软骨细胞培养 | 体内血栓模型 |
| 生长因子芯片 | 血管内皮细胞培养 | 关节炎模型 |
| 炎症因子芯片 | 神经元细胞培养 | I型和II型糖尿病模型 |
| 血管生成因子芯片 | 内皮组细胞原代培养 | 裸鼠成瘤 |
| 凋亡因子芯片 | 基因编辑动物 | |
| 趋化因子芯片 | 电生理相关服务 | 动物整体实验服务 |
| HuProt TM 20K人类蛋白组芯片 | 膜片钳实验 | |
| 细胞生物学 | 高通量测序 | 代谢组学 |
| 细胞原代培养 | mRNA测序 | 气相色谱GC/MS |
| MTT检测 | LncRNA测序 | 液相色谱LC/MS |
| 细胞凋亡检测 | 全基因组测序 | 核磁共震NMR |
| 细胞周期检测 | RNA-Seq测序 | |
| 细胞克隆形成实验 | 外显子测序 | 影像学相关实验 |
| Transwell细胞迁移/侵袭 | 16s扩增子测序 | Micro-CT |
| 流式分选 | Small RNA测序 | 小动物活体成像 |
| CCK8/XTT检测 | 宏基因组测序 | 核磁共振 |
| 台盼蓝检测细胞活性 | 单细胞测序 | PET-CT |
| 药物筛选细胞学实验 | circleRNA测序 | |
| 细胞粘附性检测 | 甲基化测序 | 基因编辑动物 |
| 细胞划痕实验 | 条件性敲除小鼠/大鼠 | |
| 细胞生物学整体实验 | 全基因敲除小鼠/大鼠 | |
| 细胞成管实验 | ||
| 病理类 | CRISPR/Cas9细胞敲除/敲入 | 基因芯片 |
| 扫描电镜 | 基因定点突变细胞系 | LncRNA芯片 |
| 透射电镜 | 单基因敲除细胞系 | miRNA芯片 |
| HE染色 | 多基因敲除细胞系 | mRNA芯片 |
| 免疫组化 | 目的基因敲入细胞系 | 甲基化芯片(限人和小鼠来源样本) |
| Tunel(原位末端凋亡法)检测 | 报告基因敲入细胞系 | SNP芯片(限人和小鼠来源样本) |
| 激光共聚焦 | miRNA/LncRNA敲除细胞系 | |
| 免疫荧光 | ||
| Masson染色 | CRISPR/Cas9动物敲除/敲入 | 科研方案设计与SCI相关服务 |
| 原位杂交 | 基因敲除大鼠/小鼠 | 科研文献论著翻译 |
| 荧光原位杂交 | 基因敲入大鼠/小鼠 | SCI论文翻译润色服务 |
| 特殊染色(PSA、茜素红、阿尔新蓝等) | 临床实验/科研实验设计方案指导 | |
| 行为学检测 | 药物筛选服务项目 | 药效学评价 |
| 水迷宫实验 | 高通量自动药物筛选平台 | 神经系统药物药效学评价 |
| 旷场实验 | 细胞高内涵药物筛选平台 | 抗肿瘤药物药效学评价 |
| 重复性刻板行为检测 | 蛋白质组学靶标研发平台 | 心血管系统药物药效学评价 |
| 动物跑台检测 | 分子药理研究平台 | 泌尿系统药物药效学评价 |
| 强迫游泳 | 生物膜片钳药物筛选平台 | 内分泌系统药物药效学评价 |
| 常规药物体外筛选 | 抗炎免疫药物药效学评价 |
【本平台合作项目】
分子生物学、细胞生物学、基因敲出/入、模式动物、SPF动物保种、病理学检测、免疫学检测、影像学检测、原代培养、细胞药筛、CRISPR/Cas9基因编辑、基因芯片、高通量测序、蛋白组学、代谢组学、高通量高内涵筛选、药效学评价、药理毒理学实验、慢病毒包装与稳转株建立、SiRNA与纳米载药、ChIP、CO-IP、生物信息学分析、知识产权服务!
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验技术产业化研发的专业人士共同创立的新型科技企业,公司专注于向国内生命科学研究、生物技术产业研发及医学临床提供全方位现代实验技术服务 。 团队于2003年组建,立足于深厚的分子生物学背景和扎实的科研实验技术服务基础,立命于终身为祖国的科研工作者提供全方位实验技术服务,并孜孜不倦地打造出我们自己研发生产的、比国际一流品牌产品还过硬的科研产品民族品牌,为国家科学技术研究和人民身心健康事业添砖加瓦!经过几年来的不懈努力,公司已建立了涵盖分子遗传学、细胞生物学、蛋白组学、免疫学 、信号传导和神经生物
创刊 3.代谢组学的应用与发展 3.1 代谢组学促进多学科,多领域交叉发展 代谢组学的不断发展,促使分子分离和检测仪器,结构解析的制造商以及相关科学家们需要不断地研发出各种针对代谢组学的硬件、软件和技术支持。也就意味着需要不同领域和学科的技术支持,特别是基于分析化学的结构解析方面。同时,在代谢组学的发展中至关重要的是基于计算机科学(程序语言)的大数据处理和分析。因此,代谢组学的发展离不开多科学、多领域的技术发展。 3.2 代谢组学在医学领域中的应用 新药的筛选和开发:新药研发存在风险高
色谱与质谱联合而达到检测大分子物质的目的。 3.代谢组学发展趋势 代谢组学是定量描述生物内源性代谢物对内外因变化应答规律的科学,能够直接反映生命体的终端和表型信息,近年来在疾病诊断和分型、生物标志物发现、药物研发、基因功能解析、代谢途径及调控机理等领域发挥着重要作用。从代谢组学和脂质组学逐年发表的 SCI 文章(图 2)可以看出,代谢组学发展迅猛。 图 2 | 代谢组学在“Web of Science 核心合集”逐年发表的文章统计图 检索日期:2020 年 5 月 3 日,检索关键
 技术资料
技术资料暂无技术资料 索取技术资料