多糖多酚植物RNA提取试剂盒
保存条件:4℃保存,保质期 2 年。DNase I 请置于-20℃保存。
产品内容:
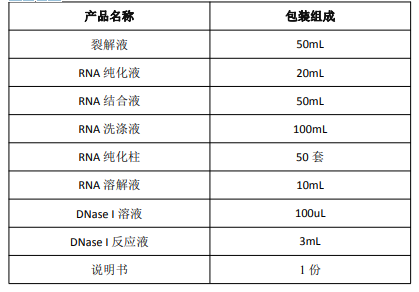
产品说明:植物 RNA 快速提取试剂盒适用于绝大多数植物(包含多糖多酚复杂植物样本)RNA 提取,可以简单快速地从各种来源的植物组织中纯化高质量的总 RNA。纯化好的总 RNA 可用于 mRNA 分离,RT-PCR,Northern 杂交等下游分子实验。
操作步骤:(样品裂解,样品纯化,RNA 收集)
离心条件均优先选择 4℃,室温离心也可以。
一:样品裂解
1. 液氮研磨法
取 1mL 裂解液加入 1.5mL 离心管中。将 100mg 植物种子用液氮研磨成粉末,将其转移到含有裂解液的离心管中,立即剧烈振荡 20 秒后用枪头吹打混匀或涡旋震荡使样本充分裂解。
注意:低温可能导致裂解液有白色悬浮物,请置于 65℃水浴充分溶解后使用。
裂解液含巯基乙醇,请于通风橱内操作。
二:样品纯化
1. 将裂解物 12,000rpm 离心 2-3min,吸取上清 1mL 到 1.5mL 离心管。
2. 在上清中加入 0.3 mL 的 RNA 纯化液 和 0.2 mL 自备氯仿,在振荡器上振荡30 秒,溶液呈均匀的乳浊状。
注意:如样品简单,此步可省略。具体操作为:吸取上清 1mL,继续 12,000 rpm离心 10min,取上清后接步骤(二,4)加等体积 RNA 结合液,上纯化柱。
3. 12,000rpm 离心 3-5min,取上清到新的 1.5mL 离心管中(避免触及分层界面,下层会有大量 DNA 和蛋白污染,避免污染。)
4. 上清中加入等体积的 RNA 结合液,颠倒混匀,分两次加入同一个 RNA 纯化柱中(如有絮状物或沉淀产生,一并加入纯化柱中)。12,000rpm 离心 1min,弃穿透液。
5. 在纯化柱中加入 0.5mL RNA 洗涤液,室温 12,000rpm 离心半分钟,弃穿透液。重复洗涤一次。(洗涤液使用后拧紧瓶盖,防止挥发)
6. 如需去除 DNA 污染,参照步骤(四)可选步骤,用 DNase I 处理。
三:RNA 收集
1. 将结合有 RNA 的纯化柱 12,000rpm 离心 1min,甩干乙醇。(乙醇的残留将会降低洗脱效果和影响下游实验,或者适当延长离心时间,将有助于乙醇的去除)
2. 弃收集管,将柱芯转移到 1.5mL 的 RNase-free 离心管中(自备),加入30-50uLRNA 溶解液,室温放置 1 分钟,12,000 rpm 离心 1 分钟洗脱 RNA。得到的 RNA 可直接用于后续实验或者 -80℃ 存放。
3. 如果要提高 RNA 产量,加入 30-50uLRNA 溶解液重复洗脱一次,合并两次穿透液;如果要提高 RNA 浓度,使用第一次的洗脱液 加回到吸附柱中重复洗脱。
注意:建议 RNA 用于下游实验之前,先进行质量检测。经变性琼脂糖凝胶电泳后,会有清晰的 28S 和 18S 条带,以及中间弥散的 mRNA 条带,其中 28S 条带是18S 条带亮度的 1.5-2 倍。有时还包括跑在最前面的较暗的 5S 条带。如果条带不清晰或者弥散,可能是提取过程中或者材料保存过程中 RNA 发生了降解。小于200bp 的 RNA 分子不能有效结合到吸附柱上。A260/A280 比值 1.8~2.0 对应 RNA纯度 90-100%之间。
四 .DNA 清除(可选步骤)
1.接样品纯化步骤(二,5)。
DNase I 工作液配置:取 RNase-free 离心管,加入 DNase I 反应液 48uL,
DNase I 溶液 2uL。吹打混匀。(DNase I 置于-20℃保存)
2.将 DNase 工作液在 37℃预热 1 分钟,然后全部加入到 RNA 纯化柱中,室温放置 2 分钟。
注意:2 分钟一般足够降解大多数情况下的 DNA 污染。 如果 DNA 没有彻底降解(可能由于样品中残留的杂质抑制了 DNase 的活性),此步骤可以延长到 5 分钟或 10 分钟。
3.直接在纯化柱中加入 0.7mLRNA 洗涤液,室温离心半分钟,弃穿透液。
4.接 RNA 收集步骤(三)
特别提示:本公司的所有产品仅可用于科研实验,严禁用于临床医疗及其他非科研用途!
