万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
111
- 英文名:
α-L-阿拉伯呋喃糖苷酶α-L-Af测试盒
- 保质期:
12个月
- 供应商:
上海酶联生物科技有限公司
- 保存条件:
避光,低温保存
- 规格:
100管/48样
α-L-阿拉伯呋喃糖苷酶α-L-Af测试盒
微量法
注 意:正式测定之前选择2-3个预期差异大的样本做预测定。

测定意义:
α-L-Af 是一种能够水解非还原呋喃阿拉伯糖残基的糖苷酶类,使细胞壁阿拉伯半乳聚糖、阿拉伯甘露聚糖等中性糖不断解离,促进果胶的增溶和降解。由于果实成熟过程中常常伴随着阿拉伯糖的丧失,该酶活性在果实成熟软化中的研究具有重大意义。
测定原理:
α-L-Af分解对硝基酚阿拉伯呋喃糖苷生成对-硝ji苯酚,后者在400nm有大吸收峰,通过测定吸光值升高速率来计算α-L-Af活性。
自备用品:
酶标仪/可见分光光度计、台式离心机、水浴锅、可调式移液器、96孔板/微量石英比色皿、研钵、冰和蒸馏水。
试剂组成和配制:
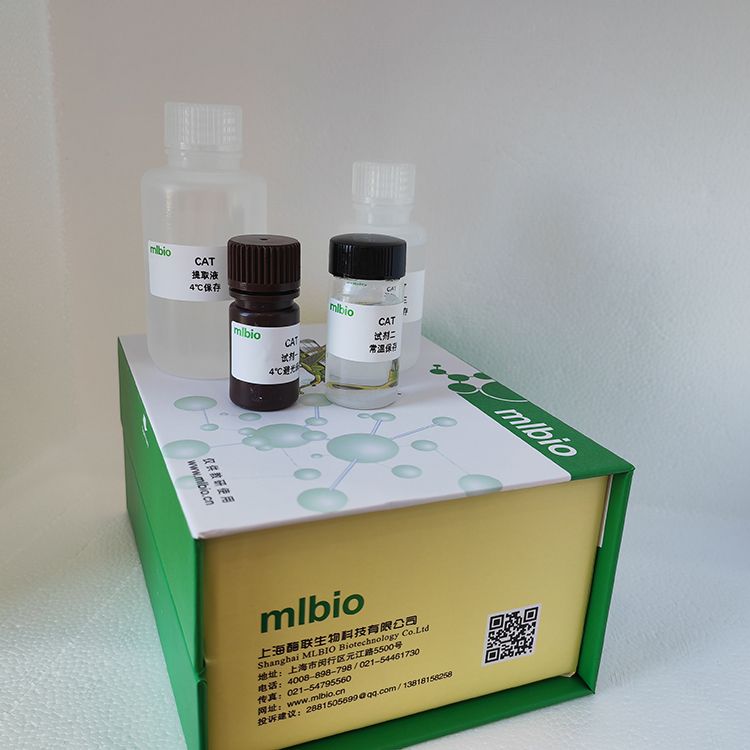
提取液:液体100mL×1瓶,4℃保存。
试剂一:粉剂×1瓶,-20℃保存;临用前加入2.5mL蒸馏水,充分溶解备用;用不完的试剂仍-20℃保存。
试剂二:液体4mL×1瓶,4℃保存。
试剂三:液体13mL×1瓶,4℃保存。
粗酶液提取:
1、细菌或培养细胞:先收集细菌或细胞到离心管内,离心后弃上清;按照细菌或细胞数量(104个):提取液体积(mL)为500~1000:1的比例(建议500万细菌或细胞加入1mL提取液),超声波破碎细菌或细胞(冰浴,功率20%或200W,超声3s,间隔10s,重复30次);15000g 4℃离心10min,取上清,置冰上待测。
2、组织:按照组织质量(g):提取液体积(mL)为1:5~10的比例(建议称取约0.1g组织,加入1mL提取液),进行冰浴匀浆。15000g 4℃离心10min,取上清,置冰上待测。
测定步骤:
1、分光光度计或酶标仪预热30min以上,调节波长至400nm,蒸馏水调零。
2、样本测定(在EP管或96孔板中依次加入下列试剂):
| 试剂名称(μL) | 测定管 | 对照管 |
| 试剂一 | 25 | |
| 蒸馏水 | 25 | |
| 试剂二 | 35 | 35 |
| 样本 | 10 | 10 |
| 试剂三 | 130 | 130 |

α-L-阿拉伯呋喃糖苷酶α-L-Af测试盒
α-L-Af活性计算:
a.用微量石英比色皿测定的计算公式如下
标准条件下测定的回归方程为y =0.00585x -0.0027;x为标准品浓度(nmol/mL),y为吸光值。
(1)按样本蛋白浓度计算:
单位的定义:每mg组织蛋白每min产生1nmol对-硝ji苯酚定义为一个酶活性单位。
α-L-Af活性(nmol/min/mg prot)=[(ΔA+0.0027)÷0.00585×V反总]÷(V样×Cpr)÷T
=39.89×(ΔA+0.0027) ÷Cpr
(2)按样本鲜重计算:
单位的定义:每g组织每小时产生1nmol对-硝ji苯酚定义为一个酶活性单位。
α-L-Af活性(nmol/min/g鲜重)=[(ΔA+0.0027)÷0.00585×V反总]÷(W×V样÷V样总)÷T
=39.89×(ΔA+0.0027) ÷W
(3)按细菌或细胞密度计算:
单位的定义:每1万个细菌或细胞每小时产生1nmol对-硝ji苯酚定义为一个酶活性单位。
α-L-Af活性(nmol/min/104cell) =[(ΔA+0.0027) ÷0.00585×V反总]÷(500×V样÷V样总)÷T
=0.08×(ΔA +0.0027)
Cpr:样本蛋白质浓度,mg/mL;V反总:反应体系总体积,0.07mL;V样:加入反应体系中样本体积,0.01mL;V样总:加入提取液体积,1mL;W:样本质量,g; 500:细胞或细菌总数,500万;T:反应时间,30min。
b.用96孔板测定的计算公式如下
标准条件下测定的回归方程为y = 0.0039x -0.0027;x为标准品浓度(nmol/mL),y为吸光值。
(1)按样本蛋白浓度计算:
单位的定义:每mg组织蛋白每小时产生1nmol对-硝ji苯酚定义为一个酶活性单位。
α-L-Af活性(nmol/min/mg prot)=[(ΔA+0.0027) ÷0.0039×V反总]÷(V样×Cpr)÷T
=59.83×(ΔA+0.0027) ÷Cpr
(2)按样本鲜重计算:
单位的定义:每g组织每小时产生1nmol对-硝ji苯酚定义为一个酶活性单位。
α-L-Af活性(nmol/min/g鲜重)=[(ΔA+0.0027)÷0.0039×V反总]÷(W×V样÷V样总)÷T
=59.83×(ΔA+0.0027) ÷W
(3)按细菌或细胞密度计算:
单位的定义:每1万个细菌或细胞每小时产生1nmol对-硝ji苯酚定义为一个酶活性单位。
α-L-Af活性(nmol/min/104cell) =[(ΔA+0.0027) ÷0.0039×V反总]÷(500×V样÷V样总)÷T
=0.12×(ΔA +0.0027)
Cpr:样本蛋白质浓度,mg/mL;V反总:反应体系总体积,0.07mL;V样:加入反应体系中样本体积,0.01mL;V样总:加入提取液体积,1mL;W:样本质量,g; 500:细胞或细菌总数,500万;T:反应时间,30min。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验C5 H10 O5 。戊糖的一种。 D-阿拉伯糖除含于一部分植物糖苷中外,几乎在自然界中是找不到的,而 L-阿拉伯糖则以植物界为中心广泛分布着,在松或杉的心材中呈结合状态或游离状态存在。植物树胶多数也是以 L-阿拉伯糖为主要成分的多糖。一般植物细胞作为细胞外间质成分而合成分泌的杂多糖常含有 L-阿拉伯糖。与 D-木糖是 4-差向异构体的关系,在生物体内经由α -D-葡萄糖 -1-磷酸→ UDP-D-葡萄糖→ UDP葡糖醛酸→ UDP- D-木糖,由特异的差向异构酶的反应生成 UDP
组。作者随后构建了体内、体外银屑病模型,用 L- 薄荷醇处理,出现了类似于 PP6 的结果,即 L- 薄荷醇能促进角质形成细胞中 Hes1 蛋白的表达,但不影响其转录。进一步研究发现,L- 薄荷醇能够通过抑制蛋白酶体对 Hes1 蛋白的降解进而增加 Hes1 蛋白的水平。 图 4 L- 薄荷醇靶向角质形成细胞中的 Hes1 并且上调其表达 作者使用 K5. Hes1fl/fl 和 Hes1fl/fl 小鼠作为研究工具,发现表皮细胞缺失 Hes1 能加重 IMQ 诱导的小鼠银屑病表型,即 K5
L-氨基酸氧化酶,存在于肾脏 肝脏 霉菌、蛇毒、细菌等中,为直接氧化 L-氨基酸的需氧性脱氢酶。 EC1. 4. 3. 2.如果不存在过氧化氢酶,则以 H2 O2 脱羧形成酮酸。 其辅酶是 FMN或 FAD。底物专一性广泛,能很好地氧化亮氨酸、甲硫氨酸等,但不作用于天冬氨酸、谷氨酸、甘氨酸等。但是,鸟类肝脏的酶对碱性氨基酸具有专一性。不过,由于活性低,因此动物的酶对氨基酸代谢是否有意义尚属疑问。但对 L-α -羟酸的氧化活性
 技术资料
技术资料