- 视频课件
- 讲师介绍
- 视频介绍
讲师介绍
李晴晴
视频介绍
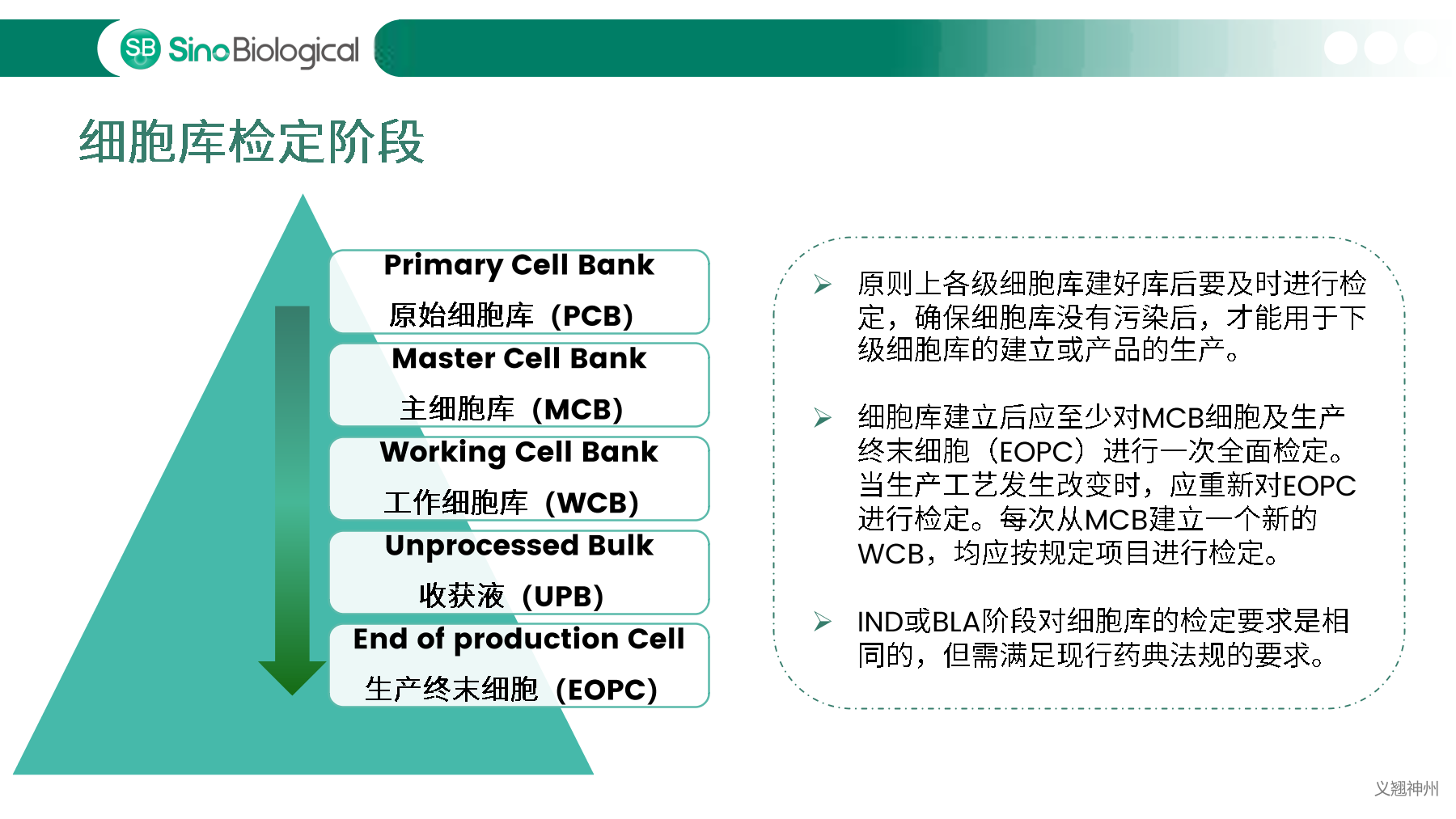
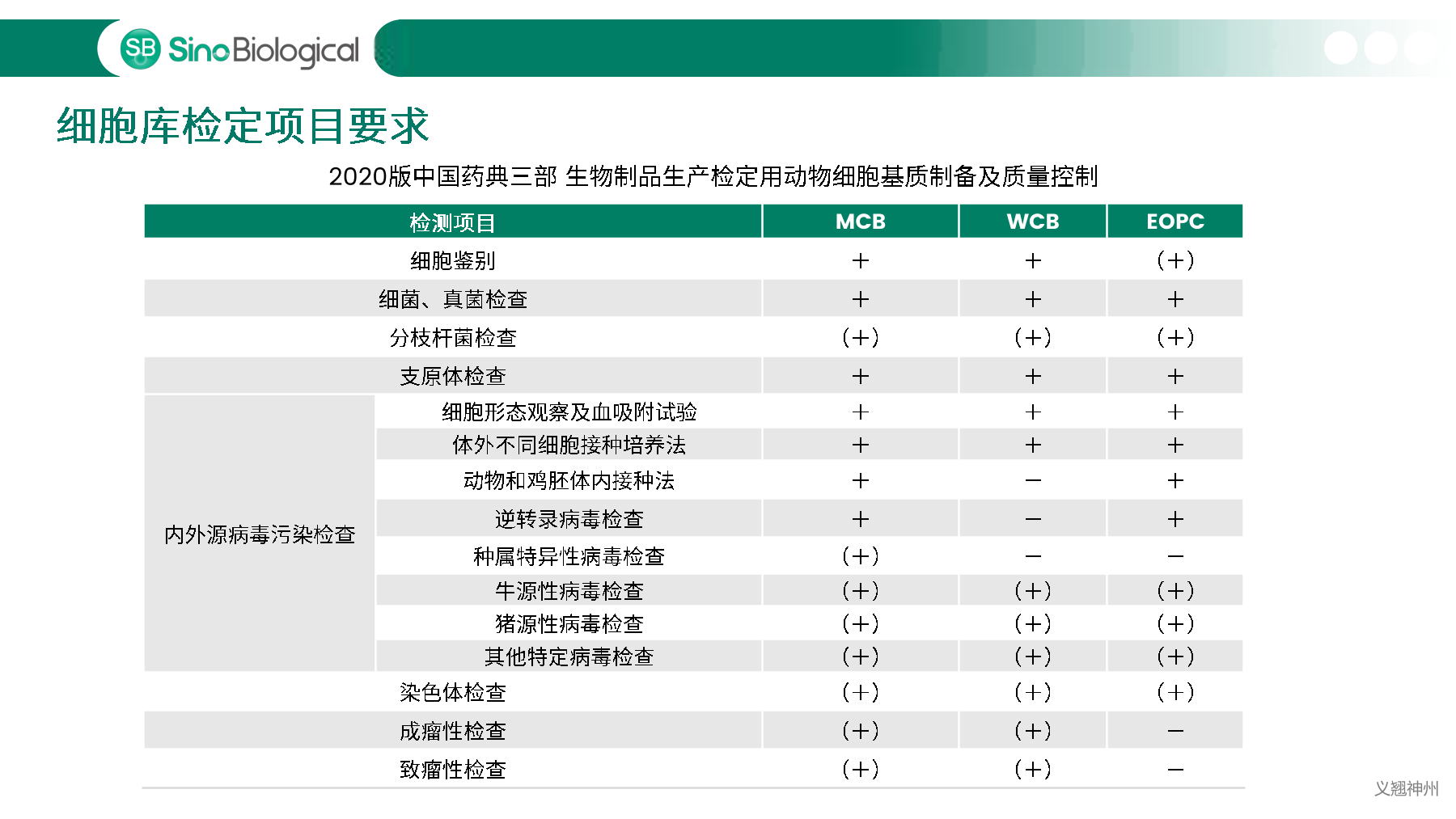
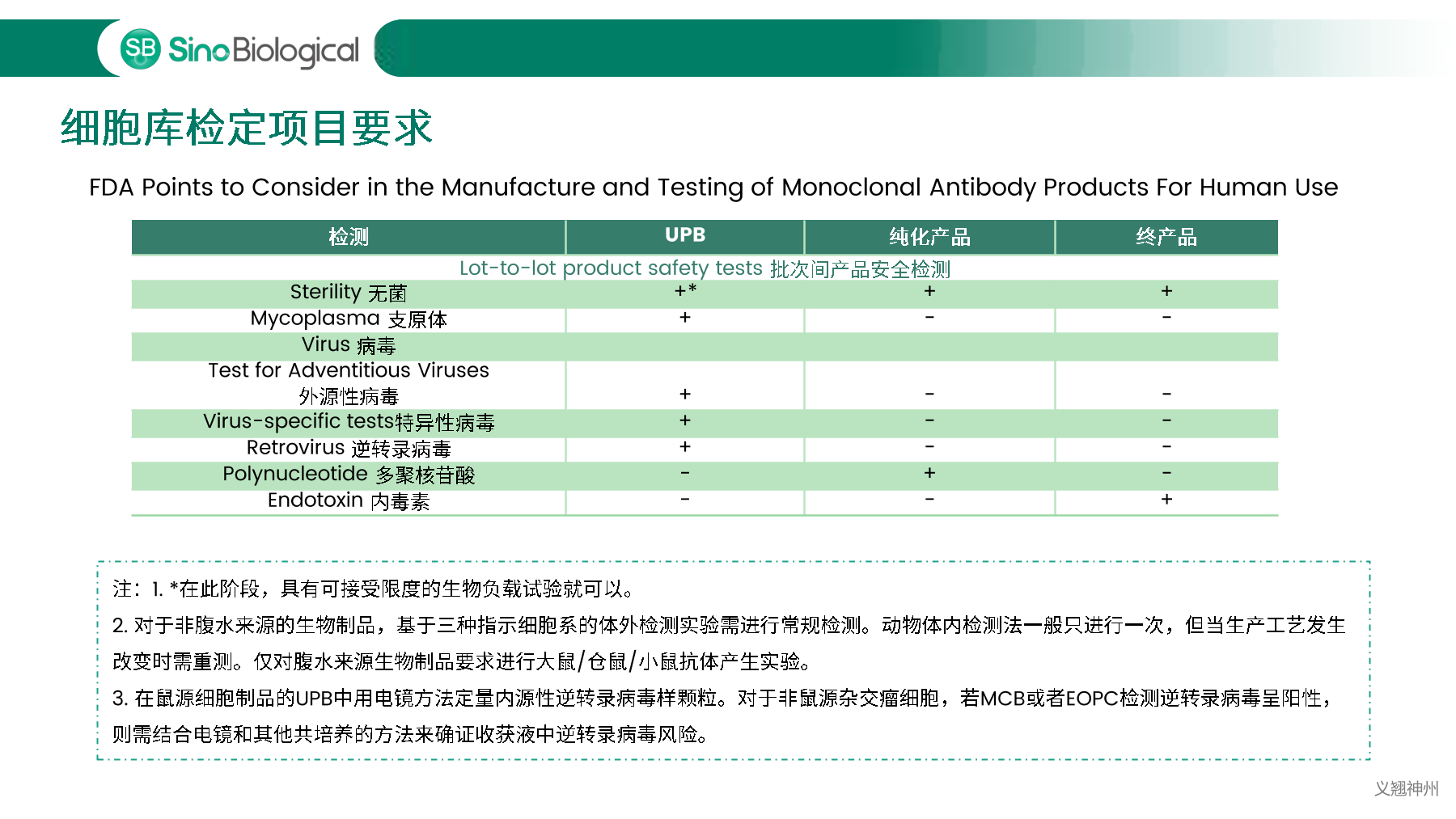
细胞库是生物制药的源头,重中之重,需要一份详尽的细胞库检测规范和工艺,确保所生产的生物制品安全性、纯度、理化指标和药效指标符合相关法规规定。细胞库可能携带病原微生物,如细菌、真菌、支原体、分枝杆菌、内源性病毒或外界污染的病毒,导致生产制备的生物制品含有污染的病原微生物,带来治疗上的安全风险。
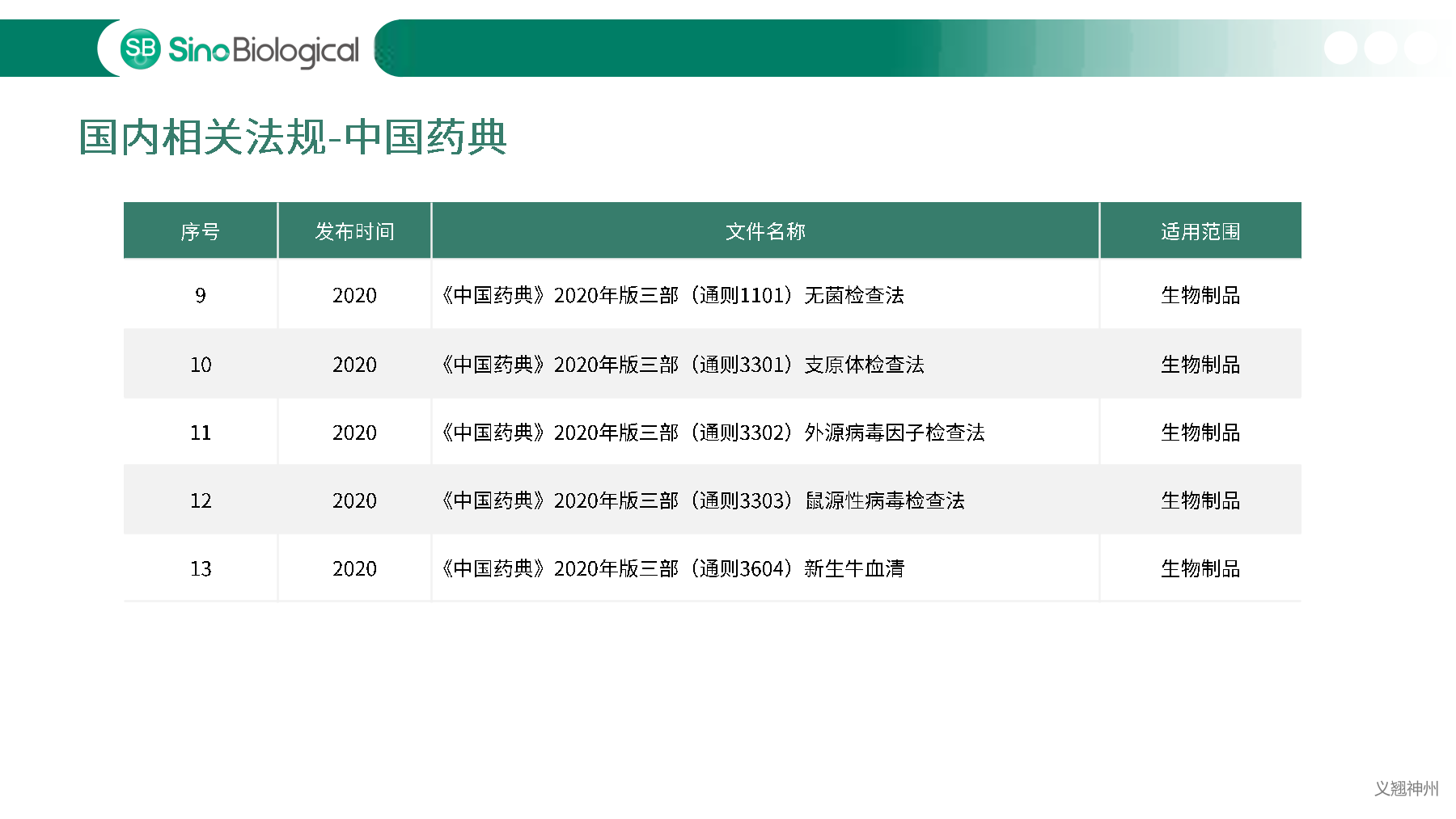
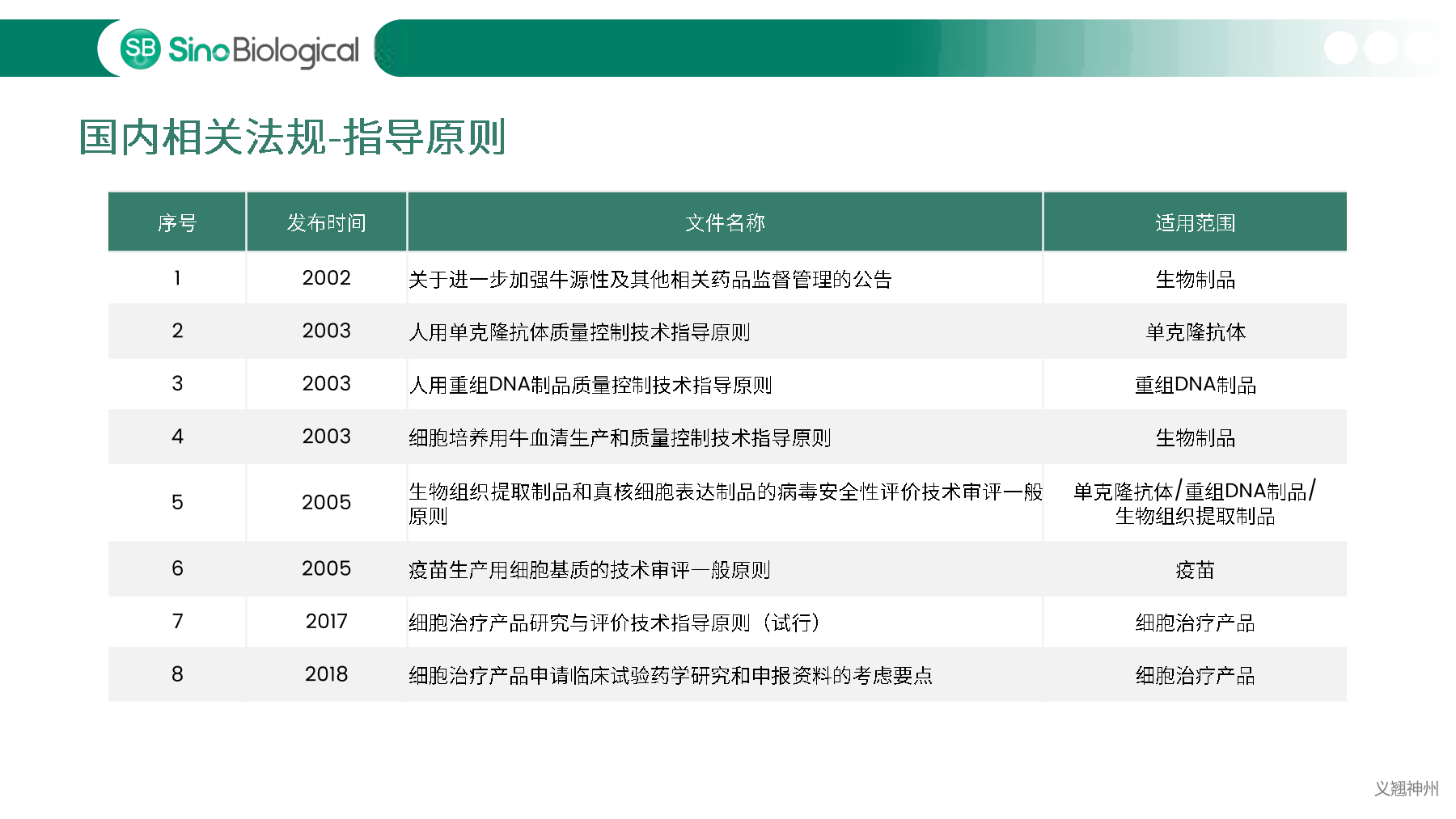
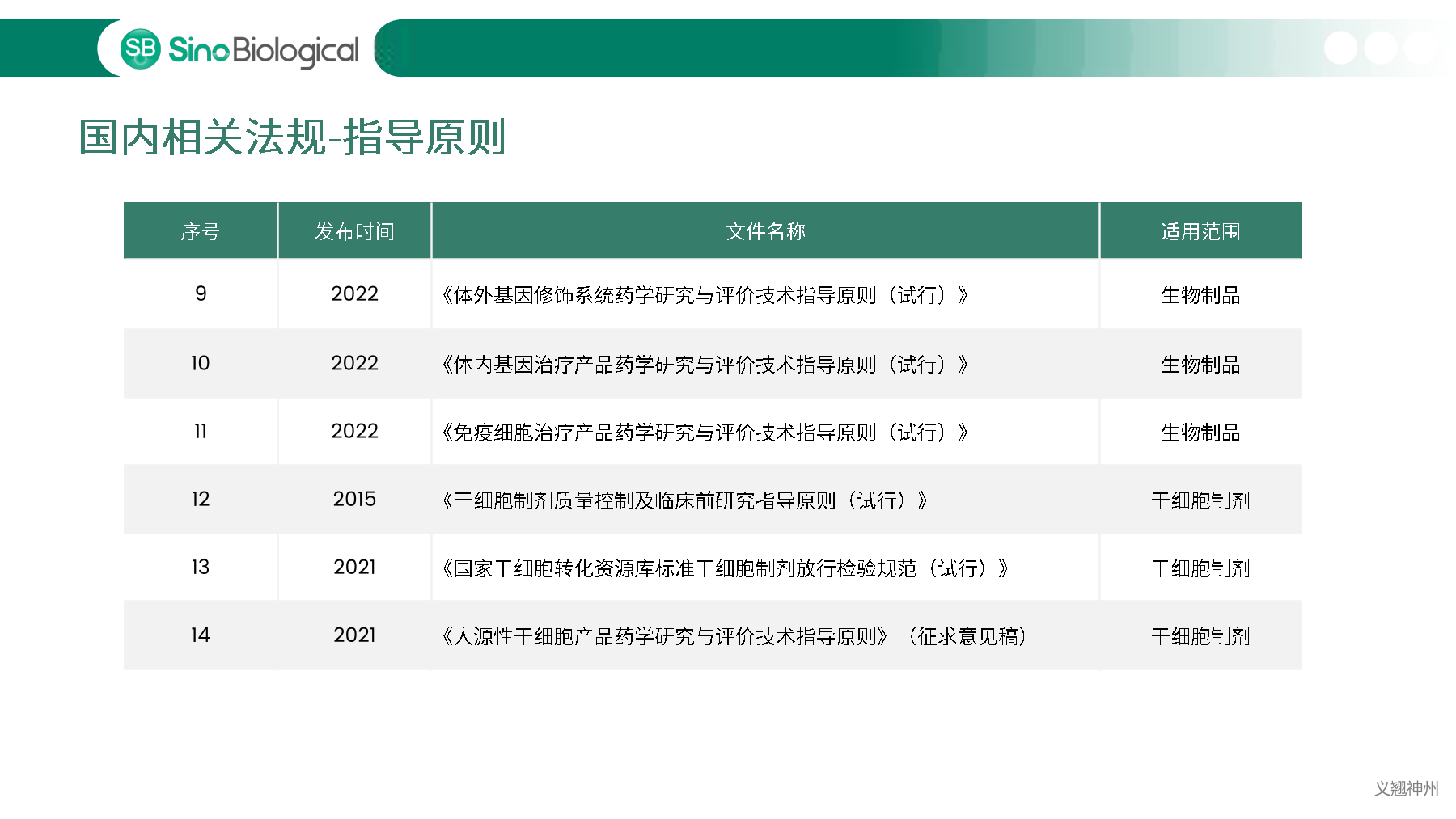
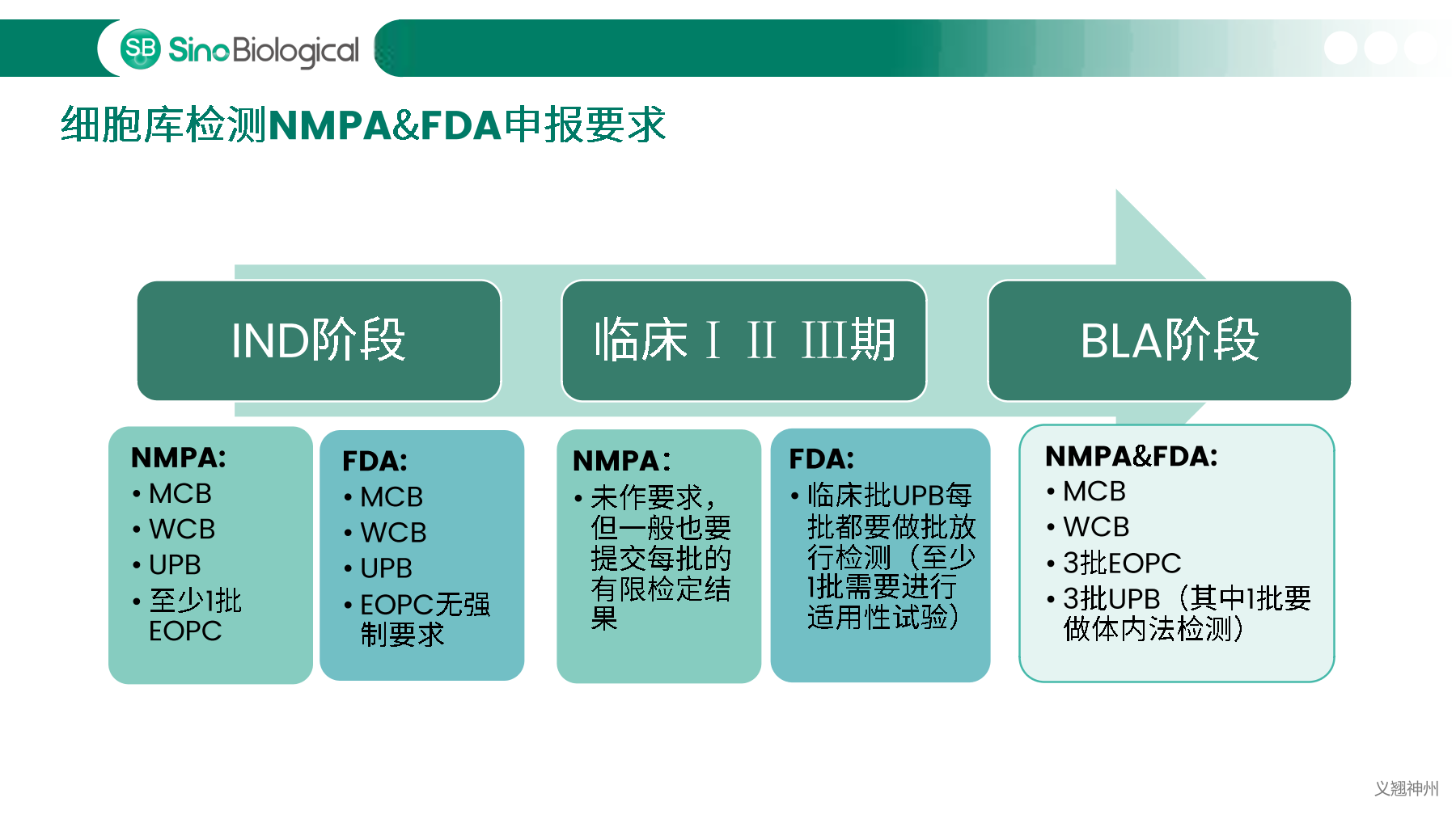
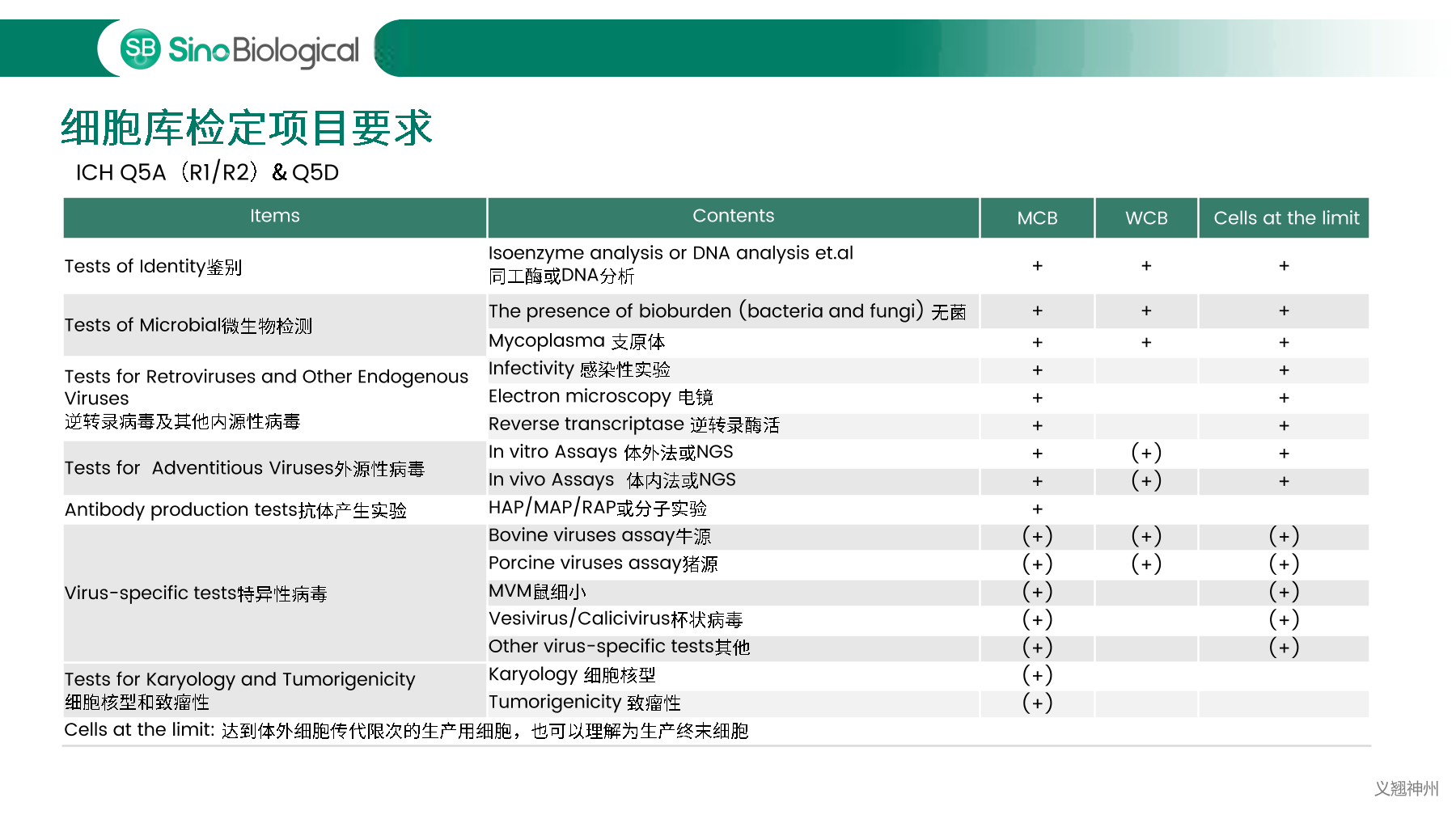
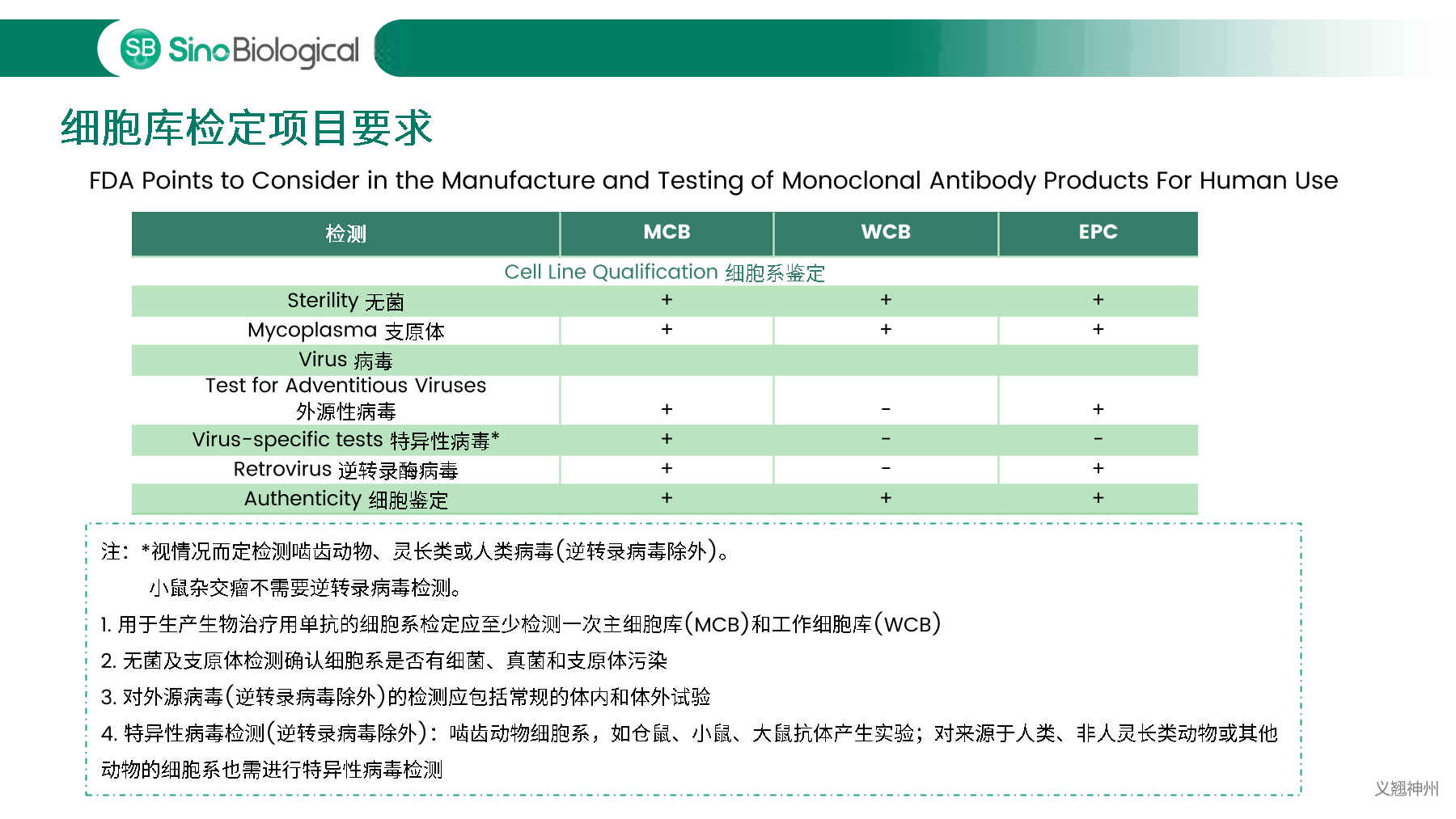
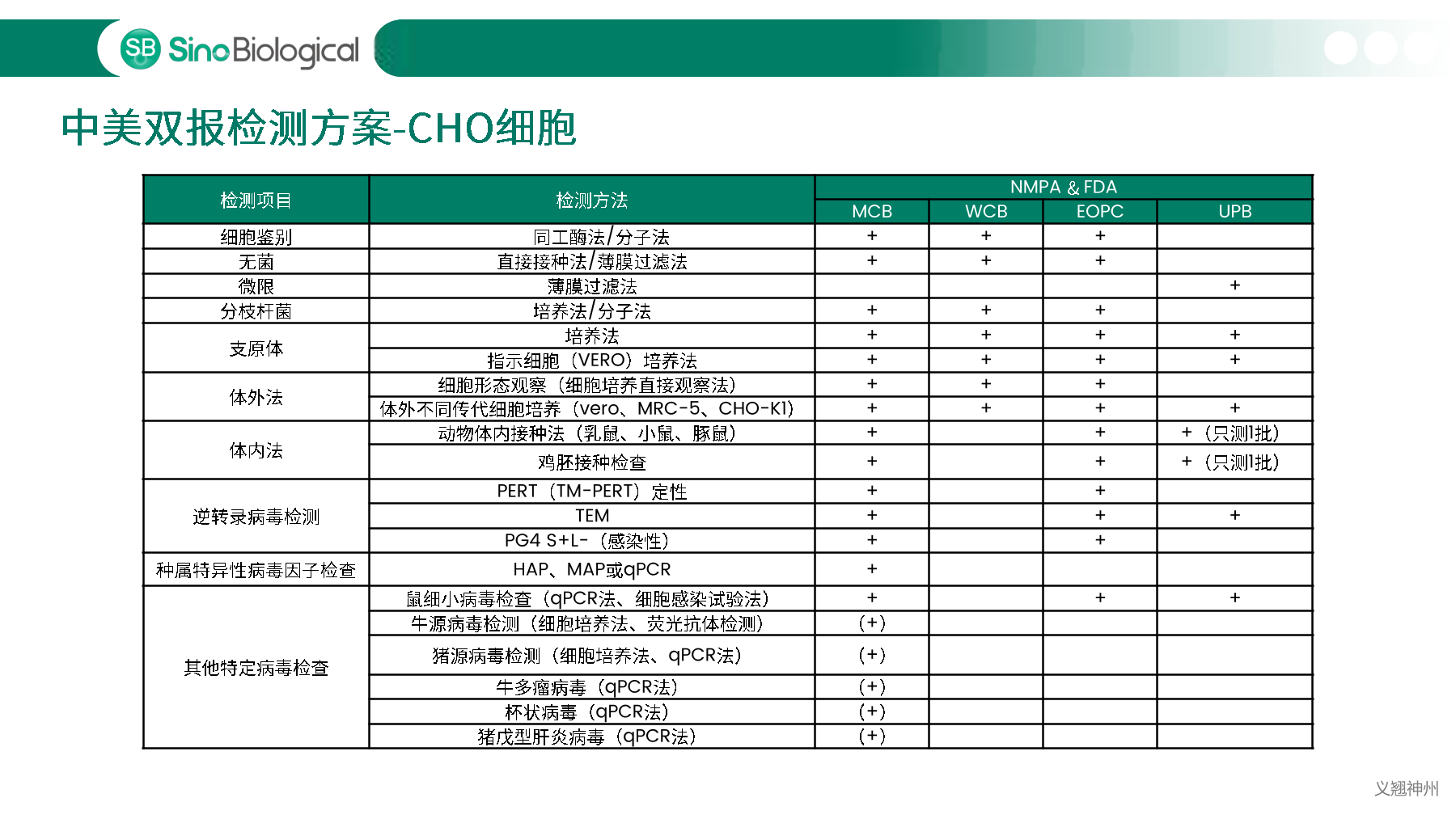
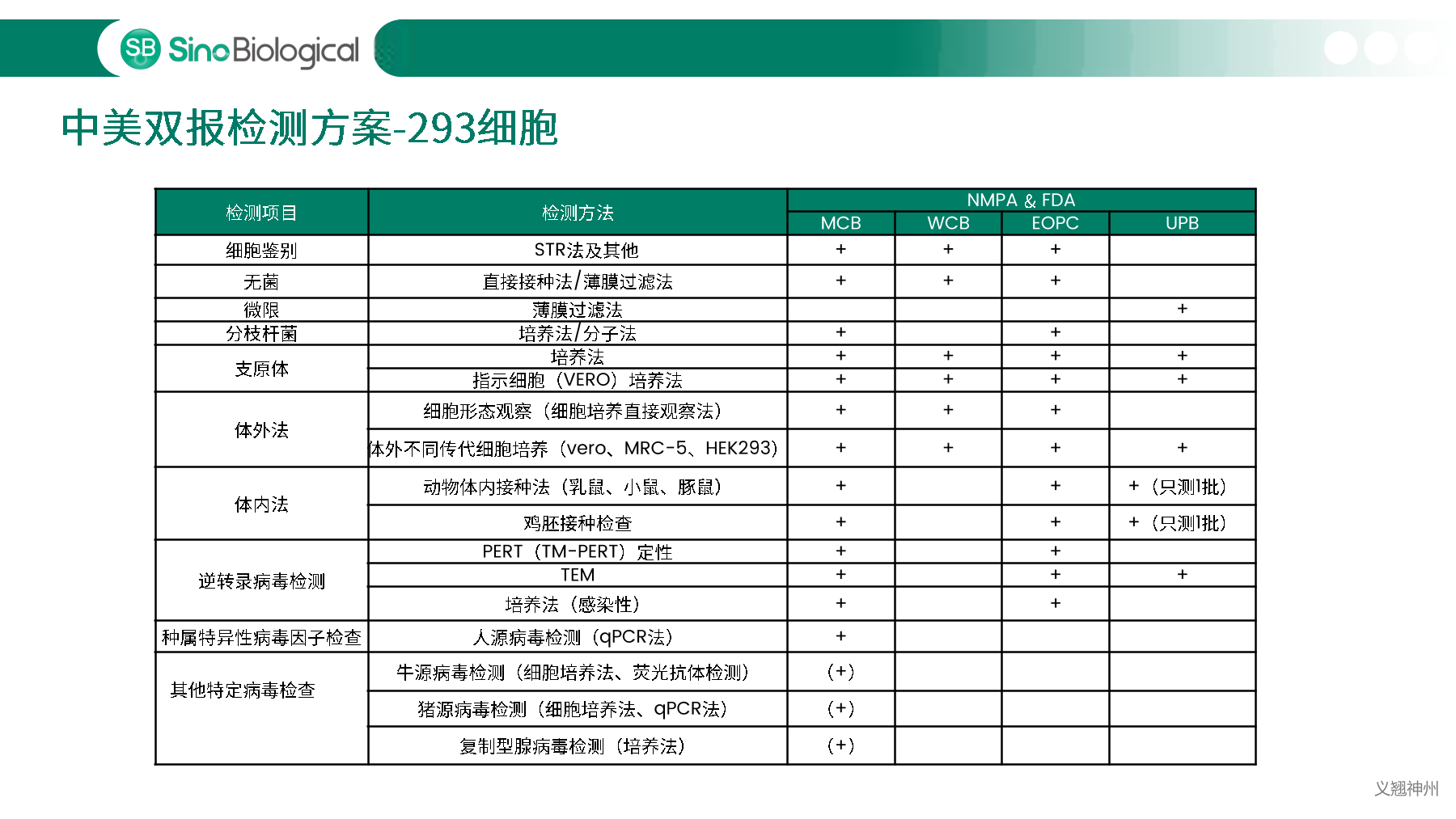
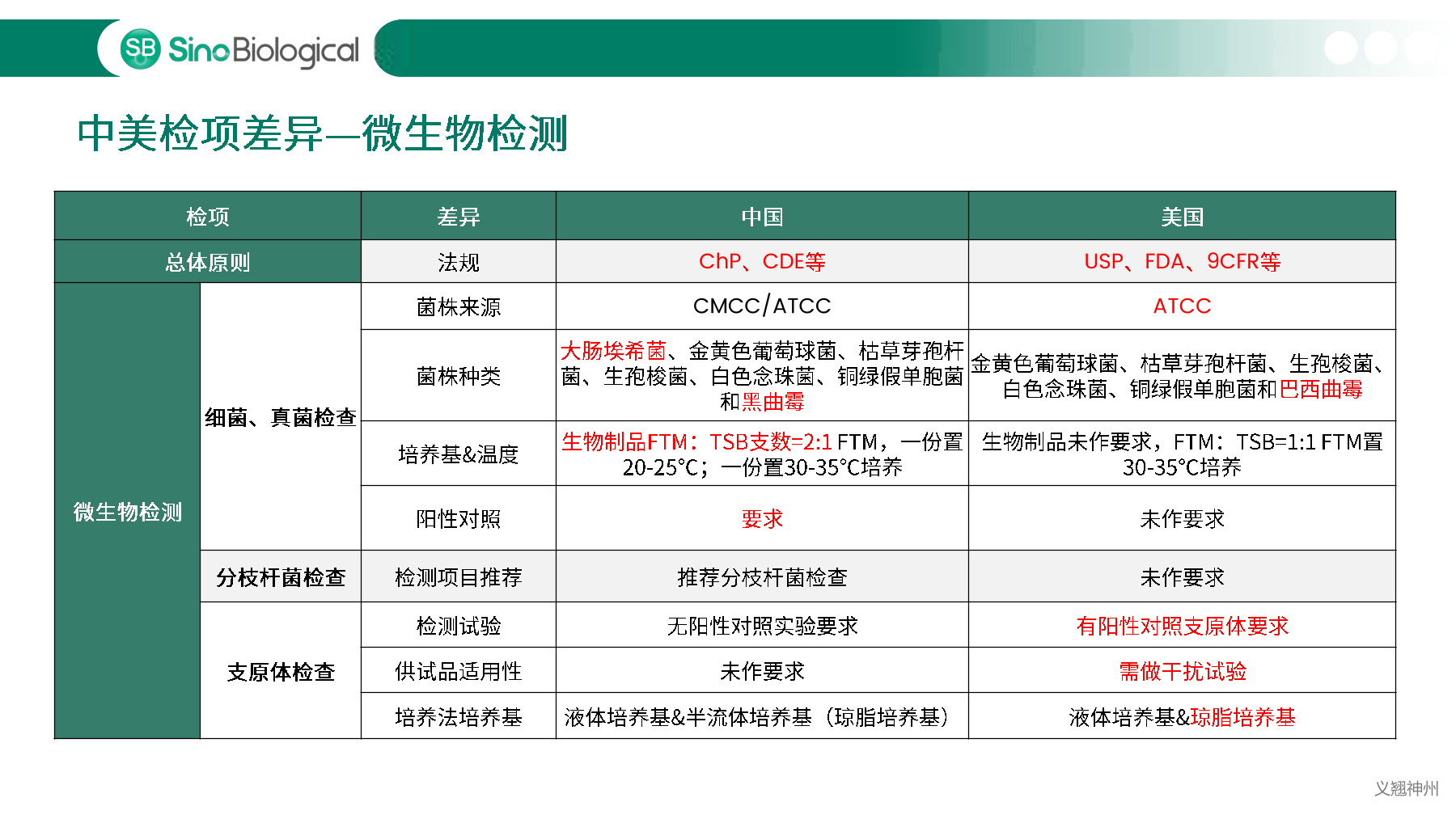
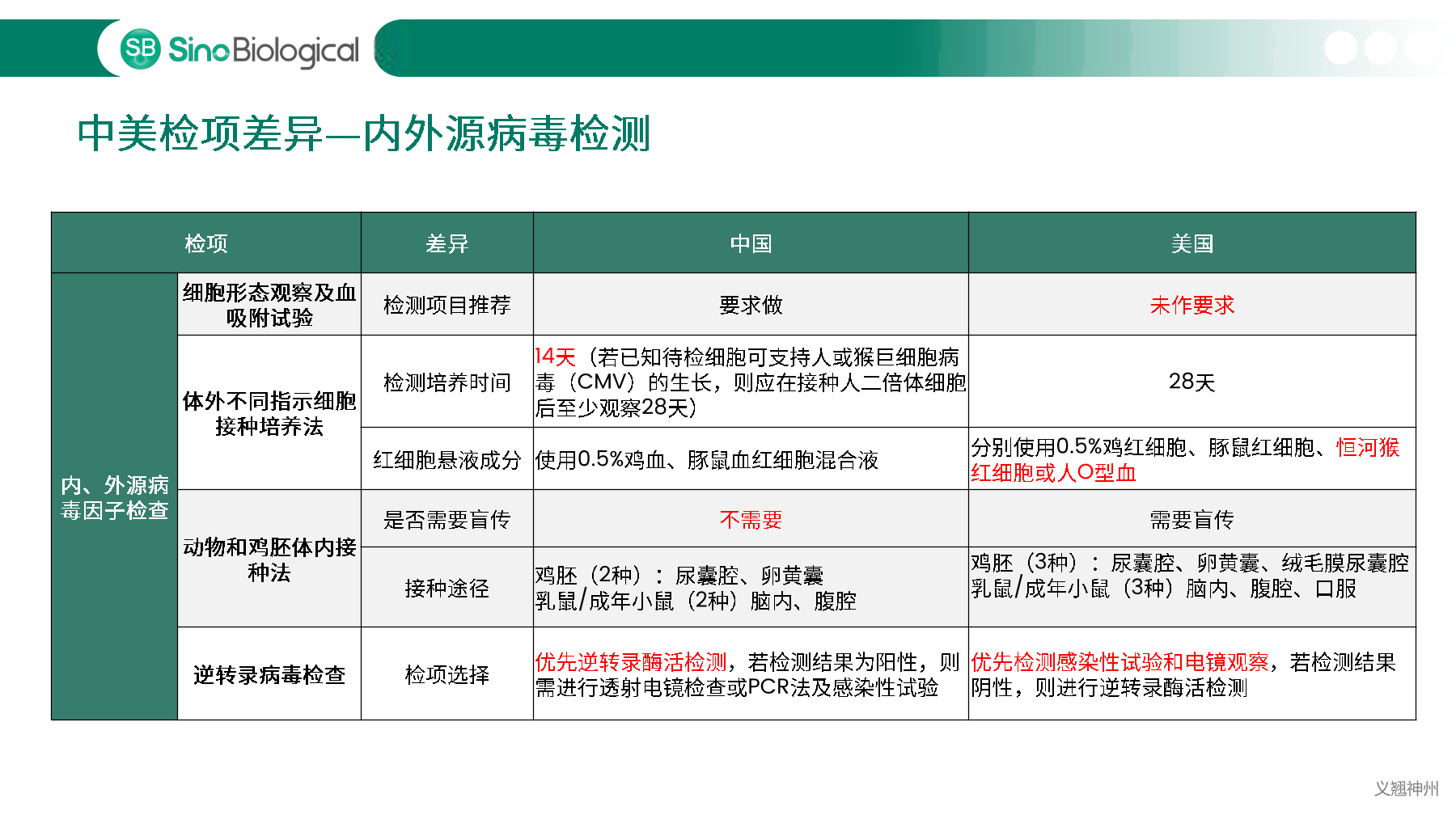
中国、美国、欧洲等药典明确规定必须对细胞库以及生产过程中相关的生物制品进行充分检定,确保细胞库没有污染后,才能用于生物制品的生产。主细胞库(MCB)、工作细胞库(WCB)、生产终末细胞(EOPC)以及收获液(UPB)等都是细胞库检定的重点范畴。随着中国自2017年加入ICH,中美双报已经成为国内各大药企药物申报的新趋势,国内外法规对于细胞库及收获液等检定要求存在一定的差异,细胞库检定如何满足中美双报也是大家讨论的热点。
本次讲座将围绕细胞库检定中美双报的策略以及具体的方法差异,与大家分享双报的要点,为相关制药企业的技术人员更好的了解和掌握细胞库中美双报提供技术指导。