|
代谢重编程是癌症的标志。然而,三阴性乳腺癌(TNBC)代谢产物的系统表征仍然缺乏。2022年02月01日,来自复旦大学附属肿瘤医院乳腺外科邵志敏教授和江一舟教授团队在国际知名期刊Cell Research(IF=20.507)上发表了题为“Comprehensive metabolomics expands precision medicine for triple-negative breast cancer”的研究论文。该研究分析了330例TNBC样本和149例配对正常乳腺组织中的极性代谢组和脂质组,以构建TNBC的大型代谢组图谱。基于代谢组数据对TNBC进行代谢组疾病分型,确定了三个不同的代谢亚型,并筛选到一些关键的亚型特异性代谢物可作为潜在的治疗靶点。该代谢组学数据集可以作为促进TNBC精准治疗的有用公共资源。
研究背景
三阴性乳腺癌(TNBC)是乳腺癌的一个亚群,其定义是缺乏雌激素受体,孕激素受体和人表皮生长因子受体2的表达。TNBC的临床管理是一个巨大的挑战,因为其内脏转移发生率很高,并且缺乏公认的治疗靶点。先前的研究基于转录组学亚型的潜在治疗靶点并未达到理想预期,因此需要寻求对TNBC的更多学科的理解,以便识别新的目标。作为癌症的一个重要标志,TNBC的代谢重编程值得进一步探索。
文章重点基于LC-MS代谢组学分析构建了一个大型代谢组学数据集,用于系统地描述TNBC的代谢组学景观。还证明了三种TNBC代谢组亚型细化了之前定义的TNBC转录组亚型。此外,靶向一些功能代谢产物的生物合成,如S1P和NAAG,可能分别对LAR和BLIS肿瘤的治疗有效。总的来说,该研究阐明了TNBC的代谢组学景观,并可能扩展TNBC的精确医学。
样本选择:330例TNBC样本和149例配对的正常乳腺组织技术策略:代谢组、转录组(先前的研究数据)
研究思路
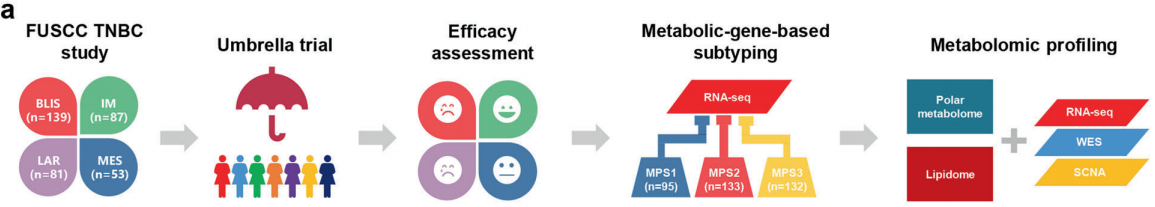

研究结果
使用TNBC队列样本集进行代谢组分析,共注释到594个极性代谢物和1944个脂质。应用Benjamini–Hochberg校正的Mann–Whitney U检验,筛选到452种代谢物(肿瘤中417种上调,35种下调),显示出肿瘤样本和正常样本之间丰度的显著差异(图1a、b)。基于KEGG代谢途径的差异丰度(DA)分析,以研究代谢途径的失调(图1c),研究显示大量参与甘油磷脂代谢、氨基糖和核苷酸糖代谢途径的代谢产物显示出较高的DA评分。此外,应用相似网络融合(SNF)方法探讨TNBC的肿瘤间代谢组学异质性,通过该分析,将TNBC分为三个亚组(图1d)。应用了相似网络融合(SNF)方法探讨TNBC的肿瘤间代谢组学异质性,通过该分析,TNBC可明确分为三个亚组(图1d)。C1亚型以鞘脂和FAs富集为特征;C2亚型以碳水化合物代谢和氧化反应上调为特征(图1e)。与正常组织相比,C3亚型显示出轻微的代谢差异(图1f)。 
图1. 三阴性乳腺癌的代谢组学景观 代谢组与转录组特征联合的综合分析 基于Recon3D数据库分析了极性代谢物丰度与配对代谢基因mRNA表达之间的相关性。重点研究了24个已知的癌症相关基因,这些基因在TNBC中经常发生突变,并应用线性回归模型研究体细胞突变和代谢物丰度之间的关联(图2c)。研究发现PIK3CA突变与FA的丰度呈正相关,与GSSG的丰度呈负相关(图2d)。此外,还研究了染色体区域12p13.33,包括编码SLC6A12/SLC6A13的基因,该基因在细胞膜中作为神经递质转运体发挥作用。研究表明,12p13.33染色体区域的拷贝数与神经递质γ-氨基(GABA)和N-乙酰-天冬氨酸-谷氨酸(NAAG)的丰度呈正相关(图2f)。总之,分析基因组特征和代谢物之间的关联可能为TNBC中代谢重编程的驱动力提供线索。 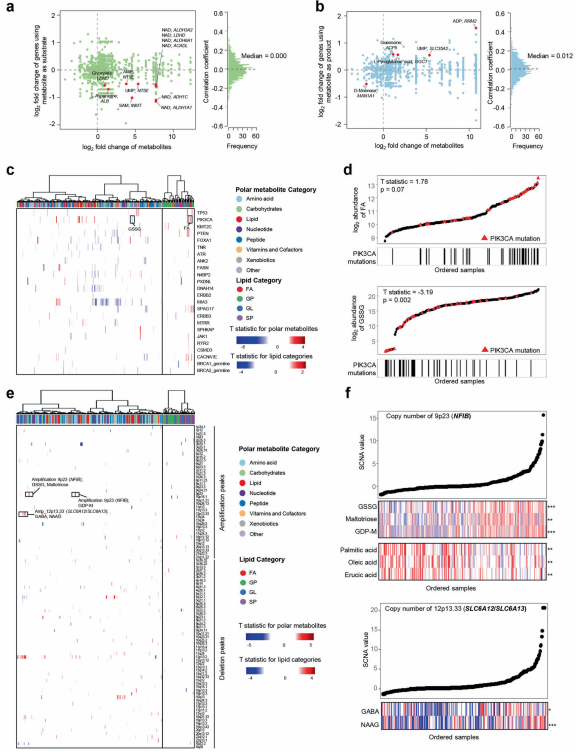
图2. 将代谢组与基因组特征联系起来的系统评估 机器学习实现代谢组数据细化BLIS肿瘤的转录组亚型 进一步探讨代谢组亚型和之前定义的转录组亚型之间的关联。在转录组亚型方面,LAR亚型几乎与代谢组C1亚型重叠;BLIS、免疫调节(IM)和间充质样(MES)亚型主要分为代谢组C2和C3亚型。关于MPS,MPS1亚型与代谢组C1亚型高度一致,而MPS2和MPS3亚型与代谢组C2和C3亚型交错(图3a)。还探讨了代谢组亚型的预后价值,并证明BLIS肿瘤包含两个预后代谢组亚型(C2和C3)。总之,代谢组学分析细化了先前开发的TNBC转录组亚型。在未来的试验中,应考虑将代谢组亚型与转录组亚型结合起来进行进一步研究(图3g)。对于LAR肿瘤,可以根据代谢组C1亚型的特征进一步探索代谢靶点。对于BLIS患者,基于机器学习的代谢组亚型系统可能会将它们分为具有明显复发风险的组别。
图3. 基于机器学习实现通过代谢组学数据细化BLIS肿瘤中的转录组学亚型
LAR亚型中神经酰胺代谢分析显示1-磷酸鞘氨醇(S1P)作为潜在治疗靶点 转录组LAR亚型几乎与代谢组C1亚型重叠,其特点是富含鞘脂代谢相关代谢物。因此该研究分析了鞘脂代谢途径的详细中间产物,以确定LAR肿瘤的关键代谢物。与正常组织和非LAR肿瘤相比,LAR肿瘤的特征是神经酰胺的富集(图4a)。进一步通路分析表明,神经酰胺途径的从头合成和降解在LAR肿瘤中更为活跃,而糖基和磷酸基团的转移没有显著上调(图4b、c)。为了研究LAR肿瘤的潜在治疗策略,研究人员在细胞系和患者源性类器官(PDO)模型中系统地阻断神经酰胺途径从头合成和降解的每一步,研究结果表明,S1P是神经酰胺途径的重要中间产物,在LAR肿瘤中起着至关重要的作用。PF-543(一种SPHK1抑制剂)和FTY-720(也称为芬戈莫德或芬戈利德,一种FDA批准的神经酰胺途径多靶点药物)可能是LAR肿瘤的亚型特异性治疗方法(图4e、f)。 
图4. 对LAR亚型中神经酰胺代谢的分析显示S1P是潜在的治疗靶点 NAAG是BLIS肿瘤中重要的肿瘤促进代谢产物 进一步探索了BLIS肿瘤的重要促肿瘤代谢物。在分析BLIS肿瘤中特异性上调并预测不良预后的代谢物后,确定了NAAG作为潜在候选物(图5a、b)。据报道,两种酶RIMKLA和RIMKLB负责NAAG的产生(图5d)。由于RIMKLB在转录组水平上显著高于RIMKLA,并且与NAAG的丰度呈正相关,我们推测RIMKLB是决定TNBC中NAAG水平的关键酶(图5e、f)。研究人员首先在TNBC细胞系中验证RIMKLB的mRNA表达与NAAG丰度的正相关。RIMKLB和NAAG的作用在体内得到进一步验证。RIMKLB基因敲除可显著降低肿瘤生长,补充NAAG可部分挽救肿瘤生长(图5i-k)。这些数据表明,NAAG是BLIS肿瘤中一种关键的促肿瘤代谢产物,靶向NAAG的生物合成可能是一种可行的治疗策略。
图5. NAAG是BLIS肿瘤中重要的肿瘤促进代谢物 小结 该研究使用这个大型TNBC代谢组学数据集,系统地描述了TNBC的代谢组学景观和异质性。此外,通过结合转录组学和代谢组学数据,确定了TNBC的几个亚型特异性代谢组学治疗靶点。其中,S1P是神经酰胺途径中一种促肿瘤中间产物,在LAR肿瘤中显著富集。此外,还发现NAAG是BLIS肿瘤中一种关键的促肿瘤代谢物,可作为BLIS肿瘤的潜在治疗靶点。该研究将有助于扩大之前基于基因组的TNBC的精准医学研究。 综合代谢组学拓展三阴性乳腺癌的精准医疗期刊名称:Cell Research影响因子:20.507样本选择:TNBC组织和配对的正常乳腺组织技术策略:代谢组学
|