| 近年来,肿瘤免疫学已在降低肿瘤负荷方面取得了长足进步。流式细胞术作为高效的单细胞表征手段,在肿瘤免疫研究中不可或缺。相比于传统流式细胞仪,全光谱流式(FSFC)可高灵敏地收集荧光染料在多激光激发下的全部光谱信息,通过先进的光谱解析算法完成超多色免疫分型,为科研人员提供了更高维度的免疫应答动态监测手段,并大幅提升检测效率。Diana L. Bonilla 等研究者发表于 Frontiers in Molecular Biosciences 的文章,综述了 Cytek® Aurora 在肿瘤免疫生物标志物探索、免疫监控、抗肿瘤药物与疫苗研发、细胞功能研究等领域中的重要应用。¹
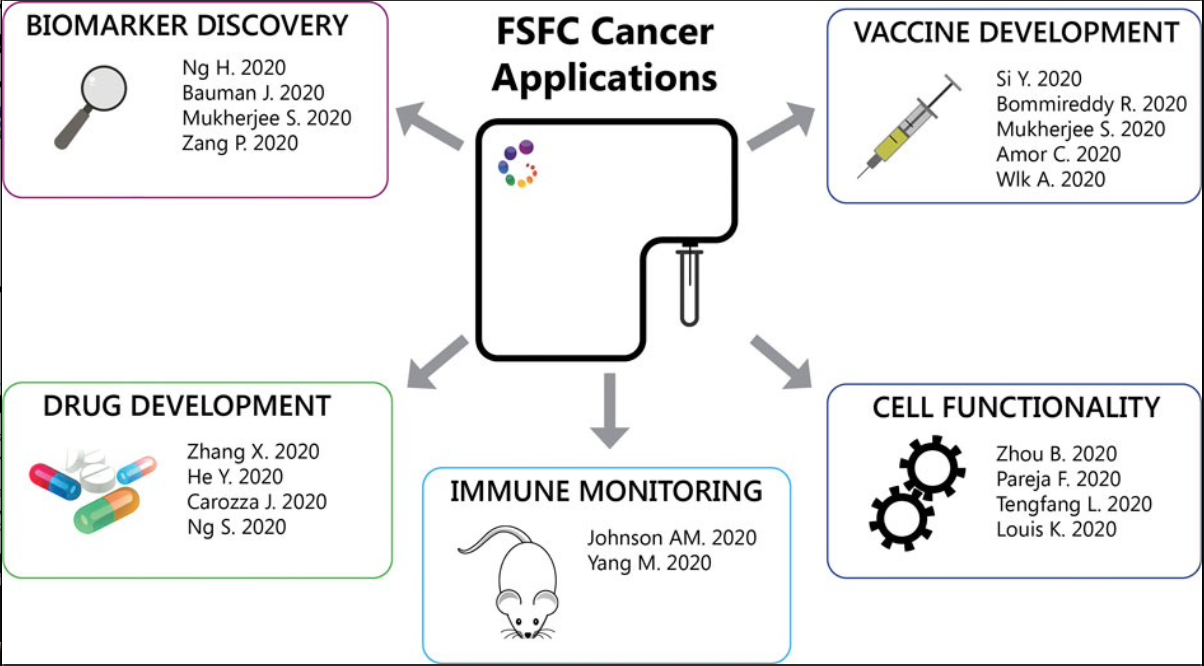 图 1. Cytek 全光谱流式引领肿瘤免疫热点研究 ¹ 1. 疾病相关生物标志物的发现 美国亚利桑那大学 Bauman 等研究人员联合 Cetuximab 和 Ficlatuzumab 治疗难治性 / 复发性头颈部鳞状细胞癌(HNSCC)患者。该研究利用 21 色全光谱流式细胞术,评估了患者经过治疗前后免疫表型的变化。结果表明外周血 T 细胞,特别是 CD8+ T 细胞亚群的增加与治疗响应相关,而一群髓系细胞的扩增则与疾病进展相关。治疗响应者外周 CD8+ T 细胞的增加是该联合方案具有潜在免疫调节活性的首次报道,对临床用药具有重要的指导意义 ²。 在肝癌研究中,肝癌患者抗 anti PD-1/PD-L1 的免疫检查点阻断 (ICB) 治疗响应率低。因此,找到预测治疗效果的相关指标很有必要。在 49 名接受 ICB 治疗的肝癌患者样本中发现,肝癌浸润的巨噬细胞中 CD38 的表达可能成为预测 ICB 治疗效果的指标,该工作使用 Cytek 全光谱流式验证了 CD38 在肝癌组织巨噬细胞中的表达 ³。
图 2. HNSCC 治疗响应和疾病进展患者免疫表型评估 ² 2. 疾病相关生物标志物的发现 来自 University of Colorado Anschutz Medical Campus 的 Amber M. Johnson 等研究者对肿瘤表达 MHCII(csMHCII)展开研究,发现 csMHCII 的表达与抗 PD1 治疗效果相关。通过诱导 MHCII 通路调节因子 CIITA 的缺失,下调 csMHCII 表达,使得肿瘤对于抗 PD-1 治疗的敏感性下降。利用 Cytek 全光谱流式超多色检测性能,22 项分子检测指标直指肿瘤微环境中免疫细胞的募集和浸润。数据显示,csMHCII 的表达下降,可引发 T 细胞浸润的减少,B 细胞增加以及巨噬细胞募集的降低,从而降低了肿瘤对于抗 PD-1 治疗的敏感性⁴。
图 3. csMHCII 表达对于小鼠肿瘤微环境的影响⁴ 3. 新药治疗靶点的评估 肿瘤细胞通过上调抗凋亡蛋白,促进肿瘤生长,干扰药物治疗并逃逸细胞凋亡,因此,此类蛋白成为抗肿瘤治疗的潜在重要靶标。美国佛罗里达大学 Daohong Zhou 团队先后发表了两篇文章,提出了小分子蛋白水解靶向嵌合体 PROTAC 靶向结合抗凋亡蛋白 Bcl-XL,用于肿瘤治疗的新思路。使用 Cytek 全光谱流式检测候选药物 PROTAC XZ739⁵和 DT2216⁶作用效果时,研究人员发现二者不仅能促进肿瘤细胞株 MOLT-4 T-ALL 发生凋亡,且在毒理学上其对血小板毒性较低。因此提出小分子蛋白水解靶向嵌合体对于肿瘤治疗将具有广泛应用价值。
图 4. PROTAC XZ739 可靶向杀伤 MOLT-4 肿瘤细胞⁵ 4. 助力肿瘤疫苗研究 肿瘤疫苗开发中,纳米颗粒疫苗能够呈递抗原激发机体免疫,但纳米颗粒疫苗的免疫原性的具体机制还不清楚。研究人员在鼻腔内接种携带 pEα 肽抗原的纳米纤维 (EαQ11) 后,发现抗原可以被肺部 CD103+CD11b + 的 DC 细胞呈递,同时上调 CD80 表达并迁移到引流淋巴结,进而引发淋巴结和肺部抗原特异性 TH17 细胞的累积。多色光谱流式解答了该类纳米颗粒疫苗的作用机制,由此也说明了纳米颗粒疫苗可能是一种新型的、无针和无佐剂的方法,可以激发皮肤和粘膜屏障表面真菌和细菌感染的保护性免疫。⁷多样化的肿瘤疫苗,如肿瘤细胞膜囊泡(TMVs)疫苗免疫也被证实了可以抑制肿瘤生长,为肿瘤治疗提供新思路⁸。
图 5. 鼻腔内接种 EαQ11 后肺部和引流淋巴结 DC 呈递抗原⁷ 以上高水平热点研究论文均使用 Cytek 全光谱流式细胞仪完成流式相关检测,相比于传统流式,Cytek 全光谱流式细胞仪凭借专利的全光谱检测技术(FSP™),得以让研究人员更灵活地搭配多色实验方案,在一管样本中高灵敏地实现超多色分析。除此之外,全光谱流式自发荧光提取功能有助于帮助科研人员发现高背景下被掩盖的信号,进一步提升弱阳性信号的分群效果,为肿瘤免疫研究提供更多的可能。
参考文献: 1. Bonilla, D. L., Reinin, G. & Chua, E. Full Spectrum Flow Cytometry as a Powerful Technology for Cancer Immunotherapy Research. Frontiers in Molecular Biosciences 7, doi:10.3389/fmolb.2020.612801 (2021). 2. Bauman, J. E. et al. Phase I Study of Ficlatuzumab and Cetuximab in Cetuximab-Resistant, Recurrent/Metastatic Head and Neck Cancer. Cancers (Basel) 12, doi:10.3390/cancers12061537 (2020). 3. Ng, H. H. M. et al. Immunohistochemical scoring of CD38 in the tumor microenvironment predicts responsiveness to anti-PD-1/PD-L1 immunotherapy in hepatocellular carcinoma. J Immunother Cancer 8, doi:10.1136/jitc-2020-000987 (2020). 4. Johnson, A. M. et al. Cancer Cell-Intrinsic Expression of MHC Class II Regulates the Immune Microenvironment and Response to Anti-PD-1 Therapy in Lung Adenocarcinoma. J Immunol 204, 2295-2307, doi:10.4049/jimmunol.1900778 (2020). 5. Zhang, X. et al. Discovery of PROTAC BCL-XL degraders as potent anticancer agents with low on-target platelet toxicity. Eur J Med Chem 192, 112186, doi:10.1016/j.ejmech.2020.112186 (2020). 6. He, Y. et al. DT2216-a Bcl-xL-specific degrader is highly active against Bcl-xL-dependent T cell lymphomas. J Hematol Oncol 13, 95, doi:10.1186/s13045-020-00928-9 (2020). 7. Si, Y. et al. Adjuvant-free nanofiber vaccine induces in situ lung dendritic cell activation and T(H)17 responses. Sci Adv 6, eaba0995-eaba0995, doi:10.1126/sciadv.aba0995 (2020). 8. Bommireddy, R. et al. Tumor Membrane Vesicle Vaccine Augments the Efficacy of Anti-PD1 Antibody in Immune Checkpoint Inhibitor-Resistant Squamous Cell Carcinoma Models of Head and Neck Cancer. Vaccines (Basel) 8, doi:10.3390/vaccines8020182 (2020). |