大家都在搜
| 我们知道心脏的跳动离不开心肌的收缩,而心肌的收缩依赖于动作电位的产生。但要想使得动作电位的电学转化为心肌收缩的力学,心肌需要一个重要的转换“中介”,这一神秘中介就是兴奋-收缩耦联(excitation-contraction coupling,ECC)。简单来说,这是一种由动作电位诱发心肌细胞肌浆网内 Ca2+浓度增加继而引发心肌细胞收缩的过程。正是由于它的存在,才能将动作电位的电学转化为心肌收缩的机械能,从而做功发挥宏观作用。其中,细胞内 Ca2+的调控是兴奋-收缩耦联的中心环节。 一、基本知识掌握 结构决定功能,要想知道心肌的兴奋-收缩耦联机制,首先我们应当了解心肌细胞的结构特征。( 心肌细胞的独特结构(文末视频超燃)) 1、肌小节 心肌细胞由肌小节组成,内部含有大量的肌原纤维和肌管系统,每个肌小节内部由粗、细肌丝沿细胞长轴规律排列,其间还分布着许多重要的细胞器和膜结构,如横管(Transverse tubule,T tubule )、肌质网(Sarcoplasmic reticulum,SR)及线粒体等。肌小节是心肌细胞收缩的基本单位。 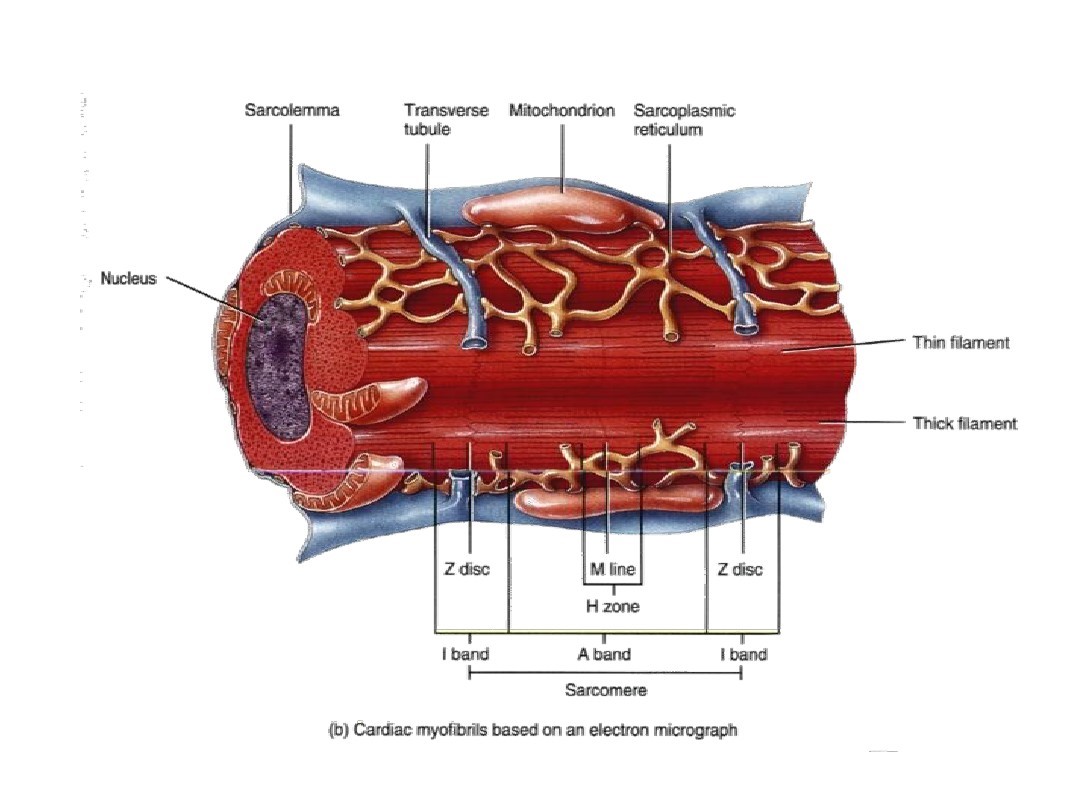
图 1 心肌细胞结构
2、肌膜 心肌细胞膜也称为肌膜(Sarcolemma),肌膜在肌小节 Z 线处向肌浆内凹陷形成的管状结构为横管(T tubule),横管深入细胞内部包绕于肌原纤维周围形成的复杂管状系统称为横管系统。横管结构将心肌动作电位传入细胞内部,引发 Ca2+从距横管近的肌质网中释放出来。 3、肌质网 肌质网是心肌细胞中特化的滑面内质网,具有储存和释放 Ca2+的能力。根据形态和功能的不同,是心肌细胞的钙库,可以分为终池(functional sarcoplasm reticulum,JSR)和纵管(longitudinal sarcoplasm reticulum,LSR),二者相连续,JSR在接触横管处膨大形成中空泡状结构,称为肌质网终池(Subsarcolemmal cisternate),与细胞膜形成二联管结构。 4、膜蛋白以下是在兴奋-收缩耦联过程中起重要作用的膜蛋白: (1)T 管膜和肌膜上的膜蛋白:电压门控钙通道(L-type voltage-gated calcium channels,L-VGCCs)——在膜去极化过程中 L-VGCCs 通道打开引起胞外 Ca诱导肌浆网大量 Ca2+释放的触发点( trigger)。L-VGCCs 在 T 管膜的密度远远高于肌膜,说明心肌细胞兴奋时大部分 Ca2+通过横管区域进入细胞内。 (2)终池上的膜蛋白:Ryanodine 受体(RyR)——心肌细胞内重要 Ca2+释放通道。 (3)纵管上的膜蛋白:肌质网钙泵蛋白(SERCA)——将细胞质中的Ca2+回收到肌质网中。 (4)肌膜上的膜蛋白:Na+-Ca2+交换体(NCX)和钙泵(Ca2+ATPase)——将细胞质中的 Ca2+排至胞外。 二、兴奋-收缩耦联基本步骤 1.T 管膜的动作电位传导:肌膜上的动作电位沿 T 管膜传至肌细胞内部,并激活 T 管膜和肌膜中的 L 型钙通道。 2.终池内 Ca2+的释放——钙诱导钙释放(calcium-induced calcium release,CICR ) 机制: 横管与肌质网紧密耦联,使位于细胞膜上的 L 型钙通道与位于肌质网上的 RyR 在空间上密切相邻。RyR 在肌质网上成簇分布,每簇 RyR 和与其在空间上对应的 L 型钙通道形成在功能上耦联的一组结构,称为耦联子(couplon )。这一接近配对是 CICR 过程的关键机制,依赖于 T 管和终池(JSR)的耦联结构基础,即二联管。在动作电位的驱动下,心肌细胞去极化,细胞膜上电压敏感的钙通道被激活开放。在这个结构区内,肌浆网上的 RyR 与肌膜和 T 管膜上的 L 型钙通道之间的距离小于 20 nm,当 L 型钙通道开放时,细胞外 Ca肌质网上的钙释放通道 RyR,使肌质网钙库释放大量 Ca2+到细胞质内,胞质内自由Ca2+浓度快速升高,即出现钙瞬变(Ca2+transient )。这一由局部少量外Ca2+进入细胞而引起 SR 内大量 Ca2+释放到细胞内,造成细胞局部范围Ca2+升高的过程称为“钙诱导钙释放”。在这个过程中,心肌细胞内 Ca2+浓度由 1OO nM 快速升高到 1μM 的水平。 
图 2 dSTORM 超分辨率观察大鼠心室肌细胞外周偶联蛋白中聚集性 RyR(白色箭头所指)。
RyR 在心肌细胞表面附近,许多 RyR团簇呈长方形或拉长状。Front Physiol. 2018;9:1472. doi:10.3389/fphys.2018.01472 
图 3 钙诱导钙释放过程 
图 4 肌浆网及肌丝结构关系
4.回摄和储存 Ca2+:心肌胞质内大部分Ca2+经 LSR 膜中的 SERCA 活动被回收,但仍有10%-20%的 Ca2+则由肌膜中的 Na+-Ca2+交换体(NCX)和钙泵(Ca2+ ATPase)排至胞外,这一过程消耗 ATP,胞质中 Ca2+浓度降低则导致肌肉舒张,可见舒张过程亦耗能。 综上,通过“钙触发”、“钙诱导”和“钙释放”将肌膜电信号转化为心肌收缩的机械能这一过程即为“神秘中介”——兴奋-收缩耦联。 三、前沿 至此,我们可以看出,如果没有心肌兴奋-收缩耦联(ECC)这一强大的中介机制,心肌的收缩过程则难以实现。目前有研究表明,哺乳动物心肌兴奋-收缩耦联机制随着出生后心肌形态结构的变化而不断变化,其中关键点是兴奋-收缩耦联过程所需的 Ca随着心肌成熟度不同而变化。成熟心肌兴奋-收缩耦联过程主要涉及两个通道:一个 Ca流通道和一个Ca2+释放通道,而在未成熟心肌介导兴奋-收缩耦联的钙内流和钙释放通道均不仅仅是一个,而是两个或多个,触发心肌收缩的 Ca而这些通道的功能在出生后心脏发育过程中有的逐渐减弱甚至消失,而另一些则逐渐增强成为成熟心肌的“骨干”通道。当然这仅是目前对此过程的了解,也不能排除未成熟心肌中存在尚未发现的关键通道,恰如成熟心肌中提供 90% Ca的心脏药物和心脏手术停搏液对发育成熟的心脏可提供较好的疗效和心肌保护作用,但对发育中的婴幼儿心脏效果并不理想,这可能与其不同于成人的心肌兴奋-收缩耦联机制有关,若未成熟心肌兴奋-收缩耦联机制得以阐明,可据此设计特异性适用于婴幼儿的药物和相应的心肌保护方法,为这些患者带来福音。 参考文献: [1]孙敏,于海奕,张幼怡,吕志珍,高炜,李子健.成年大鼠心肌细胞分离培养及兴奋-收缩耦联表征[J].中国比较医学杂志,2014,2403:1-5+83. [2]王芳,丛祥凤,陈曦.心肌兴奋-收缩耦联在出生后哺乳动物发育中的变化[J].生理科学进展,2013,4403:227-232. [3]Escobar AL,Ribeiro-Costa R,Villalba-Galea C,et al. Developmental changes of intracellular Ca2+ transients in beating rat hearts[J]. Am J Physiol Heart Circ Physiol,2004,286 H971 - H978. [4]邓建新. 正常与疾病心脏兴奋—收缩耦联调节机制的研究[D].南方医科大学,2013.
作者:陈满
配图:来源于网络 本文发布于微信公众号:心肌电生理 刊物和机构如需转载,请联系授权事宜:cvep2020@163.com |