实验动物免疫方案:1、抗原: 蛋白质、多肽、细胞器、细胞、组织等。2、免疫方式:皮下注射、腹腔注射、静脉注射、肌肉注射等。3、不同动物免疫所需抗原量(以蛋白免疫为例)。
1971年Engvall和Perlmann发表了酶联免疫吸附剂测定(enzyme linked immunosorbent assay,ELISA)用于IgG定量测定的文章,使得1966年开始用于抗原定位的酶标抗体技术发展成液体标本中微量物质的测定方法。这一方法的基本原理是:①使抗原或抗体结合到某种固相载体表面,并保持其免疫活性。②使抗原或抗体与某种酶连接成酶标抗原或抗体,这种酶标抗原或抗体既保留其免疫活性,又保留酶的活性。在测定时,把受检标本(测定其中的抗体或抗原)和酶标抗原或抗体按不同的步骤与固相载体表面的抗原或抗体起反应。用洗涤的方法使固相载体上形成的抗原抗体复合物与其他物质分开,最后结合在固相载体上的酶量与标本中受检物质的量成一定的比例。加入酶反应的底物后,底物被酶催化变为有色产物,产物的量与标本中受检物质的量直接相关,故可根据颜色反应的深浅刊物定性或定量分析。由于酶的催化频率很高,故可极大地地放大反应效果,从而使测定方法达到很高的敏感度。
常用的采血方法有割(剪)尾采血、眼眶静脉丛采血、断头采血、心脏采血、颈静脉(动脉)采血、股动脉(静脉)采血、耳静脉采血、前肢头静脉才学、后肢小静脉采血等。
在分析工作中,洗涤玻璃仪器不仅是一项必须做的实验前的准备工作,也是一项技术性的工作。仪器洗涤是否符合要求,对检验结果的准确和精密度均有影响。不同的分析工作有不同的仪器洗净要求,我们以一般定量化学分析为主介绍仪器的洗涤方法。
微生物具有容易变异的特性,因此,在保藏过程中,必须使微生物的代谢处于最不活跃或相对静止的状态,才能在一定的时间内使其不发生变异而又保持生活能力。低温、干燥和隔绝空气是使微生物代谢能力降低的重要因素,所以,菌种保藏方法虽多,但都是根据这三个因素而设计的。
30%丙烯酰胺溶液:将29g丙烯酰胺和1g NN'-亚甲双丙烯酰胺溶于总体积为60ml的水中。加热至37℃溶解之,补加水至终体积为100ml.用滤器(0.45μm孔径)过滤除菌,查证该溶液的pH值应不大于7.0置棕色瓶中保存于室温。丙烯酰胺具有很强的神经毒性并可以通过皮肤吸收,其作用具累积性。称量丙烯酰胺和亚甲双丙烯酰胺时应戴手套和面 ...
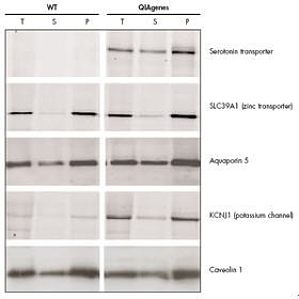
众所周知,膜蛋白在细胞间接触、表面识别、信号转导、酶活性和运输方面都扮演着重要的角色。由于它们功能多样,也就成为理想的药物靶点。然而,膜蛋白的生化和结构研究一直都很缓慢。Protein Database的统计数据表明,在成功解析出三维结构的蛋白中,膜蛋白只占1%,这与膜蛋白占总蛋白的1/3的总量的差别巨大。由此也可以看出膜蛋白研究确实困难重重。
2005年,Georg Nagel实验室和Karl Deisseroth实验室的联合研究证实,光激活细菌(信号转导)通路channelrhodopsin-2(ChR2)能活化神经信号(转导)。由于该过程简单易操作,激发了神经科学家的极大兴趣。
实验动物的麻醉是一项复杂系统的工作。正确的麻醉处理,是动物实验成功的有力保障。而麻醉处理不当,会给实验结果带来难以分析的误差。要想获得良好的麻醉效果,除掌握实验动物麻醉的基本知识和技术、遵循科学的麻醉程序外,还应了解影响实验动物麻醉的各种因素,如动物因素、环境因素等。
r为离心机转轴中心与离心套管底部内壁的距离;rpm(revolution per minute)为离心机每分钟的转数;RCF(relative eentrifugal force)为相对离心力,以地心引力,即重力加速度的倍数来表示,一般用g表示
r为离心机转轴中心与离心套管底部内壁的距离;rpm(revolution per minute)为离心机每分钟的转数;RCF(relative eentrifugal force)为相对离心力,以地心引力,即重力加速度的倍数来表示,一般用g表示。
聚合酶链反应(Polymerase Chain Reaction ,PCR)是80年代中期发展起来的体外核酸扩增技术。它具有特异、敏感、产率高、快速、简便、重复性好、易自动化等突出优点;能在一个试管内将所要研究的目的基因或某一DNA片段于数小时内扩增至十万乃至百万倍,使肉眼能直接观察和判断;可从一根毛发、一滴血、甚至一个细胞中扩增出足量的DNA供分析研究和检测鉴定。
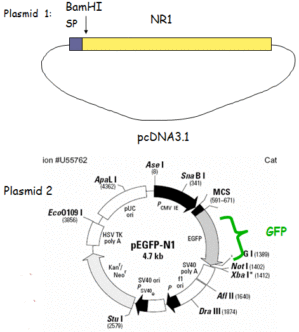
根据已知的脊椎动物某一特定基因的氨基酸序列的保守区域设计简并引物,利用RT-PCR技术获得该基因的核心片断,将该片断分离纯化后与T载体连接,转化大肠杆菌,挑取白色菌落,经 PCR反应鉴定得到阳性克隆,送阳性克隆的PCR产物去测序,从而获得目的基因的cDNA核心片断的序列。
聚合酶链反应(Polymerase Chain Reaction ,PCR)是80年代中期发展起来的体外核酸扩增技术。它具有特异、敏感、产率高、快速、简便、重复性好、易自动化等突出优点;能在一个试管内将所要研究的目的基因或某一DNA片段于数小时内扩增至十万乃至百万倍,使肉眼能直接观察和判断;可从一根毛发、一滴血、甚至一个细胞中扩增出足量的DNA供分析研究和检测鉴定。
Oligo DNA是以OD260单位来计算的,这是指在1ml体积1cm光程标准比色皿中,260nm波长下吸光度为1A260的Oligo溶液定义为1 OD260单位,根据此定义,1 OD260单位相当于33μg的Oligo DNA,您可以根据此数据和您的Oligo DNA分子量,计算得到摩尔数以计算不同摩尔浓度的溶液。
引物是人工合成的两段寡核苷酸序列,一个引物与感兴趣区域一端的一条DNA模板链互补,另一个引物与感兴趣区域另一端的另一条DNA模板链互补。
随机引物 适用于长的或具有发卡结构的RNA.适用于rRNA、mRNA、tRNA 等所有RNA的反转录反应。主要用于单一模板的RT-PCR反应。 Oligo dT 适用于具有PolyA尾巴的RNA.(原核生物的RNA、真核生物的 Oligo dT rRNA和tRNA不具有PolyA尾巴。)由于Oligo dT要结合到PolyA 尾巴上,所以对RNA样品的质量要求较高,即使有少量降解也 会使全长cDN ...
随机引物:适用于长的或具有发卡结构的RNA.适用于rRNA、mRNA、tRNA 等所有RNA的反转录反应。主要用于单一模板的RT-PCR反应。oligo dT:适用于具有PolyA尾巴的RNA.(原核生物的RNA、真核生物的 Oligo dT rRNA和tRNA不具有PolyA尾巴。)由于Oligo dT要结合到PolyA 尾巴上,所以对RNA样品的质量要求较高,即使有少量降解也 会使全长cDNA合成量大大减少。
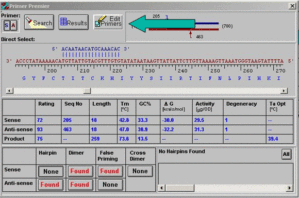
引物设计基本原则:1. 引物的长度。一般为15-30bp,常用的是18-27bp,但不能大于38,因为过长会导致其延伸温度大于74℃,即Taq酶的最适温度。2.产物的长度……
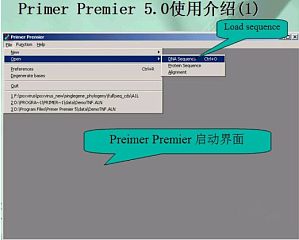
作为目前最好、最专业的引物设计软件,Oligo的功能很强,在这里我们介绍它的一些主要功能,如:普通引物对的搜索、测序引物的设计、杂交探针的设计以及评估引物对质量等等。