相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 库存:
>10
- 保修期:
1年
- 现货状态:
>10
- 供应商:
Refeyn
- 规格:
台
单分子质量光度系统—TwoMP
质量光度法是一种革命性的分析生物分子的新方法。它能够在溶液中精确测量单个分子的质量,不需要任何偶联固化或者标记标签,在天然状态下,完成对生物分子的分析。这种方法为生物分析和生物分子功能研究开辟了新的可能性。
★ 无标记无修饰;
★ 保持结构完整性和活性;
★ 测量只需要几微升的样品;
★ 设计紧凑的台式仪器,无特殊安装要求;
★ 软件自动控制采集过程,并在几分钟内进行质量分析;
★ 直观地解释质量分布的结果,而不需要任何经验和知识;
★ 准确测量在溶液(而不需真空)中的蛋白分子质量;
★ 单分子分析,可靠区分样品中所有已知和未知组分,高精度捕获高丰度和低丰度分子;
★ 快速、简单、最小样本量:纳米浓度下的微升样品体积,几分钟内获得结果,宽质量范围和高动态范围;
这么优秀的分子分析技术,您还不动心么?
技术背景:
英国Refeyn公司的质量光度计One MP于2019年3月上市,2020年进入中国市场,2021年,推出更新型号的产品---质量光度计的二代机,Two MP,在硬件和软件上均有升级。2022年2月,北京佰司特中标北京生命科学研究所质谱招标采购项目(国内第一台质量光度计二代机)TwoMP,其分辨率和稳定性,相对之前的质量光度计的一代机OneMP,有大幅提升。北京佰司特借此机会,也为国内科研人员提供更有更好的产品和服务。
2021年开始,北京佰司特科技有限责任公司获得中国大陆地区的代理权;2023年开始,北京佰司特科技有限责任公司负责英国Refeyn公司的质量光度计在国内研究单位的市场推广、产品宣传、销售和售后工作。
全新的英国Refeyn公司的质量光度计TwoMP,将质量光度法(Mass photometry)技术引入到日常的实验室生活中,这种独特的仪器可以让你以很高的灵敏度、速度、准确度和简单性来表征你感兴趣的分子,是监测蛋白质纯化、优化样品、研究蛋白质功能和相互作用的理想仪器。所有测量都可在各种各样的天然缓冲液中逐个分子地完成,还不需要标签,就可以直观地解释质量分布结果,且无需任何先验知识。
粒子散射的光与粒子体积和折射率成线性关系。由于蛋白质的光学性质和密度只有百分之几的变化,它们的散射信号与它们的序列质量成正比,这使得在高精度和大质量范围内用光来“称量”单个分子成为可能。许多生物分子(糖蛋白、核酸或脂类)的散射信号与质量的相关性是成立的,使得质量光度法能够成为溶液中生物分子的通用分析工具。

图1:质量光度法原理。附着在测量界面上的分子散射的光干扰了该界面反射的光。干涉对比度与质量成线性关系。
粒子散射的光与粒子体积和折射率成线性关系。由于蛋白质的光学性质和密度只有百分之几的变化,它们的散射信号与它们的序列质量成正比,这使得在高精度和大质量范围内用光来“称量”单个分子成为可能。许多生物分子(糖蛋白、核酸或脂类)的散射信号与质量的相关性是成立的,使得质量光度法能够成为溶液中生物分子的通用分析工具。

图2:质量光度法测量溶液中蛋白质和蛋白质组合的分子质量。通过校准,质量光度法可以高精度(平均2%)测量未知物质的质量。
质量光度法Mass photometry技术的特点:
★ 准确测量蛋白分子在溶液中的真实、天然行为;
★ 适用于在各种缓冲液中,与膜蛋白相容;
★ 无标签标记,无需修饰样品或干扰分子表面;
★ 可检测样本中所有亚群体的信息:单分子分析能够可靠地区分已知和未知样品成分,无需先验知识;
★ 单分子计数:以高精度捕获高丰度和低丰度分子;
★ 宽质量范围和高动态范围;
★ 一种分析形式可提供多个结果;
★ 保持同质性、结构完整性和活性;
★ 快速、简单、最小样本量—纳米浓度下的微升样品体积,从一滴样品中在几分钟内获得结果;
质量光度计TWOMP仪器的特点:
★ 紧凑的台式仪器,安装要求低。测量只需要几微升的样品、和干净、高质量的盖玻片,几分钟内可获得结果;
★ 直观高效——Refeyn的软件自动控制采集过程,并在几分钟内完成质量分析。您可以直观地解释质量分布结果,而无需任何先验知识;
★ 超高的精确性——由于其高灵敏度,非常适合在生理(低)浓度下进行测量,而单分子计数技术固有的高动态范围确保低丰度分子仍能被准确捕获。质量光度法能轻松量化不同种类的蛋白质分子,具有高分辨率和重复性;
质量光度计TWOMP仪器的参数:
※ 原理:干涉光散射,无需标记
※ 质量范围:30kDa – 5MDa
※ 测量精度:±2% @ 10 nM
※ 单次测量质量误差:±5% @ 10 nM
※ 分辨率(FWHM):25kDa @ 66kDa,60KDa @ 660 kDa
※ 浓度范围:100pM - 100nM(粒子浓度)
※ 灵敏度:< 1ng蛋白质
※ 样品体积:5 - 20 μ l
※ 帧率(标准设置):1 kHz(原始),100 Hz(集成)
※ 视场:4 x 11µm (@ 500 Hz)至12 x 17µm(@ 135 Hz)
※ 波长:488 nm
※ 像素尺寸:12nm
※ 控制计算机(Core i7, 16 GB RAM, 256 GB SSD, 2TB HD, Windows 10),包括键盘或鼠标和24”显示器
基于光学检测分析的分子量
※ 测量目标范围广泛,从 30 kDa 到5MDa,(动态范围从大约 10 kDa)
※ 蛋白质寡聚化/片段化
※ 抗原抗体反应,化学计量
※ AAV等病毒载体的满载/空载比
※ DNA Ladder的分子量分布、多糖的分子量分布
天然状态下测量
※ 各种溶液系统
※ 无需分离介质
※ 无标记测量,无固定和样品处理要求
※ 分析仪与样品完全非接触
测量时间在2分钟以内
※ 测量时间约1分钟
※ 样品输入约1分钟
实现超低浓度、小体积的样品量
※ 极少量的最佳浓度和容量
※ 蛋白质(<1 MDa):1 nM 至 2 μL,<1 ng
※ 病毒载体(> 1 MDa):0.1 nM 至 2 uL
应用领域:
★ 样品纯度和成分分析 Sample characterization;
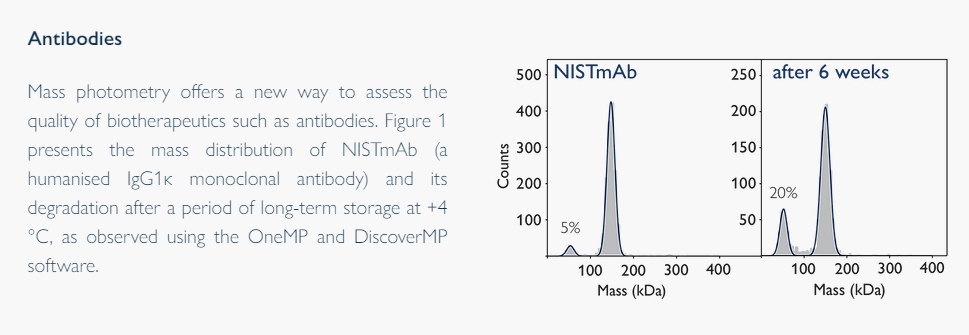
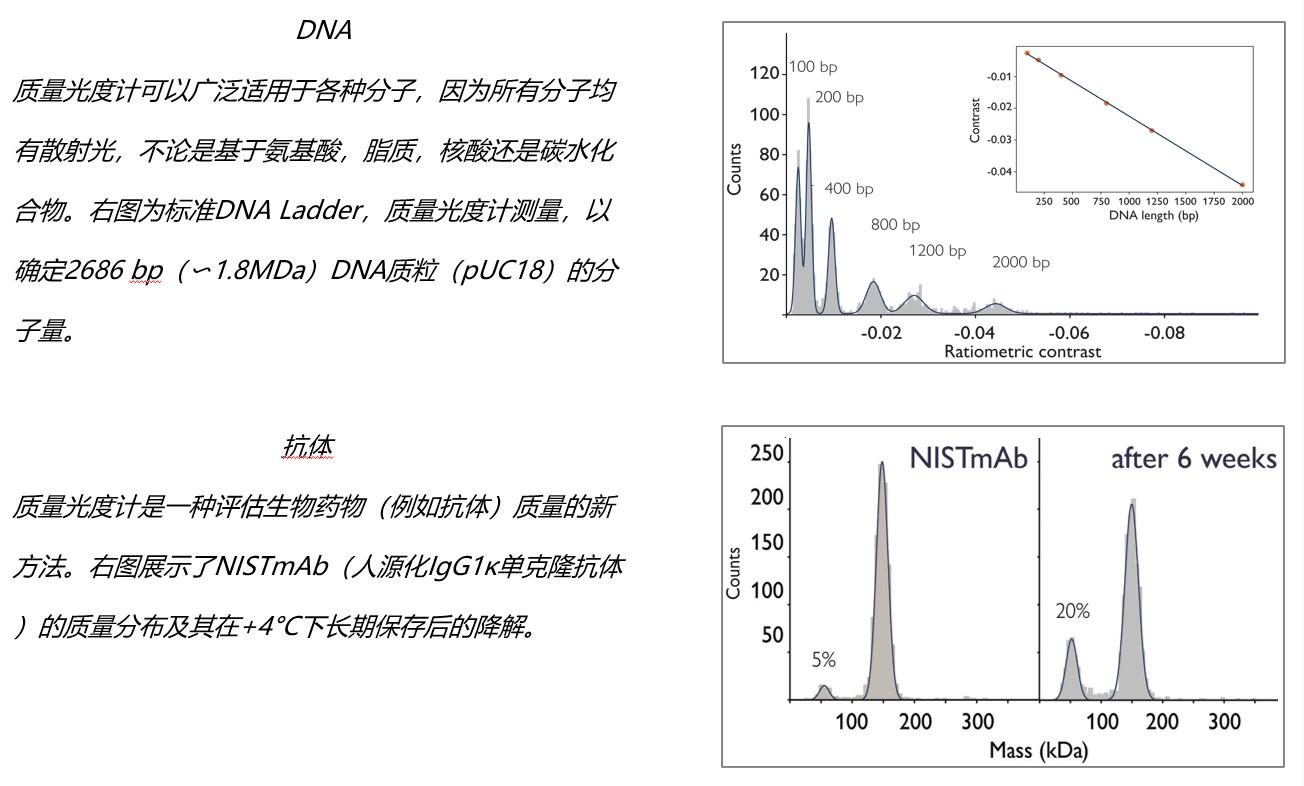
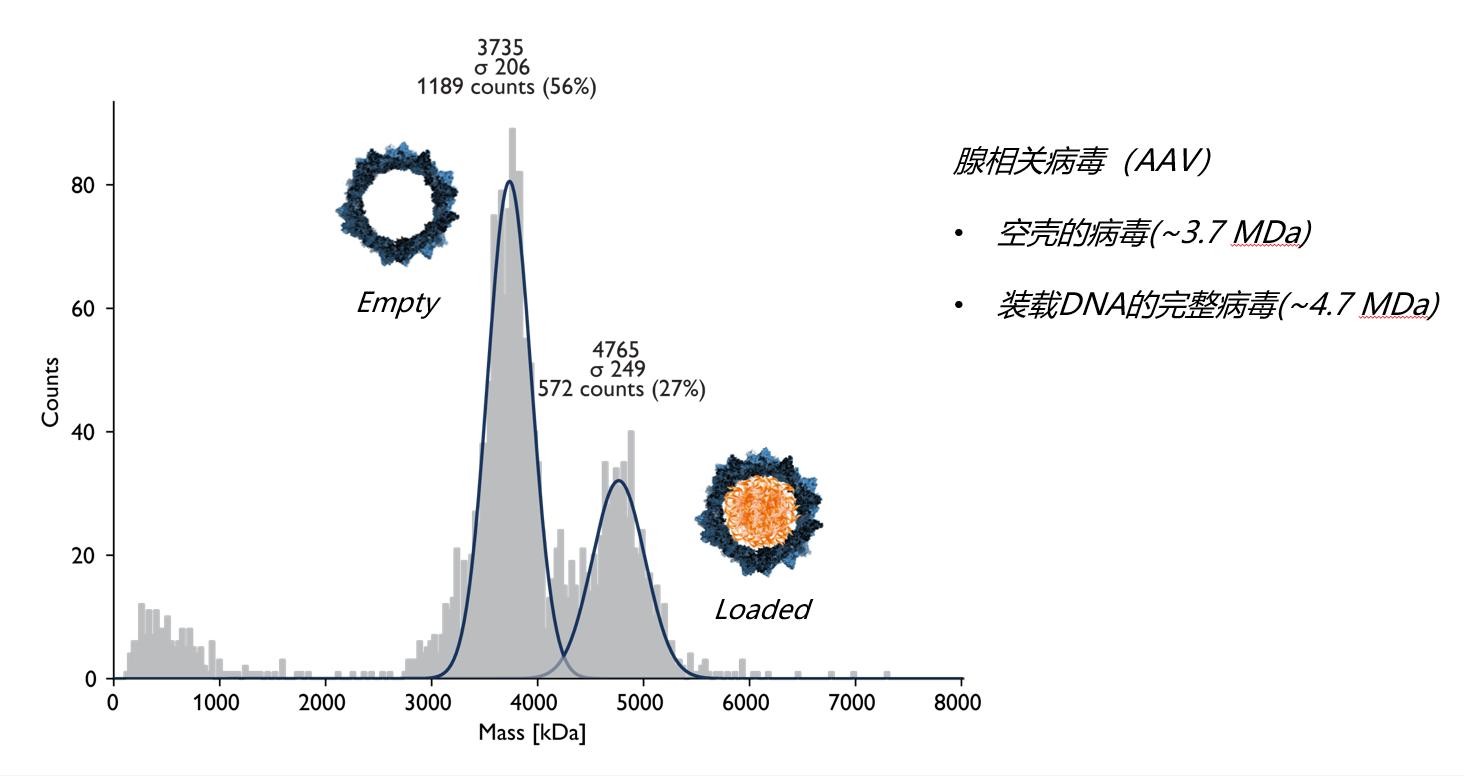
样品的纯度和稳定性是成功的生化和结构研究的关键因素。在制药生产的背景下,蛋白质的纯度是特别重要的,特别是随着蛋白质类产品如生物制剂的日益流行。
质量光度计提供了在单个分子水平上样品异质性的快速评估,使用最小的样品体积和在几分钟内。通过质量光度法获得的质量分布提供了样品中现有物种的直接信息,由于条件变化而产生的任何变化都可以用于样品优化。
★ 异质生物分子的质量分析测量 Protein oligomerization;
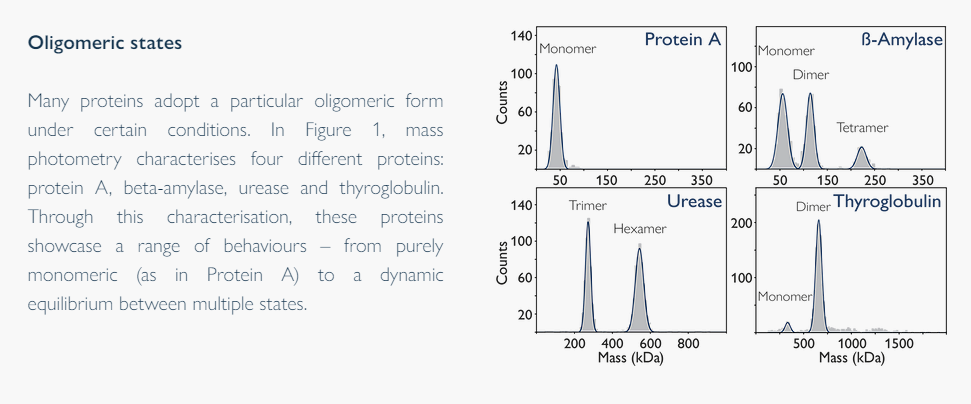
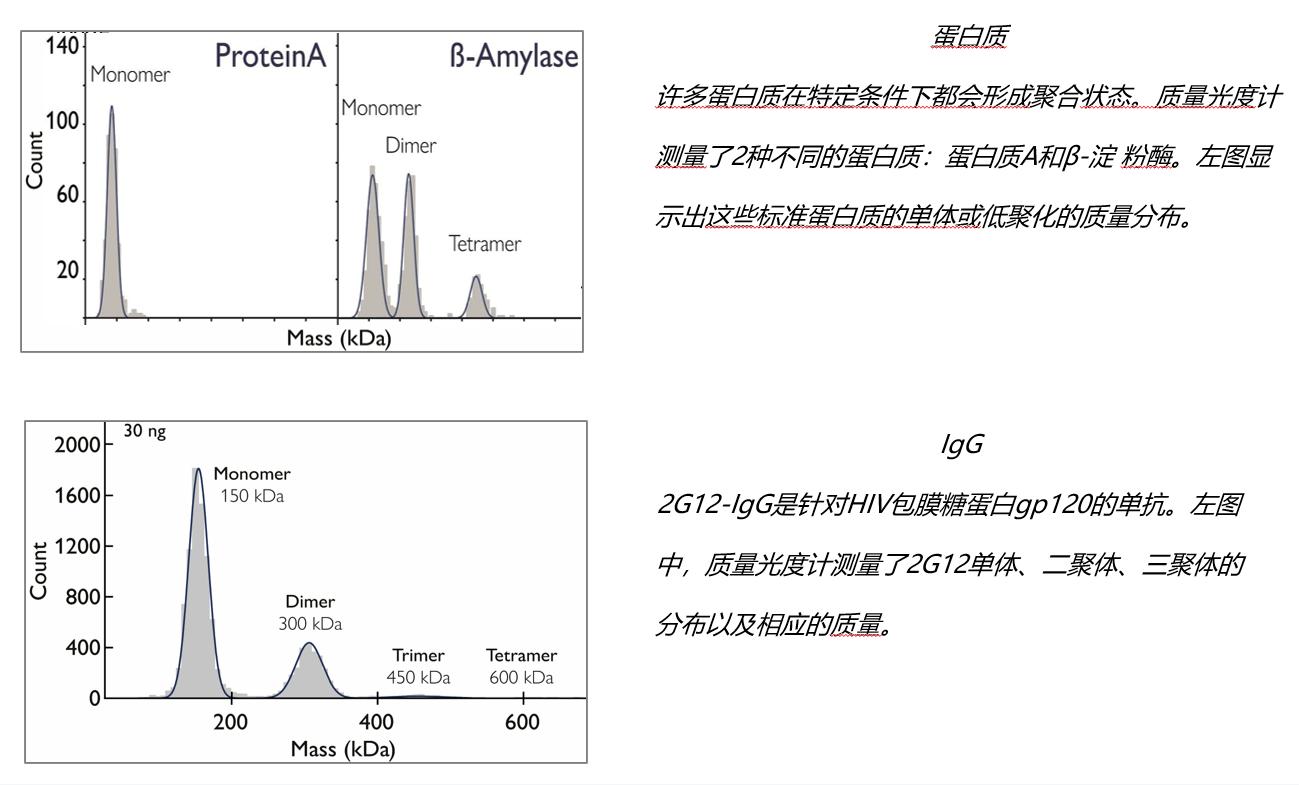
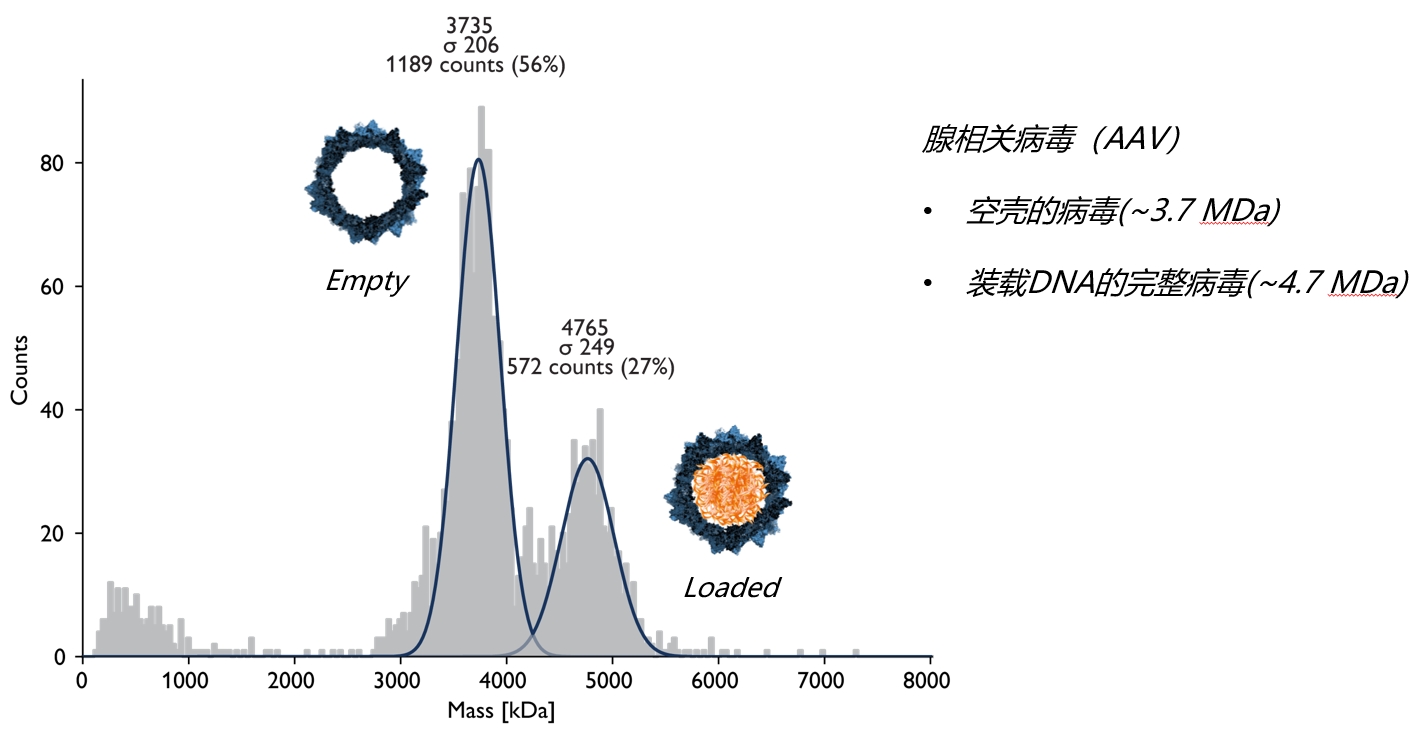
许多生物系统的一个关键特征是蛋白质自组装成特定的四级结构,这往往决定和调节它们的功能。蛋白质低聚化的评估对于详细了解复杂的生物过程是至关重要的。在这种情况下,分子质量是一个重要的参数,因为它作为低聚化的直接度量。
质量光度计提供了高分辨率的分子质量分布与单分子灵敏度。这使得我们的技术能够有效地检测出占主要样本总数不到1%的稀有物种。
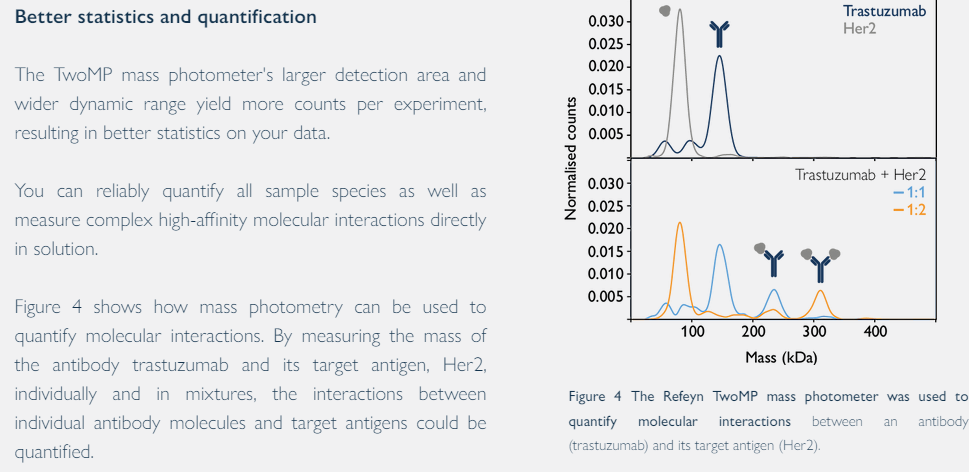
★ 生物分子间相互作用 Biomolecular interactions;
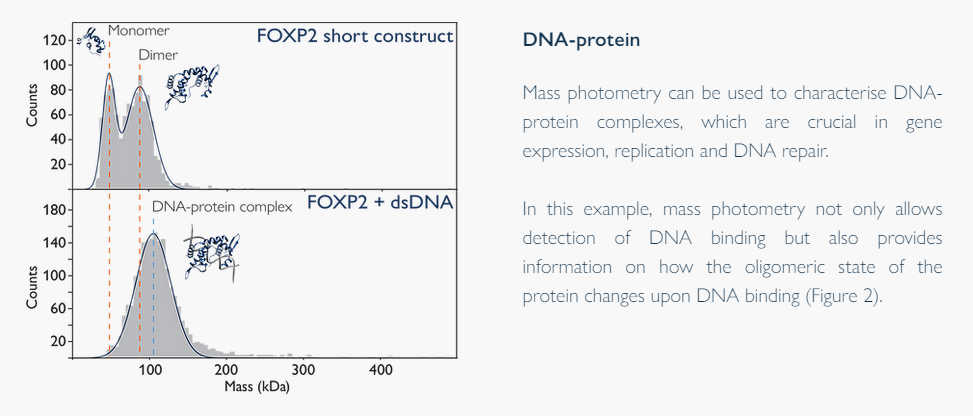
生物分子之间的相互作用在每个生物过程中起着关键作用。质量光度计非常适合于定量低浓度下的相互作用,其主要优点是检测溶液中存在的生物复合物。分子质量是反映生物分子和生物分子复合物的同质性、结构完整性和活性等多种性质的通用读数。这使得质谱光度法不仅可以用于简单的纯度测定,还可以用于活性和结合性评估,提供了独特水平的数据完整性和其他类似技术的可比性。
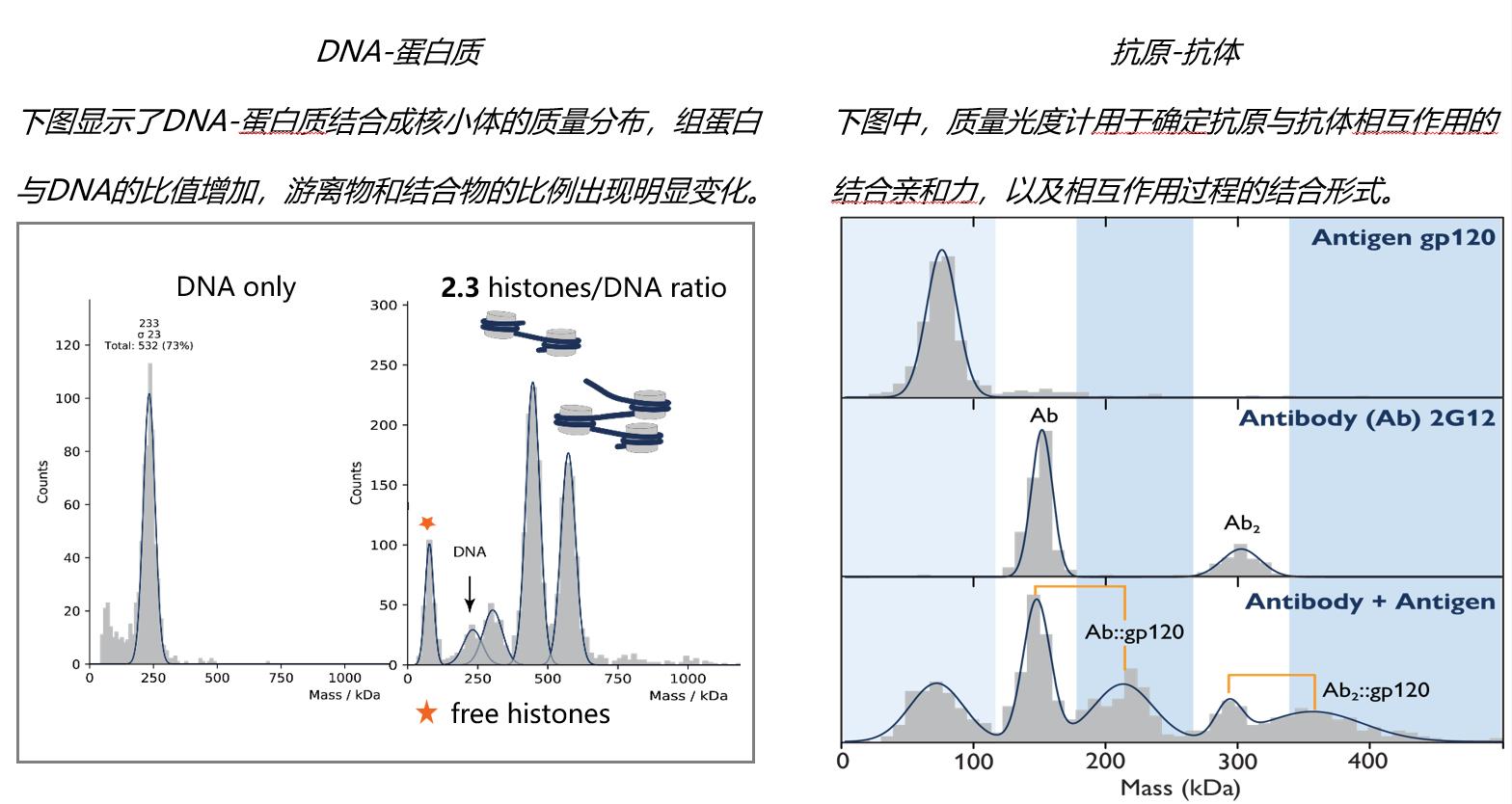
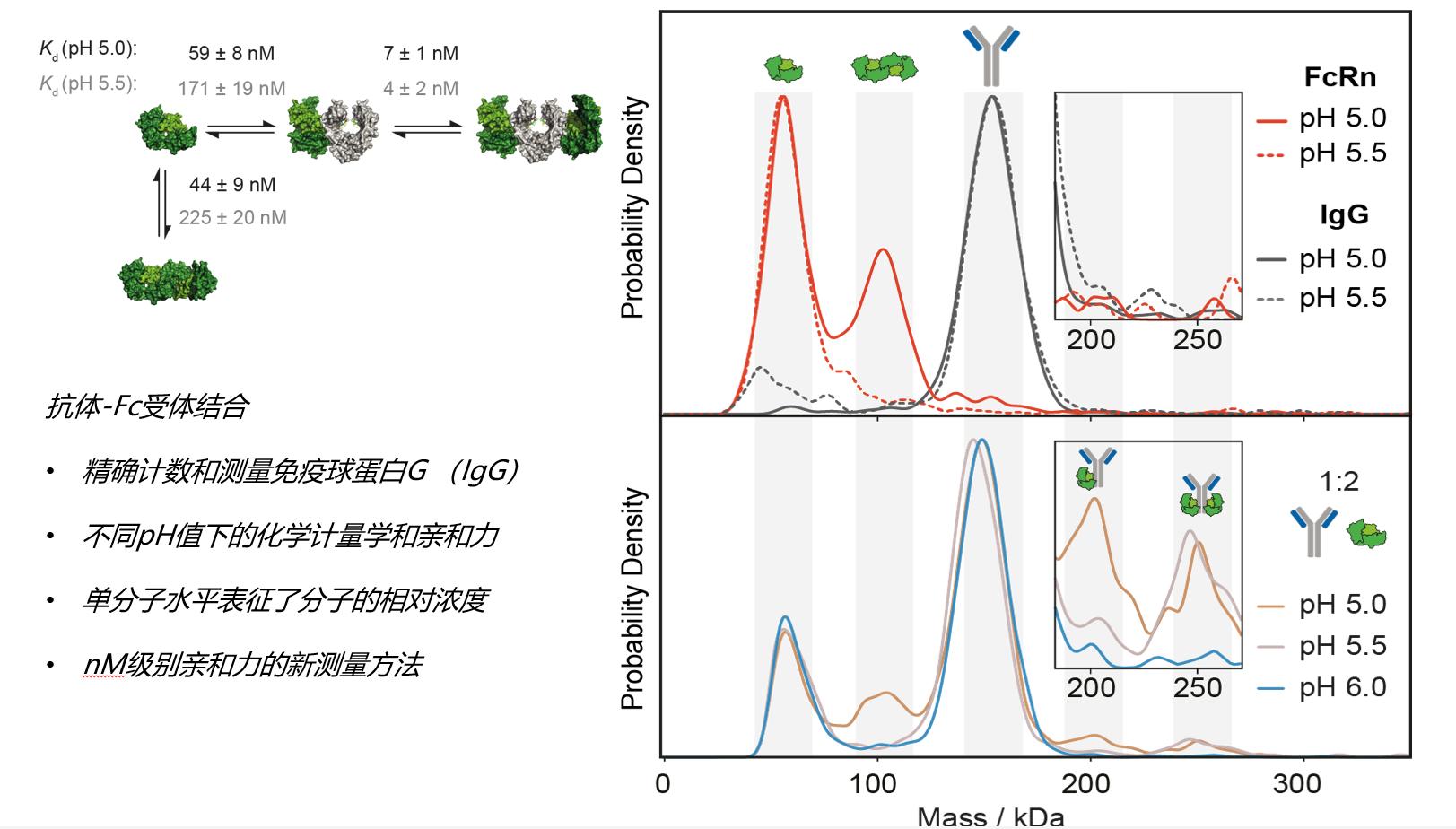
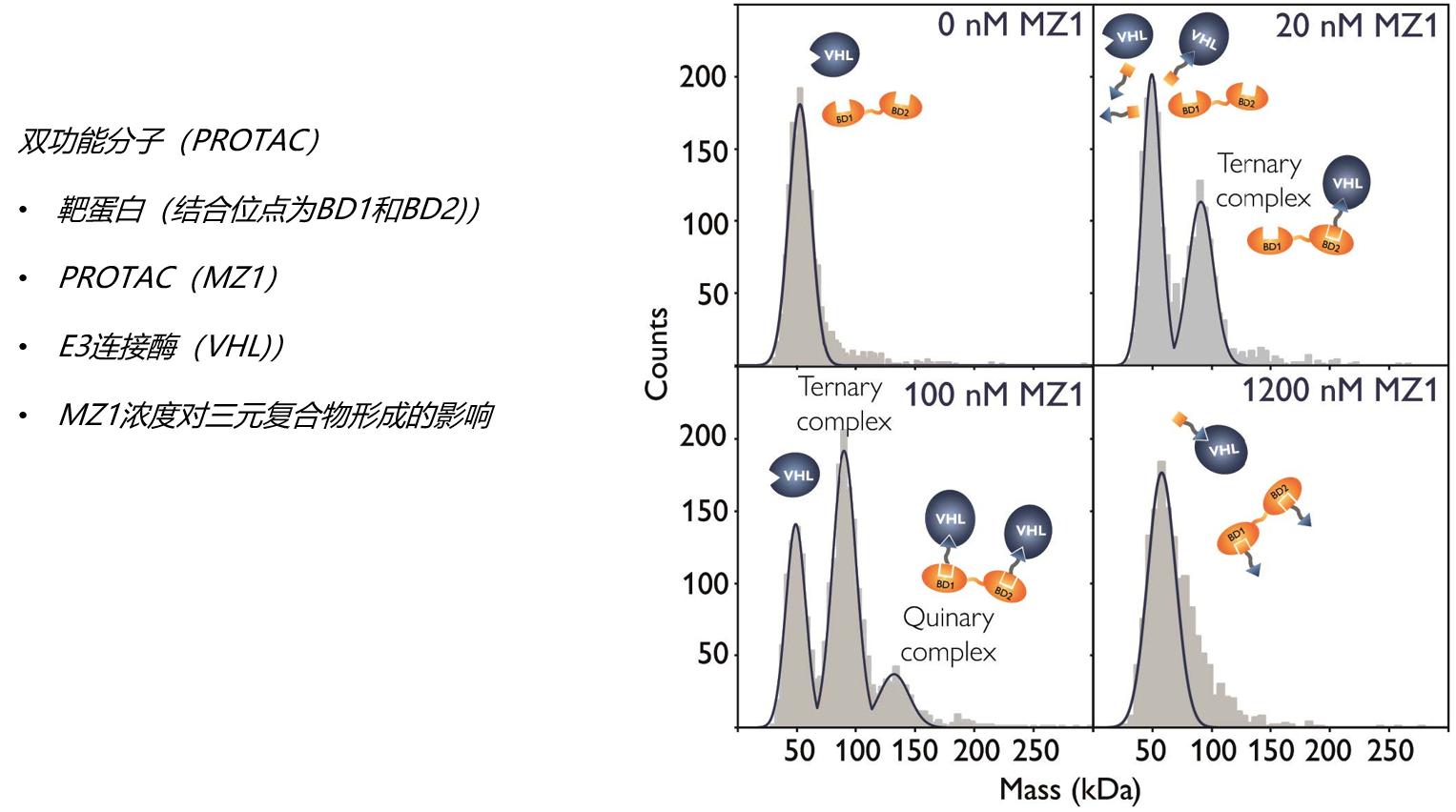
★ 蛋白质复合物的组装与化学计量 Macromolecular assemblies;
在分子自组装中,分子或分子的一部分在没有外部因素的情况下自发形成有序结构。大分子组合包括多种蛋白质,而且通常包含其他分子,如DNA、RNA、糖和/或脂类。大分子复合物在细胞内的组装是一个高度调控的多步骤过程。质量光度计能够高效、准确地表征这些复杂的粒子,使新型超分子结构的工程具有巨大的医学研究潜力。

用户评价
质量分布是蛋白质样品相对纯度和稳定性的基本特征,可作为蛋白质纯度、复杂组装、聚集或各种缓冲液中蛋白质-蛋白质相互作用的直观读数。监测质量可以指导缓冲条件的优化,避免蛋白质聚集或促进蛋白质复合物的稳定性和组装。单分子水平上的质量测量为分子相互作用的稳态分析提供了一种直接的方法。由于其高灵敏度,质量光度计TwoMP非常适合在生理(低)浓度下进行测量,而单分子计数技术固有的高动态范围确保低丰度分子仍能被准确捕获。
英国Refeyn公司首席营销官Matthias Langhorst表示,该工具的应用范围从简单的纯度检测(质量峰的数量可显示样本中有多少种蛋白质),到更复杂的分析,例如在不同条件下分析生物分子组装行为等。
在麻省理工学院研究细胞核孔复合体的Thomas Schwartz是该装置的早期测试者,他一听说质量光度测定法就联系Kukura:“这台仪器最有价值的地方在于,我们可以观察复杂的蛋白质-大分子复合物,找出混合物中的成分,是否能检测出任何与稳定性有关的问题。”“在典型的工作流程中,这是一个非常耗时的过程。”
“这些原理并不新鲜,但这种新装置的实现非常聪明和强大,因为它可以测量一个场中的每一个粒子。非常强大,具有潜在的革命性。”
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验The structural mechanism of dimeric DONSON in replicative helicase activation
Cvetkovic, M.A., Passaretti, P., Butryn, A., Reynolds-Winczura, A., Kingsley, G., Skagia, A., Fernandez-Cuesta, C., Poovathumkadavil, D., George, R., Chauhan, A.S., Jhujh, S.S., Stewart, G.S., Gambus, A., Costa, A.
Molecular Cell (2023)
Development of a 1:1-binding biparatopic anti-TNFR2 antagonist by reducing signaling activity through epitope selection
Akiba, H., Fujita, J., Ise, T., Nishiyama, K., Miyata, T., Kato, T., Namba, K., Ohno, H., Kamada, H., Nagata, S., & Tsumoto, K.
Communications Biology (2023)
The structural mechanism of dimeric DONSON in replicative helicase activation
Cvetkovic, M.A., Passaretti, P., Butryn, A., Reynolds-Winczura, A., Kingsley, G., Skagia, A., Fernandez-Cuesta, C., Poovathumkadavil, D., George, R., Chauhan, A.S., Jhujh, S.S., Stewart, G.S., Gambus, A., Costa, A.
Molecular Cell (2023)
Antagonistic roles of canonical and Alternative-RPA in disease-associated tandem CAG repeat instability
Gall-Duncan, T., Luo, J., Jurkovic, C., Fischer, L.A., Fujita, K., Deshmukh, A.L., Harding, R.J., Tran, S., Mehkary, M., Li, V., Leib, D.E., Chen, R., Tanaka, H., Mason, A.G., Lévesque, D., Khan, M., Razzaghi, M., Prasolava, T., Lanni, S., Sato, N., Pearson, C.E.
Cell (2023)
Structural insights into the complex of oncogenic KRas4BG12V and Rgl2, a RalA/B activator
Tariq, M., Ikeya, T., Togashi, N., Fairall, L., Kamei, S., Mayooramurugan, S., Abbott, L.R., Hasan, A., Bueno-Alejo, C., Sukegawa, S., Romartinez-Alonso, B., Muro Campillo, M.A., Hudson, A.J., Ito, Y., Schwabe, J.W.R., Dominguez, C., Tanaka, K.
Life Science Alliance (2023)
A morpheein equilibrium regulates catalysis in phosphoserine phosphatase SerB2 from
Pierson, E., De Pol, F., Fillet, M., & Wouters, J.
Communications Biology (2023)
Elucidation of structure–function relationships in Methanocaldococcus jannaschii RNase P, a multi-subunit catalytic ribonucleoprotein.
Phan, H., Norris, A.S., Du C., et al.
Nucleic Acids Research (2022)
Colocalized targeting of TGF-β and PD-L1 by bintrafusp alfa elicits distinct antitumor responses.
Lan, Y., Yeung, T., Huang, H., et al.
Journal for ImmunoTherapy of Cancer (2022)
Shelterin is a dimeric complex with extensive structural heterogeneity.
Zinder, J. C., Olinares P.D.B., Svetlov V., Bush, M. W., et al.
Proceedings of the National Academy of Sciences, Volume 119, Issue 31, e2201662119 (2022)
Diadenosine tetraphosphate regulates biosynthesis of GTP in Bacillus subtilis.
Giammarinaro, P.I., Young, M.K.M., Steinchen, W. et al.
Nat Microbiol (2022)
A haem-sequestering plant peptide promotes iron uptake in symbiotic bacteria.
Sankari, S., Babu, V.M.P., Bian, K. et al.
Nat Microbiol (2022)
Small-molecule screening of ribonuclease L binders for RNA degradation.
Borgelt, L., Haacke, N., Lampe, P., et al.
Biomedicine & Pharmacotherapy, Volume 154, 113589, ISSN 0753-3322, (2022)
Structural basis for shape-selective recognition and aminoacylation of a D-armless human mitochondrial tRNA.
Kuhle, B., Hirschi, M., Doerfel, L.K. et al.
Nat Commun 13, 5100 (2022)
Structure of a nucleosome-bound MuvB transcription factor complex reveals DNA remodelling.
Koliopoulos, M.G., Muhammad, R., Roumeliotis, T.I. et al.
Nat Commun 13, 5075 (2022)
Direct obsrvation of the molecular mechanism underlying protein polymerization.
Hundt N, Cole D, Hantke MF, Miller JJ, Struwe WB, Kukura P.
Sci Adv. 2022 Sep 2;8(35): eabm7935, (2022)
Elucidation of structure–function relationships in Methanocaldococcus jannaschii RNase P, a multi-subunit catalytic ribonucleoprotein.
Phan, H., Norris, A.S., Du C., et al.
Nucleic Acids Research (2022)
Colocalized targeting of TGF-β and PD-L1 by bintrafusp alfa elicits distinct antitumor responses.
Lan, Y., Yeung, T., Huang, H., et al.
Journal for ImmunoTherapy of Cancer (2022)
Shelterin is a dimeric complex with extensive structural heterogeneity.
Zinder, J. C., Olinares P.D.B., Svetlov V., Bush, M. W., et al.
Proceedings of the National Academy of Sciences, Volume 119, Issue 31, e2201662119 (2022)
Diadenosine tetraphosphate regulates biosynthesis of GTP in Bacillus subtilis.
Giammarinaro, P.I., Young, M.K.M., Steinchen, W. et al.
Nat Microbiol (2022)
A haem-sequestering plant peptide promotes iron uptake in symbiotic bacteria.
Sankari, S., Babu, V.M.P., Bian, K. et al.
Nat Microbiol (2022)
Small-molecule screening of ribonuclease L binders for RNA degradation.
Borgelt, L., Haacke, N., Lampe, P., et al.
Biomedicine & Pharmacotherapy, Volume 154, 113589, ISSN 0753-3322, (2022)
Structural basis for shape-selective recognition and aminoacylation of a D-armless human mitochondrial tRNA.
Kuhle, B., Hirschi, M., Doerfel, L.K. et al.
Nat Commun 13, 5100 (2022)
Structure of a nucleosome-bound MuvB transcription factor complex reveals DNA remodelling.
Koliopoulos, M.G., Muhammad, R., Roumeliotis, T.I. et al.
Nat Commun 13, 5075 (2022)
Direct o rvation of the molecular mechanism underlying protein polymerization.
Hundt N, Cole D, Hantke MF, Miller JJ, Struwe WB, Kukura P.
Sci Adv. 2022 Sep 2;8(35): eabm7935, (2022)
计校正匍聚糖的含水量,这点变得十分必要。在这里,贮存液是由含水量为 5% 的葡聚糖 T-500 制备而成。不同批次的葡聚糖 T-500 的分子质量也有差异。意味着,不同批次的葡聚糖 T-500,对层相分离系统的能力需要进行重新评估,并对层相分离系统组成进行必要的调整。 ( 2 ) 层相分离系统的贮存液分装后贮存于 -20°C。两相体系的构成以重量为基准,其体积取决于系统要承载多少膜材料。如表 11-3 显示了如何建立一个 27 g 的样本系统,并且该系统将与其后的 9 g 微粒体混合,从而最后
组等【1】 (图片来源:Wu RQ, J Dent Res. 2011) 1.质谱技术 质谱( Mass SPectrometry)是带电原子、分子或分子碎片按质荷比(或质量)的大小顺序排列的图谱。质谱仪是一类能使物质粒子高化成离子并通过适当的电场、磁场将它们按空间位置、时间先后或者轨道稳定与否实现质荷比分离,并检测强度后进行物质分析的仪器。质谱仪主要由分析系统、电学系统和真空系统组成。 1.1 质谱分析的基本原理 用于分析的样品分子(或原子)在离子源中离化成具有不同质量的单电行分子离子和碎片
[资源][原创] 蛋白标签纯化技术——CBP(钙调蛋白结合肽)
基于CBP标签技术的蛋白质表达与纯化系统 (用于高水平蛋白质表达和单步骤纯化)Protein Expression and Purification System是一种简单、温和、有效的方法,包括一个含有 calmodulin-binding peptide tag 钙调蛋白结合肽标签的pCAL 表达载体和一个用于分离的钙激酶亲合树脂,可快速敏感的捕捉标签融合蛋白。T7 RNA polymerase-based pCAL 载体能够快速克隆钙调蛋白结合肽标签融合蛋白。CBP标记的蛋白在低浓度钙
 技术资料
技术资料需要更多技术资料 索取更多技术资料










