相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
10
- 供应商:
广东固康生物科技有限公司
- 检测范围:
——
- 检测方法:
酶联免疫法
- 应用:
——
- 适应物种:
人
- 标记物:
——
- 样本:
血清
- 规格:
96人份(复孔检测样本:40个)/盒
【产品名称】
通用名称:阿狄科®血清S100A12蛋白检测试剂盒(酶联免疫法)
英文名称:IDK® S100A12 (Calgranulin C, EN-RAGE) (Serum)
【包装规格】
规格:96人份(复孔检测样本:40个)/盒
测试次数:96(40份样本一式两份)
【预期用途】
用于测定血清中的 S100A12。仅用于体外诊断。
【背景知识】
替代名称:Calgranulin C EN-RAGE
S100 蛋白家族的成员是具有细胞类型特异性表达和两个钙结合基序 (EF-Hande) 的小分子量酸性蛋白。 S100 蛋白质或钙颗粒被活化颗粒激活炎症组织中释放的细胞。此外,在慢性炎症中观察到浸润性单核细胞和粒细胞的表达增加。霍夫曼等人。 (1999) 将 RAGE(RAGE = 高级糖化终产物受体)确定为 S100A12 和 S100/钙颗粒蛋白超家族成员的主要受体,并将 S100A12 命名为 EN-RAGE(细胞外新鉴定的 RAGE 结合蛋白)。 S100A12 与细胞 RAGE 对内皮细胞、单核吞噬细胞和淋巴细胞的相互作用关键促炎介质的细胞活化和释放。
在小鼠模型中抑制 S100A12 通过阻断信号转导激活和炎症介质的表达来降低迟发性超敏反应和炎症性结肠炎。
由于 S100A12 由活化的中性粒细胞分泌并充当促炎介质,因此它可作为各种炎性疾病诊断和治疗控制的标志物(参见 Meijer 等人,2012 年的评论)。
适应症:
●急性炎症性疾病的炎症标志物
●评估炎症的严重程度 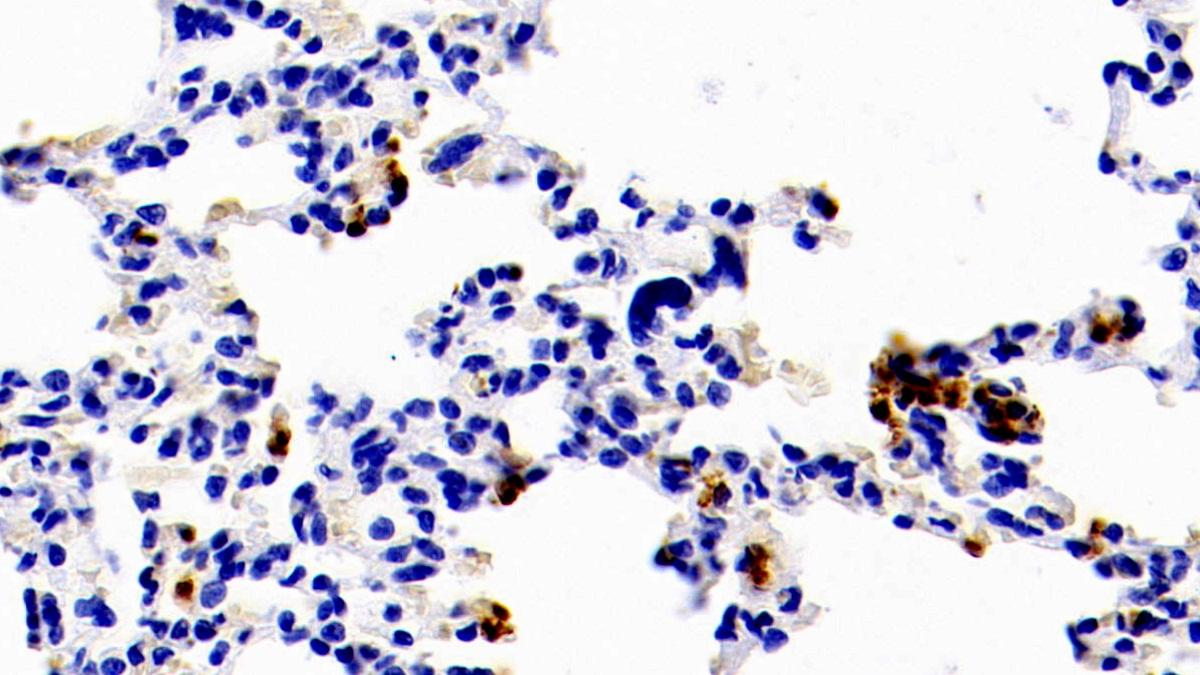
参考文献:
1. Hofmann MA, Drury S; Fu C, Qu W, Taguchi A, Lu Y, Avila C, Kambham N, Bierhaus A, Nawroth P, Neurath MF, Slattery T, Beach, D, McClary J, Nagashima M, Morser」Stern D, Schmidt AM. RAGE mediates a novel proinflammatory axis: a central cell surface receptor for S100/calgranulin polypeptides. Cell. 97: 889-901, 1999
2. Meijer, B., Gearry, R.B. & Day, A.S, 2012. The role of S100A12 as a systemic marker of inflammation. International journal of inflammation, 2012, p.907078. 
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验10% 胎牛血清。细胞培养物均根据 ATCC 的建议使用标准细胞培养方法维持和收获。 球状体形成的初始接种密度取决于细胞类型、球状体形式的生长期持续时间以及分析时球状体所需尺寸等因素。为更好地评估球状体的形成和生长,使用 96 孔球形微孔板在每孔 100 µL 生长培养基中以 40、200、1,000、5,000 和 10,000 个细胞的密度进行接种。通过CellTiter-Glo® 3D细胞活力测定法在 0、24、48 和 72 小时分别对球状体培养物进行分析。上述所有细胞系采用同一接种
,分子量 272.4 。主要由卵巢卵泡 Graffian 和胎盘分泌,肾上腺少量分泌。血液中 98%雌二醇 (E2) 主要与性激素结合球蛋白 (SHBG) 结合,以及少量的血清蛋白,如白蛋白。极少一部分成为游离激素。在靶器官,雌二醇受体联合体影响雌激素活性 . 这些器官包括卵泡、子宫、乳房、阴道、尿道、丘脑下部、垂体和肝脏,皮肤也有少量。 应用 本酶联免疫吸附测定试剂盒运用竞争抑制酶标免疫分析法定量测定牛奶中 E2 含量。试剂盒中包含 96 次检测所需的酶联免疫试验试剂,包括标准
CANDOR BIOSCIENCE: 关于ELISA板稳定性的技术探讨与比较
诊断试剂盒中试剂等组分的稳定性对于商业化的检测至关重要。现今稳定剂不仅可以延长保质期,而且可以提高检测试剂盒的可靠性。以SARS-CoV-2抗原为例,我们将解释商业化稳定剂如何在优化工作流程的同时提高分析质量。 如果在开发过程中没有充分考虑组分的稳定性,即使是技术上最先进、设计最完善的诊断检测,通常也无法实现商业化。根据将于2022年5月生效的欧盟体外诊断法规(IVDR),诊断试剂盒的分析性能在其保质期内不得改变。这使得组分的稳定性成为试剂盒进入市场的先决条件。通过使用商业化的蛋白质和结合
 技术资料
技术资料暂无技术资料 索取技术资料