万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
5×10⁵cells/T25
- 供应商:
沪震实业
- 肿瘤类型:
否
- 细胞类型:
原代细胞
- 品系:
原代细胞
- 组织来源:
脉络膜
- 相关疾病:
否
- 物种来源:
小鼠
- 免疫类型:
否
- 细胞形态:
电询
- 是否是肿瘤细胞:
不是
- 器官来源:
小鼠
- 运输方式:
干冰
- 年限:
5-10年
- 生长状态:
良好
- 规格:
5×10⁵cells/T25
| 原代细胞 | 细胞株 |
| 生长较快(5-7天铺满单层) | 较快 |
| 高 | 低 |
| 高 | 低 |
| 有限 | 较多 |
| 饱满且旋涡状排列 | 单薄且多颗粒物质 |
| 阳性反应强 | 阳性反应弱 |
| 细胞生长稳定良好 | 易发生形态生理变化 |
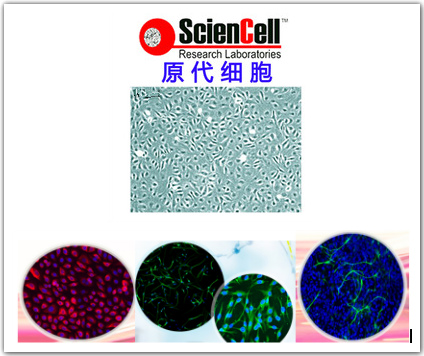
1.产品名称:小鼠脉络膜微血管内皮细胞
2.组织来源:脉络膜组织
3.产品规格:5×10^5cells/T25细胞培养瓶
小鼠脉络膜微血管内皮细胞4.细胞简介:
小鼠脉络膜微血管内皮细胞分离自眼球脉络膜组织;脉络膜在视网膜和巩膜之间,含有丰富血管和色素细胞,对外力冲击的耐受性较视网膜差,当眼球受到从前面来的外力的冲击作用通过玻璃体传到后极部时,坚硬的巩膜在其外面又有抵抗作用,使脉络膜在内外两种作用夹攻下而发生破裂和出血。脉络膜呈暗褐色,围绕视神经乳头部有照膜,为青绿色带金属光泽的三角形区。脉络膜是眼球中膜的后2/3处的薄膜,由纤维组织、小血管和毛细血管组成,软而薄,棕红色,在巩膜和视网膜之间,续连于睫状体后方。脉络膜的血循环营养视网膜外层,其含有的丰富色素起遮光暗房作用。主要功能是营养视网膜外层及玻璃体,并有遮光作用,使反射的物象清楚。同时对视觉系统起保护作用,对整个视觉神经有调节作用。续连于睫状体后方,含丰富的血管和色素细胞,有营养和遮光作用。
本公司生产的小鼠脉络膜微血管内皮细胞采用胶原酶-中性蛋白酶混合消化法结合密度梯度离心法、最后通过内皮细胞专用培养基培养筛选制备而来,细胞总量约为5×10^5cells/瓶;细胞经CD31/vWF免疫荧光鉴定,纯度可达90%以上,且不含有HIV-1、HBV、HCV、支原体、细菌、酵母和真菌等。
小鼠脉络膜微血管内皮细胞5.培养基信息:
M199、FBS、内皮细胞生长添加剂、Heparin、Ascorbic Acid、Hydrocortisone、Penicillin、Streptomycin等
我们推荐使用HZbscience小鼠脉络膜微血管内皮细胞专用完全培养基作为体外培养小鼠脉络膜微血管内皮细胞的培养基。
二、细胞培养状态
发货时发送细胞电子版照片
三、使用方法
在HZbscience技术部标准操作流程下,人肾动脉内皮细胞可传3-5代;建议您收到细胞后尽快进行相关实验。
客户收到细胞后,请按照以下方法进行操作。
1. 取出T25细胞培养瓶,用75%酒精消毒瓶身,拆下封口膜,放入37℃、5%CO2、饱和湿度的细胞培养箱中静置3-4h,以稳定细胞状态。
2. 待细胞达到80%汇合时准备进行传代培养。
3. 细胞传代
1) 吸出T25细胞培养瓶中的培养基,用PBS清洗细胞一次;
2) 添加0.25%胰蛋白酶消化液1mL至培养瓶中,轻微转动培养瓶至消化液覆盖整个培养瓶底后,吸出多余胰蛋白酶消化液,37℃温浴1-3min;倒置显微镜下观察,待细胞回缩变圆后,再加入5ml完全培养基终止消化;
3) 用吸管轻轻吹打混匀,按1:2-1:3适当的比例进行接种传代,然后补充新鲜的完全培养基至5mL,置于37℃、5%CO2、饱和湿度的细胞培养箱中静置培养;
4) 待细胞完全贴壁后,培养观察;之后每隔2-3天更换新鲜的完全培养基。
小鼠脉络膜微血管内皮细胞四、注意事项
1. 培养基于4℃条件下可保存3-6个月。
2. 在细胞培养过程中,请注意保持无菌操作。
3. 传代培养过程中,胰酶消化时间不宜过长,否则会影响细胞贴壁及其生长状态。
4. 建议客户收到细胞后前3天每个倍数各拍几张细胞照片,记录细胞状态,便于和HZbscience技术部沟通;由于运输的原因,个别敏感细胞会出现不稳定的情况,请及时和我们联系,详尽告知细胞的具体情况,以便我们的技术人员跟踪、回访直至问题得到解决。
5. 该细胞只可用于科研。
备注:由于实验所用试剂、操作环境及操作手法的不同,以上方法仅供各实验室参考
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验脑微血管内皮细胞是构成血脑屏障(blood-brain barrier,BBB)的重要成分,与外周血管内皮细胞不同,它具有高跨内皮阻抗(transendothelial electrical resistance,TER)、细胞间紧密连接、极少的胞饮小泡、缺乏窗孔结构以及含有选择性双向跨细胞膜转运系统等独有的特征,从而使血脑屏障形成一个限制大多数极性分子和蛋白质运动的选择性低渗透性的屏障[1]。由于体外培养的脑微血管内皮细胞保持了较多的其体内固有的特点[1],因此目前脑微血管内皮细胞
摘要: 目的 探讨脑微血管内皮细胞的体外培养方法并进行细胞超微结构研究及组织型纤溶酶原激活物(TPA ) 活性测定。 方法 取新生小鼠脑组织, 通过匀浆、过筛、胶原酶消化、差速粘附等技术对鼠脑微血管内皮细胞进行原代培养, 待细胞铺满瓶底时, 用01125%胰酶20102%EDTA 消化, 离心收集内皮细胞, 进行传代培养。原代、传代各取8 例, 吸取培养液用酶联免疫吸附试验测试TPA 活性。 结果 经Ð 因子相关抗原免疫组织化学鉴定、细胞超微结构观察, 证明培养的是血管内皮细胞。培养
原代微血管内皮 细 胞( Primary Microvascular Endothelial Cells )的体外分离培养 微血管内皮细胞生长因子的应用和免疫磁珠技术的发展,使微血管内皮细胞的培养和纯化变得相对简化。 1、微血管内皮细胞培养简述人体主要器官和组织的微血管内皮细胞已经培养成功的有:骨骼肌、心、脑、胃、视网膜、肺、皮肤、脉络膜、小肠、脂肪、肝窦、肾、关节滑膜、胎盘、骨髓、胰岛、角膜及食道等器官组织的微血管内皮细胞。 2、微血管内皮细胞的分离目前分离内皮细胞的方法主要有三种
 技术资料
技术资料暂无技术资料 索取技术资料