相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 英文名:
Mitophagy Detection Kit
- 供应商:
研卉生物
- CAS号:
MD01
- 规格:
1set
- Mitophagy Detection Kit线粒体自噬检测试剂盒
-
货号: MD01
线粒体(mitochondria)是细胞内制造能量的场所,在细胞器中扮演着重要的角色。近年有报告指出,去极化线粒体的积累引起的阿尔茨海默病(Alzheimer‘s disease)与帕金森病(Parkinson’s disease),可能与线粒体自噬有关。通过线粒体自噬(mitophagy)系统,将氧化应激、DNA损伤因素导致的去极化线粒体,隔离包裹成自噬体(autophagosome)后、再与溶酶体(lysosome)融合后降解。本试剂盒包括“线粒体自噬体染料(Mtphagy Dye)和溶酶体染料(Lyso Dye)。MtphagyDye通过化学键结合在细胞内的线粒体上,保持较弱的荧光。通过诱导线粒体自噬,线粒体自噬体会与溶酶体融合,Mtphagy Dye的荧光强度会增大。通过本试剂盒包含的Lyso Dye,单独标记溶酶体,来确认这一融合过程。常见问题Q&A
Q1: 本试剂盒和现存传统方法相比有何优势?
A1: 与PH敏感并基于Keima荧光蛋白检测方法相比,本试剂为小分子荧光试剂,因此无需表达荧光蛋白。
另外,可以通过与用于普通活细胞成像的荧光试剂用相同的操作方法对其进行染色和共同观察。
Q2: 使用DMSO配置后的储存液稳定性如何? A2:Mtphagy Dye、Lyso Dye均在制备后需保存在-20℃情况下可以稳定保存1个月。建议按照实验用量,
提前分装保存。
Q3: 工作液稳定性如何
A3: 无法保存,建议现配现用。 Q4: 培养基中有酚红会影响检测吗?
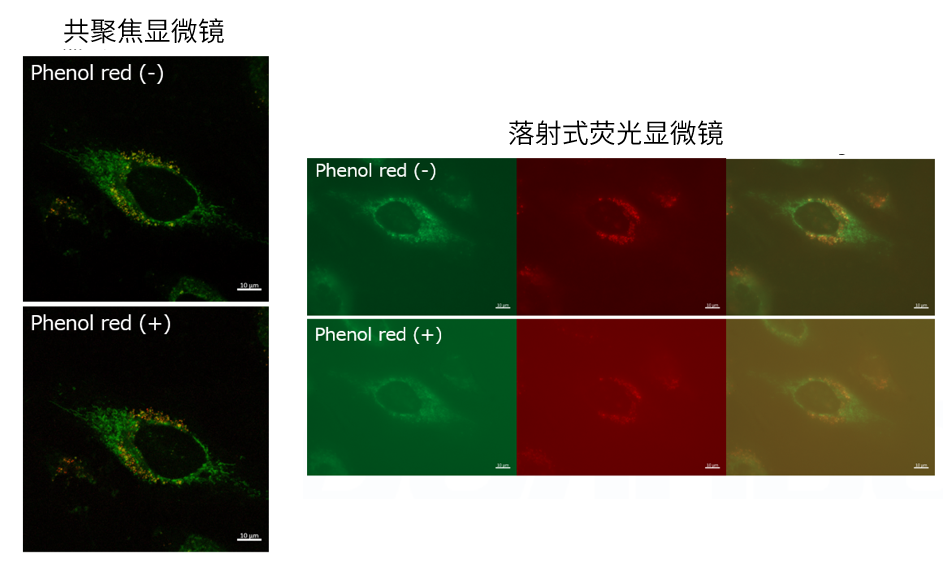
A4:观察的时候,如果使用共聚焦激光显微镜的话,几乎不会受到酚红的影响,但是使用落射型荧光显微
镜的话,会观察到酚红色的背景。(参照以下观察数据)因此使用落射型荧光显微镜时,请在Working
solution进行染色时使用不含酚红的培养基或HBSS。
Q5: 荧光显微镜推荐的滤镜是什么?
A5:根据各种试剂推荐以下波长。 Mtphagy Dye:激发(500~560 nm)、发射(670~730 nm)
Lyso Dye:激发(350~450 nm)、发射(500~560 nm)
Q6:与其他深红色染料共同染色时的注意事项。 A6:Mtphagy Dye比一般的红色系荧光染料相比波长更长,所以和Deep Red的荧光染料一起染色的时候
需要特别注意。即Mtphagy Dye在500–560 nm处激发,可在670-730 nm处检测到荧光,这时与
MitoBright Deep Red的荧光检测波长重叠。因此,有必要在不激发深红色染料的波长下激发Mtphagy
染料,同时在不激发Mtphagy染料的波长下激发深红色染料。
[泄漏的情况]
① 制备仅添加了MitoBright Deep Red(没有添加Mtphagy Dye)的细胞。
② 通过观察MitoBright Deep Red的激发/发射波长,确认是否观察到荧光(右下图)。
③ 用Mtphagy Dye的激发/发射波长观察,确认是否观察到荧光(左下图)。
和③中,观察到来自MitoBright Deep Red的荧光(左下图)。
*如果如上所述确认荧光泄漏,请参阅以下内容。
○调整激发/发射波长
如以上确认如图所示,MitoBright Deep Red也在Ex 561 nm处激发,因此可以将Mtphagy Dye的激发
波长更改为接近激光器或滤光片的500 nm,以使MitoBright深红色不被激发。
调整荧光强度和荧光检测灵敏度
如果MitoBright Deep Red的荧光泄漏到Mtphagy染料的观察波长中,请将观察过程中的激发强度或
灵敏度降低到未观察到荧光的水平。
然后,再确认改变后的观察条件下可以检测Mtphagy Dye的荧光。
[如何检查泄漏]
使用Mtphagy Dye,Lyso dye(溶酶体染色剂),MitoBrightLT Deep Red(线粒体染色剂)
进行三重染色时进行确认
1.在3个培养皿或孔中制备细胞。
(Mtphagy Dye、Lyso Dye、MitoBright Deep Red分别在在不同的皿或孔中进行染色)
2.向每个孔中添加Mtphagy Dye和MitoBright Deep Red。 (在无血清培养基中)
3.在37°C下孵育30分钟。
4.进行自噬诱导条件下(如饥饿培养等)进行培养。
5.向上述2.中未使用的细胞添加Lyso Dye。(在无血清培养基中)
6.在37°C下孵育30分钟。
7.观察每种试剂的激发波长和荧光波长以及荧光强度。
8.检查所用试剂以外的观察波长处的荧光是否没有泄漏。
[观察条件]
Lyso Dye:Ex:350-450 nm,Em:500-560 nm
Mtphagy Dye:Ex : 500-560 nm,Em :670-730 nm
MitoBright Deep Red:Ex :640 nm,Em :656-700 nm
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验参考文献
Dynabeads® Co-Immunoprecipitation Kit
, although the coupling reaction also works well with antibodies in storage buffers that include protein additives (e.g. BSA) and/or sodium azide (NaN3). This kit is not recommended for use with antibodies that have been stabilized in glycerol. 实验试剂
c-kit Mutational Analysis in Paraffin Material
The current WHO classification of mastocytosis defines one major and four minor diagnostic criteria for systemic mastocytosis (SM). One of the minor criteria is the detection of the “gain-of-function” mutation D816V of the c -kit proto
, without the use of strong chaotropic agents. The protocol is flexible and can easily be scaled up or down to suit all sample sizes. It has successfully been used in the isolation of mRNA from single cells. The high capture efficiency facilitates detection of mRNA