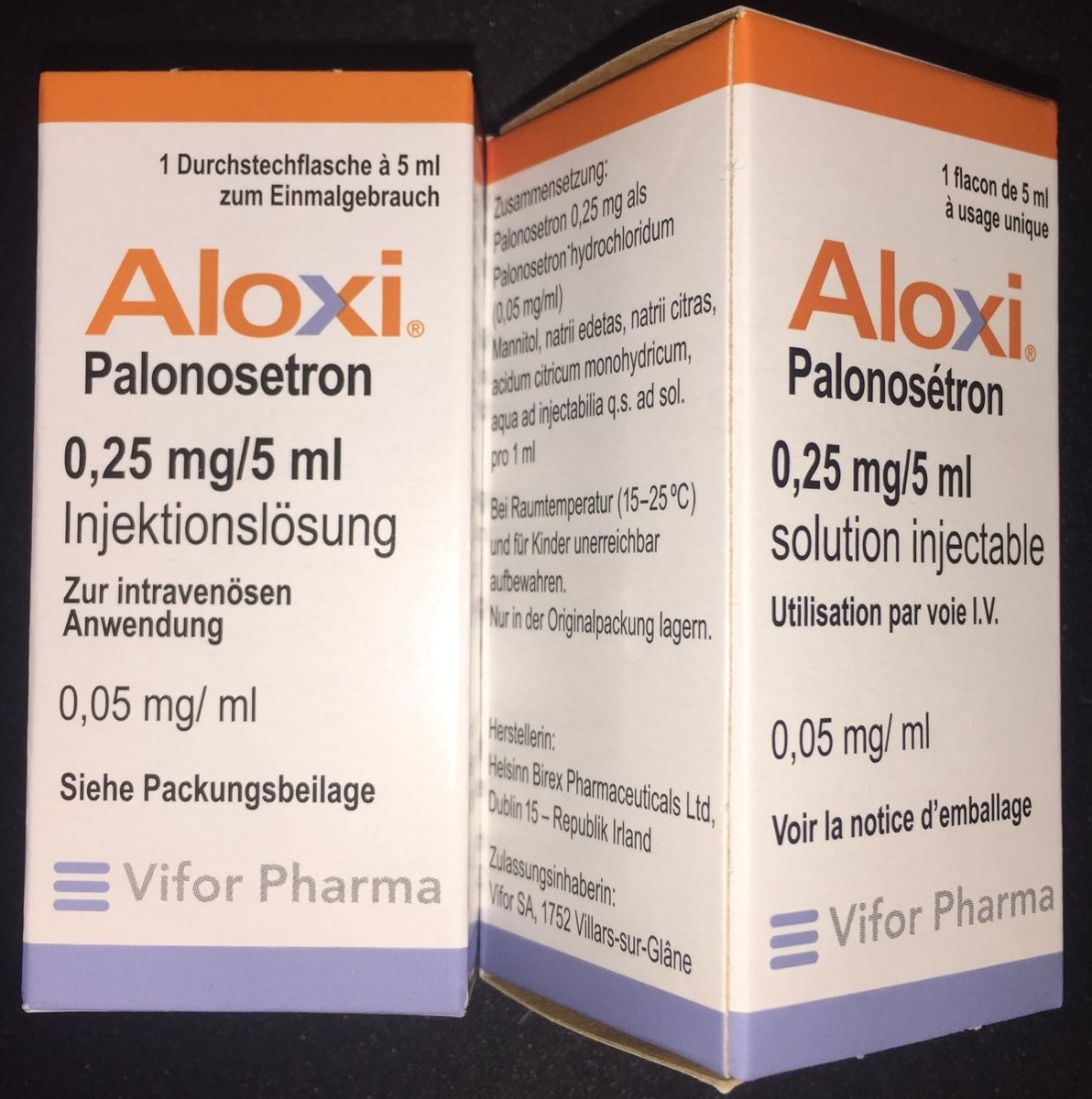
Aloxi盐酸帕罗司琼-原研参比制剂
- ¥1000 - 1500
- Aloxi
- 爱尔兰/瑞士
- 57042
- 2025年07月16日
相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 技术资料
- 英文名:
Palonosetron
- 供应商:
Vifor
美国食品和药品管理局(FDA)已经批准盐酸帕洛诺司琼(Aloxi,Eisai公司和Helsinn集团)注射剂在1个月到不足17岁的儿童中用于预防化疗引起的恶心和呕吐(CINV)。
帕洛诺司琼被批准用于预防由致吐性化疗(包括高致吐性化疗)初期和重复使用引起的急性恶心和呕吐。
这是第一款批准用于1到6个月儿童急性CINV的药品。根据该公司解释,因为在儿童生命的第一年是癌症发病率的高峰期,针对这一年龄组的批准是很重要的。
由化疗引起的恶心和呕吐的预防在儿童中仍然未满足需要,尽管有可用的治疗,”Riccardo Braglia(Helsinn集团首席执行官)在一份新闻稿中这样表示。“这一批准为CINV预防提供了一种新的治疗选择。”
CINV是接受癌症化疗患者最常见的不良反应之一,根据报道,发生在30%~80%的癌症儿童中。
该公司为响应一份来自FDA的书面要求开展了4项儿童临床试验。这一批准根据来自一项随机,双盲,非劣性关键试验的数据回顾,该试验比较了在化疗前30分钟内单剂量静脉注射帕洛诺司琼20μg/kg和化疗前30分钟内静脉注射昂丹司琼0.15mg/kg的标准治疗方案序贯昂丹司琼首剂量后4小时和8小时输注。该研究的主要终点是完全缓解,研究人员将化疗后最初24小时内无呕吐,无干呕,和不需要止吐救助定义为完全缓解。研究的主要终点在那些接受药物患者的59.4%中完成 vs 58.6%接受昂丹司琼方案的患者。
在两组之间,治疗出现的不良反应事件(TAEs)发生率具有可比性。报告称帕洛诺司琼组最常见TAE是头痛。研究表明,儿童患者需要根据体重比成人预防CINV需要更高剂量,但是研究证实这种安全特性与已知成人范围是相一致的。
临床试验数据符合FDA书面要求,满足儿童用药需求,因此该药物额外有6个月的美国市场专有权,将在2015年10月13日到期。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期