相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
102
- 英文名:
Porcine Circovirus type I Detection Kit
- 保质期:
1年
- 供应商:
上海晅科生物科技有限公司
- 保存条件:
-20℃
- 规格:
50T
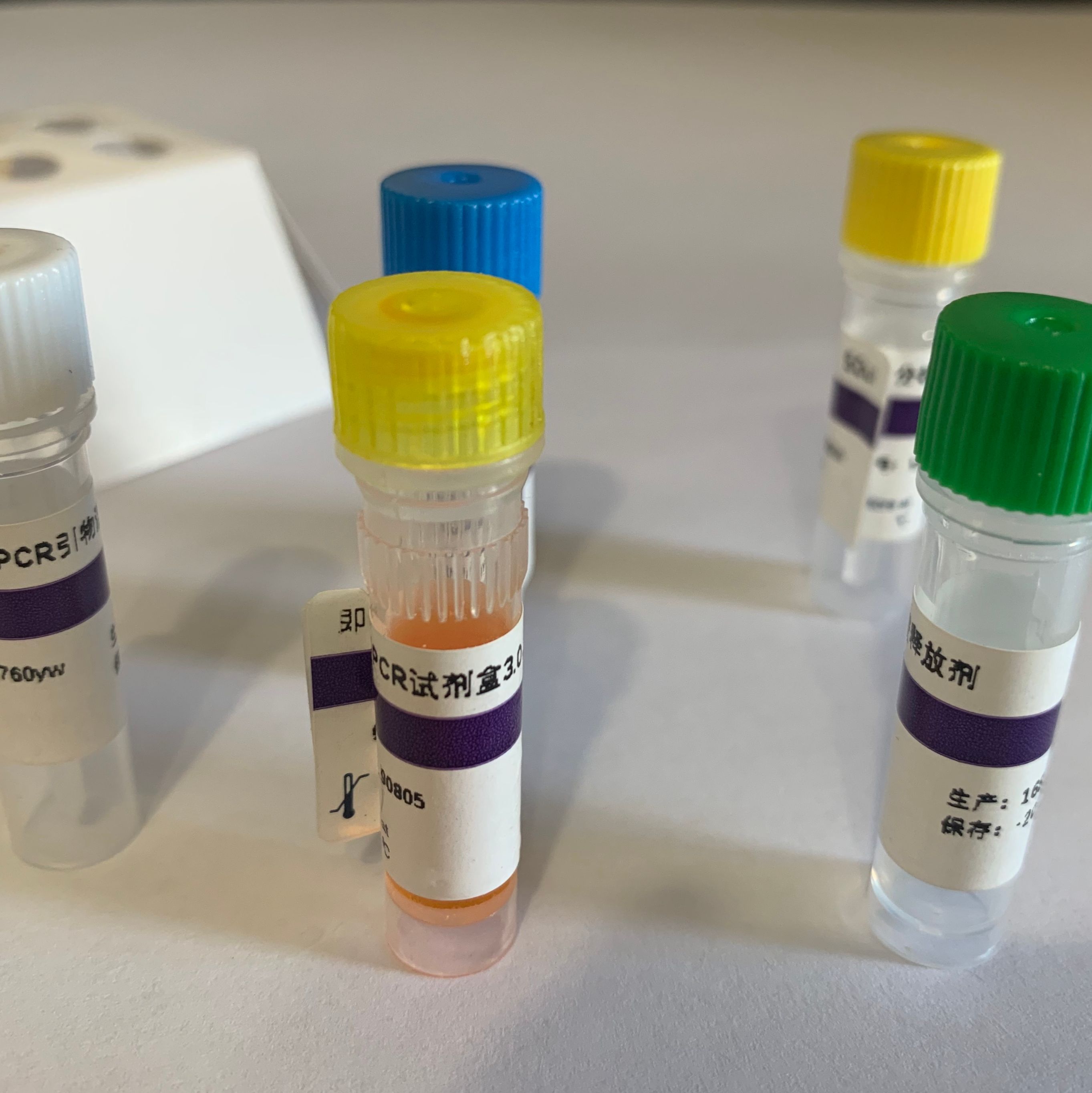
英文名称:Porcine Circovirus type I Detection Kit
猪圆环病是由猪圆环病毒(Porcine Circovirus)引起猪的一种传染性、先天性颤抖和断奶仔猪多系统功能障碍性疾病。该病毒具有 PCV1 和 PCV2 两种血清型,PCV1 无致病性。 本试剂盒适用于病死猪(包括流产的死胎)或扑杀猪主要脏器(淋巴结、脾脏、肺脏、肾脏和肝脏),血清等样 本中的猪圆环病毒 1 型,用于猪圆环病毒 1 型感染的辅助诊断。
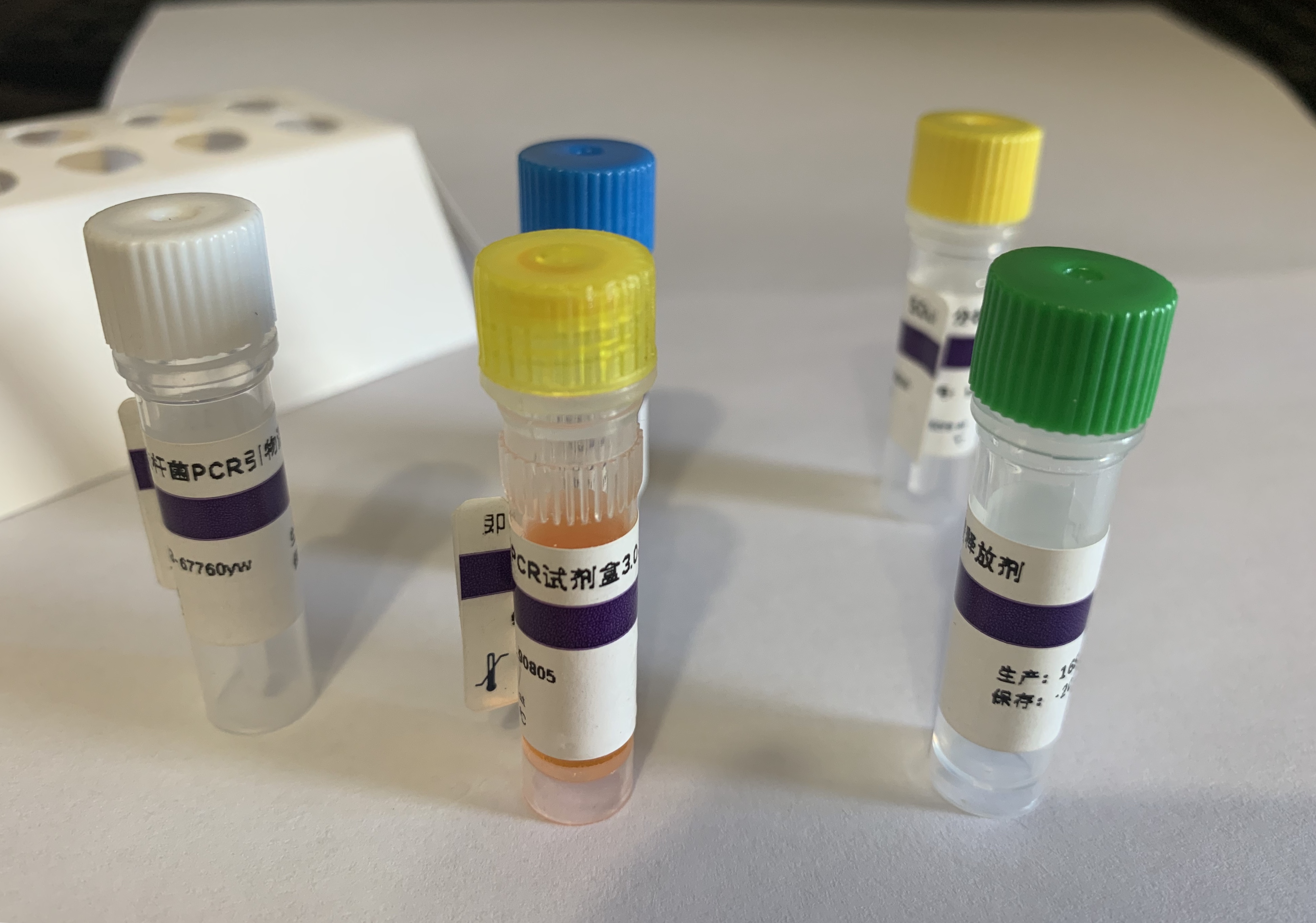
本试剂盒采用 TaqMan 探针法实时荧光 PCR 技术,设计一对猪圆环病毒 1 型特异性引物,结合一条特异性探针,用荧光 PCR 技术对猪圆环病毒 1 型的 DNA 进行体外扩增检测,用于对可疑感染病料的病原学检测。
猪圆环病毒1型(PCV-1)核酸检测试剂盒(探针法荧光PCR)试剂组成:
| 包装规格 | 25T/盒 | 50T/盒 |
| PCV-1 反应液 | 500μL×1 管 | 500μL×2 管 |
| 酶液 | 25μL×1 管 | 50μL×1 管 |
| PCV-1 阳性质控品 | 250μL ×1 管 | 250μL ×1 管 |
| 阴性质控品 | 250μL ×1 管 | 250μL ×1 管 |
储存条件及有效期:-20℃±5℃,避光保存、运输、反复冻融次数不超过 5 次,有效期 12 个月。
适用仪器:ABI7500、安捷伦 MX3000P/3005P、LightCycler、Bio-Rad、Eppendorf 等系列荧光定量 PCR 检测仪。
标本采集:组织样品采集:采取病死猪(包括流产的死胎)或扑杀猪主要脏器(淋巴结、脾脏、肺脏、肾脏和肝脏)装入灭 菌 15 mL 离心管中,编号,送实验室。血清样品采集:用无菌注射器抽取受检猪静脉血不少于 5 ml,置于无菌 离心管内,室温或者 37℃倾斜放置自然凝集 20 min ~30 min,2 000 r/min~3 000 r/min 离心 10 min,吸取上清液 到新的离心管内备用。精液样品采集:按照 GB/T 25172 的方法采集和保存精液。粪便样品采集:取猪新鲜粪便 1 g,装入 15 mI 灭菌离心管中,加入 5 mL PBS,混匀。细胞培养物:细胞培养物反复冻融 3 次,第 3 次解冻后, 将细胞培养物置于 1.5 mL 无 DNA 酶的灭菌离心管内,编号备用。
保存和运输:采集或处理好的样品在 2℃~8℃条件下保存应不超过 24 h;若需长期保存,应放置-70℃以下保存,冻融不超过 3 次。
使用方法:
1. 样品处理(样本处理区)
1.1 样本前处理 组织样品:取 1 g 解冻的组织,剪碎,加入 2 mL PBS 进行研磨,制备组织匀浆,8000 r/min 离心 5 min,取上清用于后续的核酸提取。血清和精液样品无需进行前处理,直接用于核酸提取。粪便样品:3000 r/min 离心 10 min,取上清液,转入 1.5 mL 离心管中,用于后续的核酸提取。细胞培养物:4000 r/min,4℃离心 l0 min,取上清用于后续的核酸提取。
1.2 核酸提取 推荐采用公司生产的核酸提取或纯化试剂(磁珠法或离心柱法)进行核酸提取,请 按照试剂说明书进行操作。
2. 试剂配制(试剂准备区) 根据待检测样本总数,设所需要的 PCR 反应管管数为 N(N=样本数+1 管阴性对照+1 管阳性对照;反应管数每满 10 份,多配制 1 份),每测试反应体系配制如下表: 试剂 PCV-1 反应液 酶液 用量 19μL 1μL 将混合好的测试反应液分装到 PCR 反应管中,20μL/管。
3. 加样(样本处理区) 将步骤 1 提取的核酸、阳性质控品、阴性质控品各取 5μL,分别加入相应的反应管中,盖好管盖,混匀,短暂离心。
4. PCR 扩增(核酸扩增区)
4.1 将待检测反应管置于荧光定量 PCR 仪反应槽内;
4.2 设置好通道、样品信息,反应体系设置为 25μL; 荧光通道选择: 检测通道(Reporter Dye)FAM, 淬灭通道(Quencher Dye)NONE,ABI 系列仪器请勿选择 ROX 参比荧光,选择 None 即可。
4.3 推荐循环参数设置: 步骤 循环数 温度 时间 收集荧光信号 1 1 cycle 95℃ 2min 否 2 45 cycles 95℃ 15sec 否 60℃ 30sec 是
5. 结果分析判定
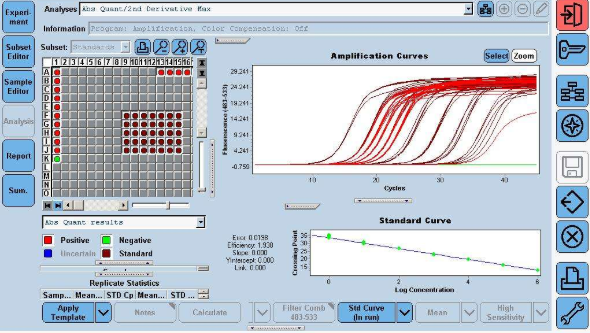
5.1 结果分析条件设定(请参照各仪器使用说明书进行设置,以分析 ABI7500 仪器为例) 反应结束后自动保存结果,根据分析后图像调节 Baseline 的 Start 值、End 值以及 Threshold 值(用户可根据实际情况自行调整,Start 值可设在 3~15、End 值可设在 5~20,使阈值线位于扩增曲线指数期,阴性质控品的扩增曲线平直或低于阈值线),点击 Analyze 自动获得分析结果。
5.2 结果判断 阳性:检测通道 Ct 值≤40,且曲线有明显的指数增长曲线; 阴性:样本检测结果无 Ct 值,且无特异性扩增曲线; 可疑:样本检测结果 40<Ct 值≤45,建议重复检测,如果检测通道仍为 40
5.3 质控标准 阴性质控品:无特异性扩增曲线或无 Ct 值显示; 阳性质控品:扩增曲线有明显指数增长期,且 Ct 值≤32; 以上条件应同时满足,否则实验视为无效。
6. 检测方法的局限性
1. 样本检测结果与样本收集、处理、运送以及保存质量有关;
2. 样本提取过程中没有控制好交叉污染,会出现假阳性结果;
3. 阳性对照、扩增产物泄漏,会导致假阳性结果;
4. 病原体在流行过程中基因突变、重组,会导致假阴性结果;
5. 不同的提取方法存在提取效率差异,会导致假阴性结果;
6. 试剂运输,保存不当或试剂配制不准确引起的试剂检测效能下降,出现假阴性或定量检测不准确的结果;
7. 本检测结果仅供参考,如须确诊请结合临床症状以及其他检测手段。
注意事项
1. 所有操作严格按照说明书进行;
2. 试剂盒内各种组分使用前应自然融化,完全混匀并短暂离心;
3. 反应液应避光保存;
4. 反应中尽量避免气泡存在,管盖需盖紧;
5. 使用一次性吸头、一次性手套和各区专用工作服;
6. 样本处理、试剂配制、加样需在不同区进行,以免交叉污染;
7. 实验完毕后用 10%次氯酸或 75%酒精或紫外灯处理工作台和移液器;
8. 试剂盒里所有物品应视为污染物对待,并按照《微生物生物医学实验室生物安全通则》进行处理。
相关产品:
| 抗水解随机引物(6碱基,硫代法),0.1 mM |
| 甜菜碱溶液(PCR和LAMP级,5M) |
| T7体外转录及加帽试剂盒 |
| T3体外转录及加帽试剂盒 |
| SP6体外转录及加帽试剂盒 |
| RNA GpppG帽甲基化试剂盒(Cap0 RNA甲基化试剂盒)( Cap0 RNA加Cap1试剂盒) |
| SP6体外转录试剂盒 |
| 亚硫酸氢盐修饰DNA试剂盒 (凝胶法) |
| Proteinase K Solution 蛋白酶K溶液,10mg/mL |
| 病毒DNA纯化试剂盒(沉淀法) |
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验(beads)为基质,微球悬浮于液相体系,每种微球可根据不同研究目的标定上特定抗体或受体探针,可对同一样品中多个不同的分子同时进行检测。微球表面可进行一系列修饰以适合固定各种蛋白、多肽或核酸等生物分子。xMAP技术可应用于蛋白或核酸的功能及其相互作用研究,分别称之为液相蛋白芯片技术和液相基因芯片技术。液相蛋白芯片体系主要包括微球、蛋白探针分子、被检测物和报告分子四种成分。在液相系统中,为了区分不同的探针,每一种用于标记探针的微球都带有独特的色彩编码,其原理是在微球中掺入不同比例的红色分类荧光及发色剂
酸和天冬氨酸以外的任意一种氨基酸)N--糖基化序列的特异天冬酰胺残基上开始,当新合成的蛋白质进入内质网腔后就发生 N 端序列糖基化反应(图 25-1B )。接着,当糖蛋白从内质网经高尔基体到达其最终目的地时,Glc3Man9GlcNAC2 前体沿着分泌途径进行进一步加工处理。如果糖基侧链能被内质网和高尔基体中的糖苷酶和糖基转移酶加工的话,Glc3Man9GlcNAc2 前体就会被成功转化为 Man9GlcNAc2 和 Man5GlcNAC2 范围内的髙甘露糖型 N-聚糖(图 25-1A), 以及复杂
-4,单以氨基酸顺序推测编码的DNA序列是不精确的,但可以设计成对兼并引物,扩增所有编码已知顺序的核酸序列。用兼并引物时寡核苷酸中核苷酸序列可以改变,但核苷酸的数量应相同。兼并度越低,产物特异性越强,设计引物时应尽量选择兼并性小的氨基酸,并避免引物3’末端兼并,针对兼并的混合引物已成功地用于未知靶DNA的扩增、克隆和序列分析。现已成功地克隆了猪尿酸氧化酶基因、糖尿病相关肽基因和哺乳动物与禽类的嗜肝病毒基因。用脱氧肌苷(deoxyinosine;DI)引物进行PCR,可以代替编码蛋白的多种兼并密码子中的
 技术资料
技术资料暂无技术资料 索取技术资料