相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
100
- 英文名:
Seneca virus A,SVA
- 保质期:
1年
- 供应商:
上海晅科生物科技有限公司
- 保存条件:
-20℃
- 规格:
50次
英文名称:Seneca virus A,SVA
荧光定量PCR( realtime fluorescence quantitative PCR,RTFQ PCR) 是1996 年由美国Applied Biosystems 公司推出的一种新定量试验技术,它是通过荧光染料或荧光标记的特异性的探针,对PCR产物进行标记跟踪,实时在线监控反应过程,结合相应的软件可以对产物进行分析,计算待测样品模板的初始浓度。为此本公司开发了简单快捷的塞内卡病毒A PCR 检测试剂盒。
产品特点:
1. 即开即用,用户只需要提供病毒样品。
2. 根据塞内卡病毒A保守序列设计的专一性引物,与相关病毒无交叉反应。
3. 灵敏度可以达到几百拷贝/反应。
4. 一管式荧光定量 PCR 检测,避免后续污染。
5. 本试剂盒足够 50 次 20μL 反应体系的荧光定量 PCR。
6. 本产品只适用于科研,不能用于临床诊断。
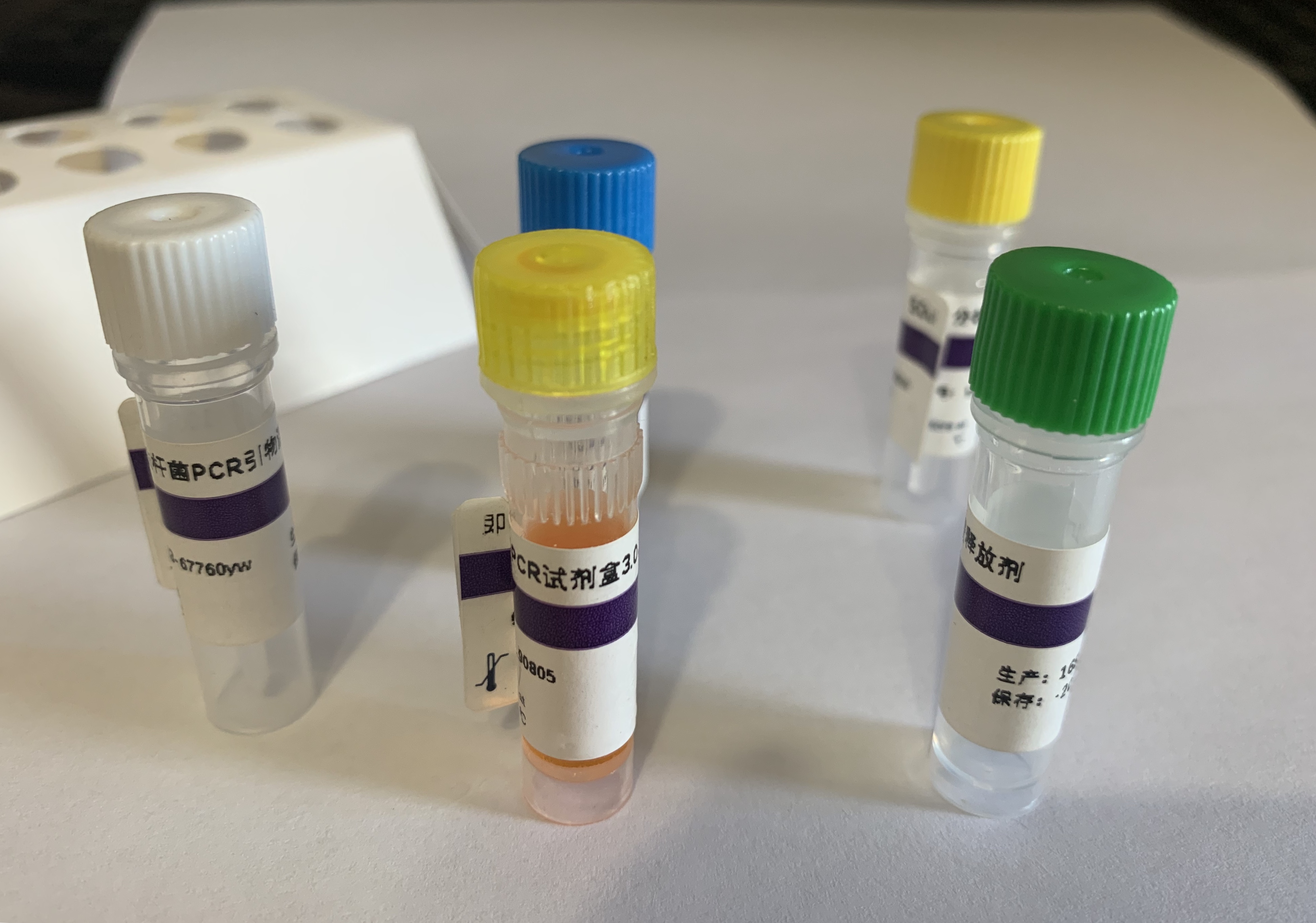
塞内卡病毒A(Seneca virus A,SVA)RT-PCR试剂盒包装规格及成分:
| 编号 |
成分 |
规格 |
| 试剂一 |
PCR MagicMix 3.0 | 1 mL(红盖) |
| 试剂二 |
超纯水 | 1 mL(亮黄色) |
| 试剂三 |
塞内卡病毒APCR 引物混合液 | 100 μL(白盖) |
| 试剂四 |
塞内卡病毒APCR 阳性对照 (1×10E8 拷贝/μL) | 50 μL(黄盖) |
| 试剂五 |
使用手册 | 1 份 |
运输及保存:低温运输,-20℃保存,保存期限为一年。阳性对照需要单独放置,不要污染其 他试剂。
自备试剂:DNA 模板
使用方法:
一、样品 DNA 的制备
1. 用自选方法纯化 N+2 个样品的 DNA,本试剂盒跟市场上大多数核酸提取试剂盒兼容。
2. 如果有 N 个样品,则需要做 N+2 个提取,包括一个样品制备阳性对照和一 个样品制备阴性对照。样品制备阳性对照是在适量水(取决于试剂盒要求 的样品起始量)中加 10μL 塞内卡病毒APCR 阳性对照的 1000 倍稀释液 而得,样品制备阴性对照是直接用水。提取结束后最后得到模板 DNA 放冰 上待用。
二、设置 PCR 反应(40μL 体系)
3. 对 N+2 个样品,在 PCR 时需要增加一个 PCR 阳性对照和一个 PCR 阴性 对照,故需要设置 N+4 个反应。在 N+4 个 PCR 管中分别加入下列成分:
| 成分 | N+2 个 样品管 | PCR 阴性 对照 | PCR 阳性 对照 |
| PCR Magic Mix 3.0 | 各 20 μL | 20 μL | 20 μL |
| 塞内卡病毒APCR 引物 混合液 | 各 2 μL | 2 μL | 2 μL |
| N+2 个样品 DNA 模板 | 各 18 μL | ||
| PCR 阴性对照(水) | 18 μL | ||
| PCR 阳性对照(塞内卡病毒APCR 阳性对照的 1000 倍稀释液) | 18 μL |
4. 按下表设置 PCR 反应:
| 过程 | 温度 | 时间 |
| 预变性 | 95℃ | 5 min |
| PCR 反应 (35 个循环) | 95℃ | 30 sec |
| 55℃ | 30 sec | |
| 72℃ | 30 sec | |
| 最后延伸 | 72℃ | 7 min |
三、电泳检测 5. 取 10-20 μL PCR 产物。1%琼脂糖凝胶电泳检测 PCR 产物。本产品提供的 PCR Mix 在扩增结束后可以直接上样,不需要另外再加 loading buffer。阳性对照必须有预期条带出现,阴性对照必须无任何扩增,否则实 验无效。对没有扩增产物的样品,可以稀释 10 倍后重复 PCR 扩增以排 除 PCR 抑制剂的感染。

塞内卡病毒A(Seneca virus A,SVA)RT-PCR试剂盒相关产品:
| 产品名称 |
方法 |
产品规格 |
价格 |
| 塞内卡病毒ALAMP试剂盒 | LAMP |
50次 |
2490 |
| 塞内卡病毒APCR试剂盒 | PCR |
50次 |
1990 |
| 塞内卡病毒A染料法荧光定量PCR试剂盒 | 染料法 |
50次 |
2490 |
| 鲍疱疹样病毒探针法荧光定量PCR试剂盒 | 探针法 |
50次 |
2990 |
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验PCR仪 PCR/RT-PCR/qPCR试剂 PCR引物 PCR试剂 PCR对照 特异性PCR试剂盒 PCR克隆试剂盒 RNA
Core Sample PCR: A method to re-PCR unique bands from products of mixed size
PCR仪 PCR/RT-PCR/qPCR试剂 PCR引物 PCR试剂 PCR对照 特异性PCR试剂盒 PCR克隆试剂盒 RNA RNase检测/去除 RT-PCR试剂 RT-PCR标准品
。 【产品研发意义】 埃博拉出血热(EHF)是由埃博拉病毒(Ebola virus,EBOV)引起的一种急性出血性传染病,发病率快,致死率高,是人类危害最严重的传染病之一,对公共卫生安全和人类的健康有很大的威胁。 到目前为止,EHF还没有有效治疗的药物和疫苗。我国尚未有检测到EBOV病毒,为了防止EBOV进入我国,建立一种快速、准确、敏感的检测方法显得尤为重要。为此,我公司研制出埃博拉病毒Z亚型核酸荧光PCR检测试剂盒、埃博拉病毒Z、S亚型双重核酸荧光PCR检测试剂盒和埃博拉病毒Z、S、B、C、R